¿Qué es el acetato de etilo?
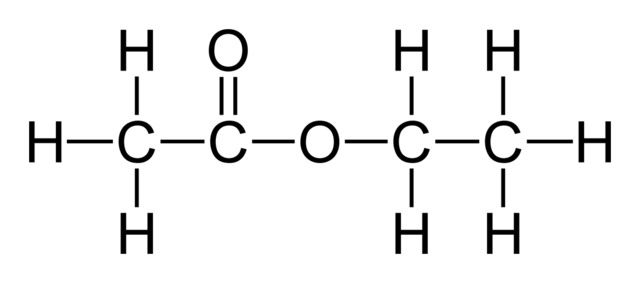
El acetato de etilo o etanoato de etilo es un compuesto orgánico cuya fórmula química es CH3COOC2H5. Consiste en un éster, donde el componente alcohólico deriva del etanol, mientras que su componente ácido carboxílico proviene del ácido acético.
Es un líquido bajo condiciones normales de temperatura y presión, presentando un aroma agradable a frutas. Esta propiedad entra perfectamente en armonía por lo que se espera de un éster, que es de hecho la naturaleza química del acetato de etilo. Por esta razón encuentra uso en productos alimenticios y bebidas alcohólicas.
En la imagen superior se muestra el esqueleto estructural del acetato de etilo. Nótese a la izquierda su componente ácido carboxílico, y a la derecha el componente alcohólico. Desde un punto de vista estructural, podría esperarse que este compuesto se comportara como un híbrido entre el vinagre y el alcohol, sin embargo, exhibe propiedades específicas de él.
Es aquí donde tales híbridos llamados ésteres se destacan por ser diferentes. El acetato de etilo no puede reaccionar como un ácido, ni tampoco deshidratarse por la ausencia de un grupo OH. En lugar de eso, sufre hidrólisis básica en presencia de una base fuerte, como hidróxido de sodio, NaOH.
Esta reacción de hidrólisis se utiliza en los laboratorios de docencia para los experimentos de cinética química, donde la reacción, además, es de segundo orden. Cuando ocurre la hidrólisis, prácticamente el etanoato de etilo regresa a sus componentes iniciales: el ácido (desprotonado por el NaOH), y el alcohol.
En su esqueleto estructural se observa que predominan los átomos de hidrógeno sobre los de oxígeno. Esto influye en su capacidad para interaccionar con especies no tan polares como las grasas. Asimismo, se emplea para disolver compuestos como las resinas, colorantes, y en general, sólidos orgánicos. Por ello se utiliza como disolvente en las artes plásticas.
A pesar de tener un aroma agradable, una prolongada exposición a este líquido genera un impacto negativo (como casi todos los compuestos químicos) en el organismo.
Estructura del acetato de etilo
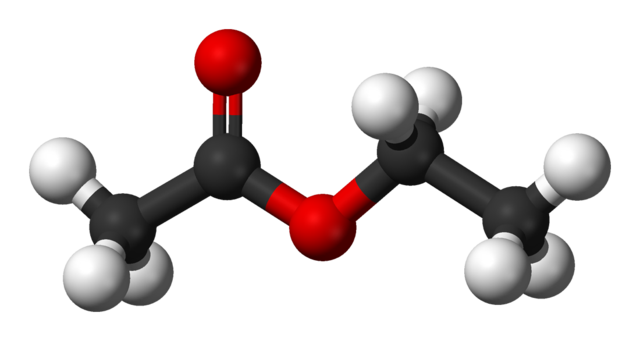
En la imagen superior se muestra la estructura del acetato de etilo con un modelo de esferas y barras. En este modelo se resaltan los átomos de oxígeno con esferas rojas. A su izquierda está la fracción derivada del ácido, y a su derecha la fracción derivada del alcohol (grupo alcoxi, -OR).
El grupo carbonilo se aprecia por el enlace C=O (las dobles barras). La estructura en torno a este grupo y el oxígeno adyacente es plana, debido a que hay una deslocalización de la carga por resonancia entre ambos oxígenos, hecho que explica una relativamente baja acidez de los hidrógenos α (los del grupo -CH3, enlazado al C=O).
La molécula, al rotar dos de sus enlaces, favorece directamente en cómo interacciona con otras moléculas. La presencia de los dos átomos de oxígeno, y la asimetría en la estructura, le confieren un momento dipolar permanente, que, a su vez, es responsable de sus interacciones tipo dipolo-dipolo.
Por ejemplo, la densidad electrónica es mayor cerca de los dos átomos de oxígeno, disminuyendo considerablemente en el grupo -CH3, y paulatinamente en el grupo OCH2CH3.
Debido a estas interacciones, las moléculas de acetato de etilo forman un líquido en condiciones normales, el cual tiene un punto de ebullición considerablemente alto (77 °C).
Ausencia de átomos donadores de puentes de hidrógeno
Si se observa detenidamente la estructura, se notará la ausencia de un átomo capaz de donar un puente de hidrógeno. Sin embargo, los átomos de oxígeno son aceptores de tal, y por el acetato de etilo es muy soluble en agua, e interacciona en un grado estimable con compuestos polares y donadores de puentes de hidrógeno (como los azúcares).
Asimismo, esto le permite interaccionar excelentemente con el etanol, razón por la cual no se extraña su presencia en las bebidas alcohólicas.
Por otro lado, su grupo alcoxi lo vuelve capaz de interaccionar con ciertos compuestos apolares, tales como el cloroformo, CH3Cl.
Propiedades físicas y químicas
- Nombres: acetato de etilo; etanoato de etilo; éster etil acético; acetoxietano.
- Fórmula molecular: C4H8O2 o CH3COOC2H5
- Peso molecular: 88,106 g/mol.
- Descripción física: líquido incoloro claro.
- Color: líquido incoloro.
- Olor: característico de los éteres, semejante al olor de la piña.
- Sabor: agradable cuando se diluye, aporta un sabor a fruta a la cerveza.
- Umbral de olor: 3,9 ppm. 0,0196 mg/m3 (olor bajo); 665 mg/m3 (olor alto). Olor detectable a 7-50 ppm (media = 8 ppm).
- Punto de ebullición: 171 °F a 760 mmHg (77,1 °C).
- Punto de fusión: -118,5 °F (-83,8 °C).
- Solubilidad en agua: 80 g/L.
- Solubilidad en solventes orgánicos: miscible con etanol y éter etílico. Muy soluble en acetona y benceno. Miscible además con cloroformo, aceites fijos y volátiles, y también con solventes oxigenados y clorinados.
- Densidad: 0,9003 g/cm3.
- Densidad del vapor: 3,04 (en relación aire:1).
- Estabilidad: se descompone lentamente con la humedad; incompatible con varios plásticos y agentes oxidantes fuertes. La mezcla con el agua puede ser explosiva.
- Presión de vapor: 93,2 mm Hg a 25 °C.
- Viscosidad: 0,423 mPoise a 25 °C.
- Calor de combustión: 2.238,1 kJ/mol.
- Calor de vaporización: 35,60 kJ/mol a 25 °C.
- Tensión superficial: 24 dinas/cm a 20 °C.
- Índice de refracción: 1,373 a 20 °C/D.
- Temperatura de almacenamiento: 2-8 °C.
- pKa: 16-18 a 25 °C.
Síntesis
Reacción de Fisher
El etil acetato es sintetizado industrialmente mediante la reacción de Fisher, en la cual se esterifica el etanol con el ácido acético. La reacción se realiza a temperatura ambiente.
CH3CH2OH + CH3COOH <=> CH3COOCH2CH3 + H₂O
La reacción se acelera por catálisis ácida. El equilibrio se desplaza a la derecha, es decir, hacia la producción de etil acetato, mediante la remoción de agua, de acuerdo a Ley de Acción de Masa.
Reacción de Tishchenko
También se prepara industrialmente el acetato de etilo empleando la reacción de Tishchenko, conjugándose dos equivalentes de acetaldehído con el uso de un alcóxido como catalizador.
2 CH3CHO => CH3COOCH2CH3
Otros métodos
- Se sintetiza acetato de etilo como un coproducto en la oxidación de butano a ácido acético, en una reacción realizada a una temperatura de 175 °C y 50 atm de presión. Se usa como catalizador al cobalto y iones de cromo.
- El acetato de etilo es un coproducto de la etanólisis del acetato de polivinilo a alcohol polivinílico.
- También se produce en la industria el acetato de etilo mediante la deshidrogenación de etanol, catalizándose la reacción mediante el uso del cobre a una temperatura elevada, pero inferior a 250 °C.
Usos
- Solvente: el acetato de etilo es utilizado como disolvente y diluyente, empleándose en la limpieza de tableros de circuitos. Se usa como solvente en la fabricación del extracto de lúpulo modificado, y en el descafeinado del café y de las hojas de té. Se usa en las tintas para marcar frutas y verduras. El acetato de etilo es empleado en la industria textil como un agente limpiante, en la calibración de termómetros, en la separación de azúcares. En la industria de las pinturas, se utiliza como disolvente y diluyente de los materiales.
- Sabores artificiales: se utiliza en la elaboración de sabores de frutas. Por ejemplo: banana, pera, durazno y piña, así como aroma de uva, etc.
- Analíticos: se emplea en la determinación de bismuto, boro, oro, molibdeno y platino, así como disolvente del talio. El acetato de etilo tiene la capacidad de extraer muchos compuestos y elementos presentes en solución acuosa, tales como: fósforo, cobalto, tungsteno y arsénico.
- Síntesis orgánicas: el acetato de etilo se emplea en la industria como un reductor de la viscosidad de las resinas para las formulaciones fotorresistentes. Se usa en la producción de acetamida, acetato de acetilo y metil heptanona.
- Cromatografía: en los laboratorios se utiliza el acetato de etilo como fase móvil de las cromatografías en columnas y como solvente de extracción. Al tener el acetato de etilo un punto de ebullición relativamente bajo, es de fácil evaporación, lo que permite concentrar las sustancias disueltas en el solvente.
- Entomología: se utiliza en entomología para asfixiar los insectos colocados en un recipiente, lo que permite su recolección y estudio. Los vapores de acetato de etilo matan al insecto sin destruirlo y evitando su endurecimiento, facilitando su montaje para colección.
Riesgos
- El LD50 del acetato de etilo en ratas, indica una toxicidad baja. Sin embargo, puede irritar la piel, los ojos, la piel, la nariz y garganta.
- La exposición a niveles elevados puede causar mareo y desmayo. Asimismo, la exposición a largo plazo puede afectar el hígado y el riñón.
- La inhalación de acetato de etilo a una concentración de 20.000-43.000 ppm, puede producir edema pulmonar y hemorragia.
- El límite de exposición laboral, ha sido fijado por la OSHA en 400 ppm en el aire, como promedio, durante un turno laboral de 8 horas.
Referencias
- Illustrated Glossary of Organic Chemistry: ethyl acetate (EtOAc). Recuperado de chem.ucla.edu.
- Ethyl acetate. Recuperado de chm.bris.ac.uk.