¿Qué es el ácido peryódico?
El ácido peryódico es un oxácido, que se corresponde con el estado de oxidación VII del yodo. Existe en dos formas: el ortoperyódico (H5IO6) y el ácido metaperyódico (HIO4). Fue descubierto en 1838 por los químicos alemanes H. G. Magnus y C. F. Ammermüller.
En disoluciones acuosas diluidas, el ácido peryódico se encuentra principalmente bajo la forma de ácido metaperyódico y ion hidronio (H3O+). Mientras, en disoluciones acuosas concentradas, el ácido peryódico se presenta como ácido ortoperyódico.
Ambas formas del ácido peryódico están presentes en un equilibrio químico dinámico, dependiendo de la forma preponderante del pH existente en la disolución acuosa.
El H5IO6 puede expresarse como HIO4∙2H2O, y, por lo tanto, hay que deshidratarlo para obtener el HIO4; lo mismo sucede en sentido inverso, al hidratar el HIO4 se produce el H5IO6.
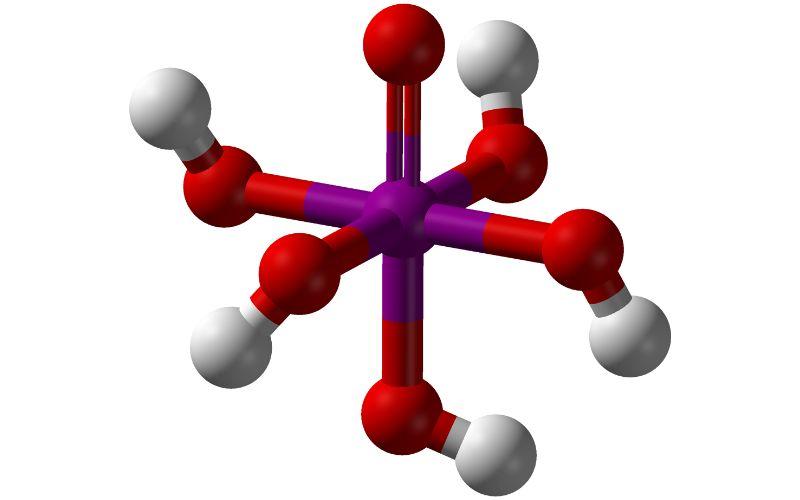
Estructura del ácido peryódico
La estructura del ácido peryódico consiste en un tetraedro en cuyo centro se sitúa el átomo de yodo, y en sus vértices los átomos de oxígeno. Tres de los átomos de oxígeno forman un doble enlace con el yodo (I=O), mientras que uno de ellos forma un enlace simple (I-OH).
Esta molécula es ácida por la presencia del grupo OH, siendo capaz de donar un ion H+; y aún más cuando la carga parcial positiva del H es más grande debido a los cuatro átomos de oxígeno enlazados al yodo. El HIO4 puede formar cuatro puentes de hidrógeno: uno a través del OH (dona) y tres por sus átomos de oxígeno (acepta).
Estudios cristalográficos han demostrado que el yodo puede de hecho aceptar dos oxígenos de una molécula vecina de HIO4. Al hacerlo, se obtienen dos octaedros IO6, unidos por dos enlaces I-O-I en posiciones cis. Es decir, se encuentran en un mismo lado y no están separados por un ángulo de 180°.
Estos octaedros IO6 se enlazan de tal manera que terminan creando cadenas infinitas, que al interaccionar entre sí “arman” el cristal de HIO4.
Ácido ortoperyódico
El ortoperyódico (H5IO6), es la forma más estable e hidratada del ácido peryódico.
Hay cinco grupos OH, correspondientes a los cinco iones H+ que teóricamente pudiera liberar la molécula de H5IO6. No obstante, debido a las crecientes repulsiones electrostáticas, solamente puede liberar tres de esos cinco, estableciendo diferentes equilibrios de disociación.
Estos cinco grupos OH le permiten al H5IO6 aceptar varias moléculas de agua, y es por esta razón que sus cristales son higroscópicos, es decir, absorben la humedad presente en el aire. Asimismo, estos son responsables de su punto de fusión considerablemente alto para un compuesto de naturaleza covalente.
Las moléculas de H5IO6 forman entre sí muchos puentes de hidrógeno, y, por lo tanto, otorgan una direccionalidad tal que les permite además disponerse ordenadamente en el espacio. Como resultado de dicho ordenamiento, el H5IO6 forma cristales monoclínicos.
Propiedades
- Pesos moleculares: ácido metaperyódico: 190,91 g/mol. Ácido ortoperyódico: 227,941 g/mol.
- Apariencia física: sólido blanco o amarillo pálido, para el HIO4, o cristales incoloros, para el H5IO6.
- Punto de fusión: 128 °C (263,3 °F, 401,6 °F).
- Punto de ignición: 140 °C.
- Estabilidad: estable. Oxidante fuerte. En contacto con materiales combustibles puede originar fuego. Higroscópico. Incompatible con materiales orgánicos y agentes reductores fuertes.
- pH: 1,2 (solución de 100 g/L de agua a 20 °C).
- Reactividad: el ácido peryódico es capaz de romper el enlace de dioles vecinales presentes en carbohidratos, glucoproteínas, glucolípidos, etc., originando fragmentos moleculares con grupos terminales aldehídos.
- Esta propiedad del ácido peryódico es empleada en la determinación de la estructura de los carbohidratos, así como de la presencia de sustancias relacionadas con estos compuestos.
- Los aldehídos formados por esta reacción pueden reaccionar con el reactivo de Schiff, detectándose la presencia de carbohidratos complejos (se colorean de púrpura). El ácido peryódico y el reactivo de Schiff se acoplan en un reactivo que se abrevia como PAS.
Nomenclatura
Tradicional
El ácido peryódico tiene su nombre debido a que el yodo trabaja con la mayor de sus valencias: el +7 (VII). Este es el modo de nombrarlo de acuerdo a la vieja nomenclatura (la tradicional).
En los libros de química siempre colocan al HIO4 como el único representante del ácido peryódico, siendo sinónimo del ácido metaperyódico.
El ácido metaperyódico debe su nombre al hecho de que el anhídrido yódico reacciona con una molécula de agua, esto es, su grado de hidratación es el más bajo:
I2O7 + H₂O => 2HIO4
Mientras que para la formación del ácido ortoperyódico, el I2O7 debe reaccionar con una cantidad de agua superior:
I2O7 + 5H2O => 2H5IO6
Reaccionando con cinco moléculas de agua en lugar de una.
El término orto-, se utiliza exclusivamente para referirse al H5IO6, y por eso el ácido peryódico alude solo al HIO4.
Sistemática y stock
Otros nombres, menos comunes, para el ácido peryódico son:
- tetraoxoyodato (VII) de hidrógeno.
- ácido tetraoxoyódico (VII).
Usos
Médicos
- Las tinciones púrpuras de PAS obtenidas por la reacción del ácido peryódico con los carbohidratos se usan en la confirmación de una enfermedad de almacenamiento de glucógeno. Por ejemplo, la enfermedad de Von Gierke.
- Se usa en las afecciones médicas siguientes: enfermedad de Paget, sarcoma de la parte blanda alveolar, detección de agregados de linfocitos en la micosis fungoides y en el síndrome de Sezany.
- También se emplea en el estudio de la eritroleucemia, una leucemia de glóbulos rojos inmaduros. Las células se tiñen de un color fucsia brillante. Además, se utiliza en el estudio las infecciones con hongos vivos, tiñéndose las paredes de los hongos de un color magenta.
En el laboratorio
- Se utiliza en la determinación química del manganeso, además de su uso en la síntesis orgánica.
- El ácido peryódico se usa como un oxidante selectivo en el campo de las reacciones de la química orgánica.
- El ácido peryódico puede producir la liberación de acetaldehído y aldehídos superiores. Además, puede liberar formaldehído para su detección y aislamiento, así como la liberación de amoníaco de los hidroxiaminoácidos.
- Las soluciones de ácido peryódico se utilizan en el estudio de la presencia de aminoácidos que tienen grupos OH y NH2 en posiciones adyacentes. La solución de ácido peryódico se usa en forma conjunta con carbonato de potasio. Al respecto, la serina es el hidroxiaminoácido más simple.
Referencias
- Periodic acid. Recuperado de en.wikipedia.org.