¿Qué es el buffer de fosfatos?
El buffer de fosfatos, BPS o buffer fosfato salino, es una solución amortiguadora e isotónica, cuya función es mantener el pH y la presión osmótica lo más parecido al ambiente biológico natural (fisiológico). Las siglas PBS significan Phosphate Buffered Saline.
El pH y la osmolaridad son dos aspectos muy importantes que deben controlarse en ciertos protocolos de laboratorio. En el caso del pH, es imprescindible que sea controlado, especialmente en reacciones bioquímicas, ya que estas pueden variar o no ejecutarse si los reactantes están en un pH inadecuado.
En tanto que el control de la osmolaridad es esencial sobre todo cuando se trabaja con células vivas, pues las membranas plasmáticas de las células reaccionan de acuerdo a la concentración de solutos en la que se encuentren.
Si las células son trasladadas a un medio hipertónico, se deshidratarán, ya que el gradiente de agua se transportará a donde hay mayor concentración de solutos. Si, por el contrario, se colocan células en un medio hipotónico, las células absorberán líquido hasta lisarse.
Es por ello que se utiliza el buffer PBS para protocolos de laboratorio que requieren el mantenimiento de células in vitro, de esta manera las células no se dañarán.
El PBS está compuesto por una combinación de sales, como cloruro de sodio, fosfato de sodio, cloruro de potasio y fosfato de potasio. La composición del PBS puede variar dependiendo del protocolo.
Fundamento del buffer de fosfatos
Básicamente, la función del buffer fosfato salino es mantener un pH fisiológico constante junto a una concentración electrolítica similar a la que se encuentra en el interior del organismo.
En este ambiente las células son capaces de mantenerse estables, pues se simulan en lo posible las condiciones fisiológicas.
A la formulación original del PBS pueden agregarse otros compuestos de ser necesarios, por ejemplo, la adición de EDTA al buffer es útil para el lavado de glóbulos rojos en la prueba de incompatibilidad cruzada.
El EDTA impide que la fracción del complemento C1 presente en el suero, se escinda y lise a los glóbulos rojos, es decir, evita resultados falsos de incompatibilidad. Además, el EDTA ayuda a disociar a las células.
Preparación del buffer de fosfatos
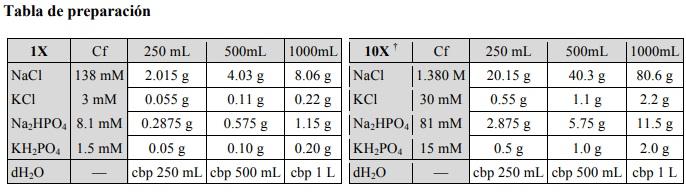
La cantidad de sales que se deben pesar para la elaboración del buffer fosfato salino PBS dependerá de la cantidad que se requiera preparar:
Solución madre buffer fosfato salino (PBS 10X)
Para un litro de solución:
- Pesar: 80,6 g de NaCl, 2,2 g de KCl, 11,5 g de Na2HPO4, 2,0 g de KH2HPO4
- En un vaso de precipitado colocar las sales pesadas, agregar suficiente agua (80%) y mezclar sobre la plancha agitadora con barra magnética hasta que se disuelvan las sales.

- Filtrar para eliminar las partículas no disueltas. Utilizar filtros con poros de 0,45 µm.
- Esterilizar en autoclave y distribuir asépticamente en campana de flujo laminar en frascos de vidrio con tapa.
A la solución 10X (concentrada) no se ajusta el pH. El ajuste se realiza una vez diluida a la concentración buffer PBS 1X, (dilución 1:10).
Buffer fosfato salino (PBS 1X)
El PBS 1X puede prepararse de forma directa, pesando las cantidades correspondientes de cada sal, o puede prepararse diluyendo la solución madre (1:10) con agua destilada estéril.
Para preparar directamente un litro de buffer fosfato salino PBS 1X:
- Pesar 8,06 g de NaCl, 0,22 g de KCl, 1,15 g de Na2HPO4, 0,20 g de KH2HPO4
- Proceder como se explicó en la solución concentrada. Posteriormente, se debe ajustar el pH.
- Para ello medir el pH y dependiendo del resultado, utilizar ácido (HCl) o base (NaOH) para bajar o subir el pH respectivamente según sea necesario, hasta que quede en 7,4.
- El ácido o la base se agregan gota a gota mientras se va monitoreando el valor del pH de la solución empleando un pH-metro.
- Filtrar, esterilizar en autoclave y distribuir asépticamente en tubos cónicos o frascos según sea necesario.
Para preparar el PBS 1X a partir de la solución madre 10X:
- Realizar una dilución 1:10. Por ejemplo, para preparar 1 litro de PBS 1X, medir 100 ml de la solución madre y agregar 700 ml de agua destilada estéril.
- Ajustar el pH y completar la cantidad de agua hasta llegar a 1.000 ml.
El buffer PBS preparado es incoloro y transparente. El PBS de uso diario se puede guardar a temperatura ambiente y el resto en nevera.
Soluciones para el ajuste de pH
HCl
Para 100 ml de HCL (ácido clorhídrico) al 1 molar.
- Medir 91 mL de agua destilada y colocarlo en un vaso precipitado de 250 ml de capacidad.
- Medir 8,62 mL de HCl concentrado y agregarlo lentamente en el vaso de precipitados que contiene el agua (nunca hacerlo al revés). Tomar las medidas de bioseguridad pertinentes al manipular ácidos fuertes (sustancia altamente corrosiva).
- Mezclar por 5 minutos utilizando preferiblemente una plancha agitadora con una barra magnética en el interior del vaso.
- Pasar a un balón de 100 ml y enrasar a 100 ml con H₂O destilada.
NaOH
Para 100 ml de NaOH (hidróxido de sodio) 10 molar.
- Medir 40 mL de agua destilada y colocar en un vaso de precipitados de 250 ml de capacidad.
- Medir 40 gr de NaOH y agregar al agua.
- Mezclar haciendo uso de una plancha agitadora con una barra magnética en el interior del vaso.
- Pasar a un balón aforado de 100 ml y enrasar con agua destilada. Cumplir con las normas de bioseguridad, debido a que esta reacción es exotérmica (libera energía en forma de calor).
Si se desea preparar otras cantidades de solución fosfato salino, se puede consultar la siguiente tabla:
Usos del buffer de fosfatos
- Principalmente, se usa en laboratorios de biología celular, inmunología, inmunohistoquímica, bacteriología, virología e investigación.
- Es ideal para hacer lavados celulares por centrifugados (glóbulos rojos), lavados de monocapas celulares, en técnicas de elipsometría espectroscópica, en la cuantificación de biopelículas bacterianas, en el mantenimiento de cultivos celulares para virus, como solución de lavado en la técnica de inmunofluorescencia indirecta y en técnicas para la caracterización de anticuerpos monoclonales.
- También sirve para transportar células o tejidos, como diluyente para el contaje de células, la preparación de enzimas celulares (tripsina), como diluyente del método de desecación de biomoléculas y para preparar otros reactivos.
- Por otra parte, algunos investigadores demostraron que el PBS es útil en laboratorios de ciencias forenses, específicamente en la recuperación de espermatozoides provenientes de frotis vaginales, o en la recuperación de células vaginales de frotis de pene. De esta manera se puede establecer si ha habido una relación sexual.
Limitaciones del buffer de fosfatos
- Algunos buffers PBS traen como preservante una sustancia llamada azida de sodio. Este compuesto puede generar sustancias explosivas si se pone en contacto con plomo o cobre. Por este motivo se debe tener especial cuidado al descartar este reactivo por el desagüe. Si se descarta por esta vía debe agregarse abundante agua para diluir al máximo.
- Al buffer fosfato no se le debe adicionar zinc, ya que hace precipitar algunas sales.
- Wangen y colaboradores en el 2018 determinaron que el uso de PBS no era adecuado para el lavado de células primarias de leucemia mieloide aguda (AML) extraídas de sangre periférica, debido a que se pierden muchas células por lisis, con una gran disminución del material proteico. Por tanto, determinaron que las células primarias de AML no deben lavarse con PBS después del almacenamiento en nitrógeno líquido.
Referencias
- Coll J. Técnicas de diagnóstico en virología. Ed. Díaz de Santos.
- Cultivo celular. Cambio de Medio. Recuperado de personal.us.es.
- Tampón fosfato salino. Recuperado de es.wikipedia.org.
- Tópicos en biofísica molecular. Recuperado de users.df.uba.ar.
- Rediar. Manual de Instrucciones. PBS+EDTA. Recuperado de felsan.com.ar.