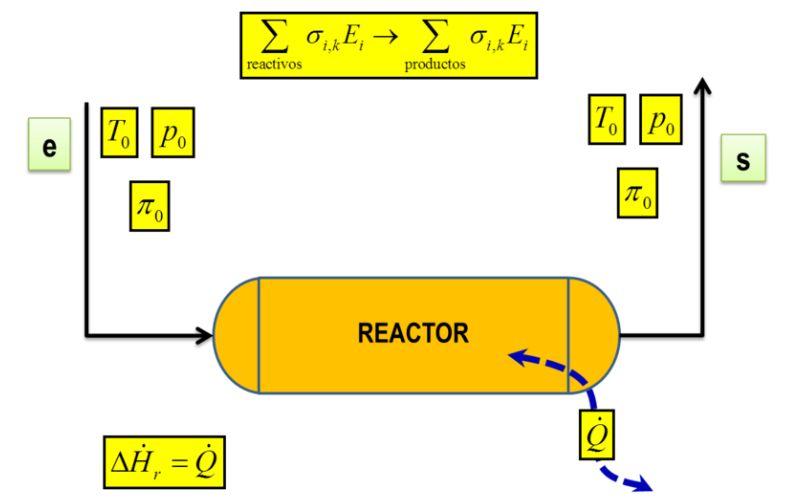
¿Qué es el calor de reacción?
El calor de reacción, o entalpía de reacción (ΔH), es la cantidad de energía por mol que se libera o se produce en una reacción química a una presión constante. Es una unidad termodinámica de medida útil para calcular la energía liberada o producida.
Dado que la entalpía se deriva de la presión, el volumen y la energía interna, las cuales todas son funciones de estado, la entalpía es también una función de estado.
ΔH, o el cambio de entalpía, surgió como una unidad de medida destinada a calcular el cambio de energía de un sistema cuando se hizo demasiado difícil encontrar el ΔU, o cambio en la energía interna de un sistema, midiendo simultáneamente la cantidad de calor y trabajo intercambiado.
Dada una presión constante, el cambio de entalpía es igual al calor, y se puede medir como ΔH = q.
La notación ΔHº o ΔHºr surge entonces para explicar la temperatura y la presión precisas del calor de reacción ΔH.
La entalpía estándar de reacción está simbolizada por ΔHº o ΔHºrxn y puede asumir tanto valores positivos como negativos. Las unidades para ΔHº son kiloJulios por mol, o kj / mol.
Concepto previo para entender el calor de reacción: diferencias entre ΔH y ΔHºr
– Δ = representa el cambio en la entalpía (entalpía de los productos menos la entalpía de los reactantes).
Un valor positivo indica que los productos tienen mayor entalpía, o que es una reacción endotérmica (se requiere calor).
Un valor negativo indica que los reactantes tienen mayor entalpía, o que es una reacción exotérmica (se produce calor).
– º = significa que la reacción es un cambio de entalpía estándar, y se produce a una presión / temperatura preestablecida.
– r = denota que este cambio es la entalpía de la reacción.
– El estado estándar: el estado estándar de un sólido o líquido es la sustancia pura a una presión de 1 bar, o lo que es lo mismo, 1 atmósfera (105 Pa) y una temperatura de 25 °C, o lo que es lo mismo, 298 K.
– El ΔHºr es el calor estándar de reacción o entalpía estándar de una reacción, y como ΔH también mide la entalpía de una reacción. Sin embargo, ΔHºrxn tiene lugar en condiciones “estándar”, lo que significa que la reacción tiene lugar a 25 °C y 1 atm.
El beneficio de una medición de ΔH bajo condiciones estándar radica en la capacidad de relacionar un valor de ΔHº con otro, ya que se producen en las mismas condiciones.
Calor de formación
El calor estándar de formación, ΔHfº, de un producto químico es la cantidad de calor absorbido o liberado de la formación de 1 mol de ese producto químico a 25 °C y 1 bar de sus elementos en sus estados estándar.
Un elemento está en su estado estándar si está en su forma más estable y su estado físico (sólido, líquido o gas) a 25 °C y 1 bar.
Por ejemplo, el calor estándar de formación para dióxido de carbono implica oxígeno y carbono como reactivos.
El oxígeno es más estable como moléculas de gas O2, mientras que el carbono es más estable como grafito sólido (el grafito es más estable que el diamante en condiciones estándar).
Para expresar la definición de otra manera, el calor estándar de formación es un tipo especial de calor estándar de reacción.
La reacción es la formación de 1 mol de un producto químico de sus elementos en sus estados estándar en condiciones estándar.
El calor estándar de la formación también se llama entalpía estándar de la formación (aunque realmente es un cambio en la entalpía).
Por definición, la formación de un elemento de sí mismo no produciría ningún cambio en la entalpía, por lo que el calor estándar de reacción para todos los elementos es cero.
Cálculo de la entalpía de reacción
1. Cálculo experimental
La entalpía se puede medir experimentalmente mediante el uso de un calorímetro. Un calorímetro es un instrumento donde se hace reaccionar una muestra al través de unos cables eléctricos que proveen la energía de activación. La muestra se encuentra en un recipiente rodeado de agua, la cual se agita constantemente.
Al medir con un calorímetro el cambio de temperatura que se produce al hacer reaccionar la muestra, y sabiendo el calor específico del agua y su masa, se calcula el calor que libera o absorbe la reacción mediante la ecuación q=Cesp x m x ΔT.
En esta ecuación, q es el calor, Cesp es el calor específico, en este caso del agua, que es igual a 1 caloría por gramo, m es la masa de agua y ΔT es el cambio de temperatura.
El calorímetro es un sistema aislado que tiene una presión constante, por lo que ΔHr=q
2. Cálculo teórico
El cambio de entalpía no depende de la vía particular de una reacción, sino solo del nivel de energía global de los productos y reactivos. La entalpía es una función del estado, y como tal, es aditiva.
Para calcular la entalpía estándar de una reacción, podemos sumar las entalpías estándar de formación de los reactivos y restarla de la suma de las entalpías estándar de formación de los productos. Dicho matemáticamente, esto nos da:
ΔHr° = Σ ΔHfº (productos) – Σ ΔHfº (reactantes).
Las entalpías de reacciones se calculan habitualmente a partir de entalpías de formación de reactivos en condiciones normales (presión de 1 bar y temperatura 25 °C).
Para explicar este principio de la termodinámica, calcularemos la entalpía de la reacción para la combustión del metano (CH4) según la fórmula:
CH4 (g) + 2O2 (g) → CO₂ (g) + 2H2O (g)
Para calcular la entalpía estándar de reacción, necesitamos buscar las entalpías estándar de formación para cada uno de los reactivos y productos implicados en la reacción.
Estos se encuentran normalmente en un apéndice o en varias tablas en línea. Para esta reacción, los datos que necesitamos son:
Hfº CH4 (g) = -75 kjoul/mol.
Hfº O2 (g) = 0 kjoul/mol.
Hfº CO₂ (g) = -394 kjoul/mol.
Hfº H₂O (g) = -284 kjoul/mol.
Nótese que debido a que se encuentra en su estado estándar, la entalpía estándar de formación para oxígeno gas es 0 kJ / mol.
A continuación, resumimos nuestras entalpías estándar de formación. Hay que tener en cuenta que debido a que las unidades están en kJ / mol, necesitamos multiplicar por los coeficientes estequiométricos en la ecuación de reacción balanceada.
Σ ΔHfº (productos) = ΔHfº CO₂ +2 ΔHfº H₂O
Σ ΔHfº (productos) = -1 (394 kjoul/mol) -2 (284 kjoul/mol) = -962 kjoul/mol
Σ ΔHfº (reactantes) = ΔHfº CH4 + ΔHfº O2
Σ ΔHfº (reactantes) = -75 kjoul/mol + 2 (0 kjoul/mol)= -75 kjoul/mol
Ahora, podemos encontrar la entalpía estándar de la reacción:
ΔHr° = Σ ΔHfº (productos) – Σ ΔHfº (reactantes) = (- 962) – (- 75) =
ΔHr° = – 887kJ / mol.
Referencias
- Enthalpy of Reaction Definition. Recuperado de thoughtco.com.
- (S.F.). Standard Enthalpy of Reaction. Recuperado de boundless.com.