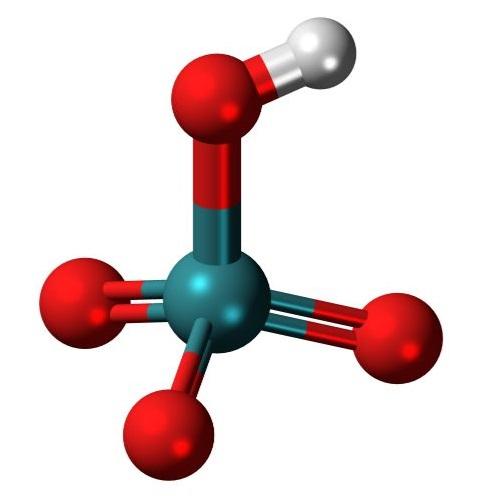
¿Qué es un oxácido?
Un oxácido, u oxoácido, es un ácido que contiene oxígeno. Está compuesto de hidrógeno, oxígeno y un elemento no metálico que constituye el llamado átomo central. Dependiendo del número de átomos de oxígeno, y por consiguiente, los estados de oxidación del elemento no metálico, pueden formarse varios oxácidos.
Los oxácidos presentan una gran cantidad de usos, que resultan difíciles de describir en forma general. Su aplicación dependerá enormemente del átomo central y del número de oxígenos.
Pueden servir desde compuestos para síntesis de materiales, fertilizantes y explosivos, hasta para fines analíticos o producción de bebidas gaseosas, como ocurre con el ácido carbónico y el ácido fosfórico, H3PO4, formando parte de la composición de estas bebidas.
Características y propiedades de un oxácido
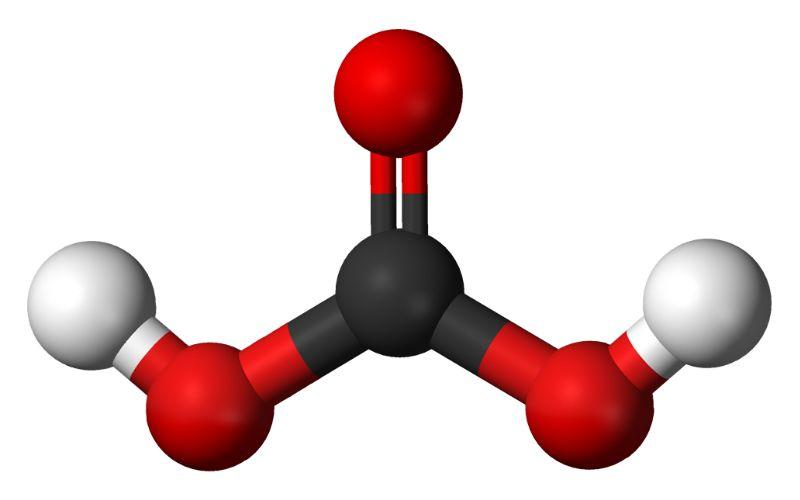
- Grupos hidroxilos: una de las principales características de un oxácido no es solo que posee oxígeno, sino que además este se halla como un grupo OH. Por otro lado, algunos oxácidos poseen lo que se denomina un grupo oxo, E=O. En el caso del ácido fosforoso, tiene un grupo oxo, P=O. Carecen de átomos de H, por lo que “no son responsables” de la acidez.
- Átomo central: el átomo central (E) puede o no ser un elemento electronegativo, dependiendo de su ubicación en el bloque p de la tabla periódica. Por otro lado, el oxígeno, elemento ligeramente más electronegativo que el nitrógeno, atrae los electrones del enlace OH, permitiendo así la liberación del ion H+. E está, por tanto, enlazado a grupos OH. Al liberarse un ion H+ se produce la ionización del ácido, es decir, adquiere una carga eléctrica, que en su caso es negativa. Un oxácido podrá liberar tantos iones H+ como grupos OH tenga en su estructura, y mientras más haya, mayor será la carga negativa.
- Fuerza ácida: la fuerza de casi todos los oxácidos que tienen el mismo átomo central (no metal), aumenta con el incremento del estado de oxidación del elemento central, el cual a su vez se relaciona directamente con el incremento del número de átomos de oxígeno.
Por ejemplo, se muestran tres series de oxácidos cuyas fuerzas de acidez están ordenadas de menor a mayor:
H2SO3 < H2SO4
HNO2 < HNO3
HClO < HClO2 < HClO3 < HClO4
En la mayoría de los oxácidos que tienen elementos distintos con el mismo estado de oxidación, pero pertenecientes al mismo grupo de la tabla periódica, la fuerza de acidez aumenta en forma directa con la electronegatividad del átomo central:
H2SeO3 < H2SO3
H3PO4 < HNO3
HBrO4 < HClO4
Formación de los oxácidos
Como se mencionó al principio, los oxácidos se generan cuando ciertas sustancias, llamadas óxidos ácidos, reaccionan con el agua. Se explicará esto utilizando el mismo ejemplo del ácido carbónico.
CO₂ + H₂O <=> H2CO3
Óxido ácido + agua => oxácido
Lo que sucede es que la molécula de H₂O se une covalentemente con la de CO₂. Si se elimina el agua mediante calor, se desplaza el equilibrio a la regeneración del CO₂, es decir, una bebida gaseosa caliente perderá más pronto su sensación efervescente que una fría.
Por otro lado, los óxidos ácidos se forman cuando reacciona un elemento no metálico con el agua, aunque, más precisamente, cuando el elemento reaccionante forma un óxido con carácter covalente, cuya disolución en agua genera iones H+.
Ya se ha dicho que los iones H+ son producto de la ionización del oxácido resultante.
Ejemplos de formación
El óxido clórico, Cl2O5, reacciona con el agua para dar el ácido clórico:
Cl2O5 + H₂O => HClO3
El óxido sulfúrico, SO3, reacciona con el agua para formar el ácido sulfúrico:
SO3 + H₂O => H2SO4
Y el óxido peryódico, I2O7, reacciona con el agua para formar el ácido peryódico:
I2O7 + H₂O => HIO4
Además de estos mecanismos clásicos para la formación de oxácidos, existen otras reacciones con el mismo fin.
Por ejemplo, el tricloruro de fósforo, PCl3, reacciona con el agua para producir el ácido fosforoso, un oxácido, y el ácido clorhídrico, un ácido halohídrico.
PCl3 + 3H2O => H3PO3 + HCl
Y el pentacloruro de fósforo, PCl5, reacciona con el agua para dar el ácido fosfórico y el ácido clorhídrico.
PCl5 + 4 H₂O => H3PO4 + HCl
Oxácidos metálicos
Algunos metales de transición forman óxidos ácidos, es decir, se disuelven en el agua para dar oxácidos.
El óxido de manganeso (VII) (anhidro permangánico) Mn2O7 y el óxido de cromo (VI) son los ejemplos más comunes.
Mn2O7 + H₂O => HMnO4 (ácido permangánico)
CrO3 + H₂O => H2CrO4 (ácido crómico)
Nomenclatura
Cálculo de la valencia
Para nombrar correctamente un oxácido debe empezarse con determinar la valencia o número de oxidación del átomo central E. Partiendo de la fórmula genérica HEO, se considera lo siguiente:
- El O tiene valencia -2.
- La valencia de los H es +1.
Con esto en mente, el oxácido HEO es neutro, por lo que la suma de las cargas de las valencias debe ser igual a cero. Así, se tiene la siguiente suma algebraica:
-2 + 1 + E = 0
E= 1
Por lo tanto, la valencia de E es +1.
Luego debe recurrirse a las valencias posibles que puede tener E. Si entre sus valencias están los valores +1, +3 y +4, E entonces “trabaja” con su menor valencia.
Nombrar al ácido
Para nombrar HEO se empieza llamándolo ácido, seguido del nombre de E con los sufijos -ico, si trabaja con la mayor valencia, u -oso, si trabaja con la menor. Cuando hay tres o más, se recurre a los prefijos hipo- y per- para referirse a la menor y mayor de las valencias.
Así, HEO se llamaría:
Ácido hipo(nombre de E)oso
Ya que +1 es la menor de sus tres valencias. Y si se tratara de HEO2, entonces E tendría valencia +3 y se llamaría:
Ácido (nombre de E)oso
Y de igual modo para HEO3, con E trabajando con la valencia +5:
Ácido (nombre de E)ico
Ejemplos
- Ácido crómico (H2Cr2O4). Es un ácido fuerte, inestable a altas temperaturas.
- Ácido dicrómico (H2Cr2O7). Su presencia se nota en las mezclas de ácido crómico que se usan para limpiar el vidrio.
- Ácido hipocloroso (HClO). Repara con rapidez tejidos de la piel.
- Ácido bromoso (HBrO2). Es un compuesto intermedio, inestable. Compuesto de bromo.
- Ácido ortofosfórico (H3PO4). Ácido irritante para la piel no combustible.
- Ácido permangánico (HMnO4). Ácido muy fuerte.
- Ácido peryódico (HIO4). En química orgánica se utiliza para analizar las estructuras de otras moléculas.
- Ácido brómico (HBrO3). Oxácido del bromo. Sus sales son poderosamente oxidantes.
- Ácido hipobromoso (HBrO). Se emplea en disolución acuosa diluida y se obtiene por reacción entre el agua y el Br2.
- Ácido metafosfórico (HPO3). Sólido muy corrosivo, incoloro e inodoro a temperatura ambiente.
- Ácido yódico (HIO3). Reactivo empleado para detectar la morfina en un producto.
- Ácido sulfuroso (H2SO3). Causante de la lluvia ácida.
- Ácido sulfúrico (H2SO4). Habitual para el procesado de metales y en los fertilizantes, es uno de los compuestos químicos más usados.
- Ácido nítrico (HNO3). Reactivo de laboratorio, muy peligroso porque puede quemar la piel.
- Ácido clórico (HClO3). Al descomponerse produce una gran cantidad de productos. Es estable en frío hasta una concentración del 30%.
- Ácido arsenioso (H3AsO3). Contiene arsénico y es muy tóxico y cancerígeno. Se usa en herbicidas y pesticidas.
- Ácido ortosilícico (H4SiO4). Ácido débil empleado como soporte o agente desecante.
- Ácido carbónico (H2CO3). Se usa para fabricar bebidas gaseosas.
- Ácido nitroso (HNO2). En disolución está notablemente disociado.
- Ácido metabórico (HBO2). Sólido blanco cristalino ligeramente soluble en agua.
Referencias
- Common Oxoacid Compounds. Recuperado de thoughtco.com.