
¿Qué es el óxido de plata?
El óxido de plata es un compuesto inorgánico cuya fórmula química es Ag2O. Es un polvo fino negro o café oscuro, que se utiliza para preparar otros compuestos de plata.
La fuerza que une sus átomos es de naturaleza enteramente iónica, por lo tanto, consta de un sólido iónico donde existe una proporción de dos cationes Ag+ interaccionando electrostáticamente con un anión O2-.
Las propiedades del óxido de plata son tales que no carcomen, a primera vista, la superficie metálica original. Se forma a temperatura ambiente por simple contacto con el oxígeno del aire. Aún más interesante, puede descomponerse a elevadas temperaturas (por encima de 200 °C).
El óxido de plata tiene además otras propiedades y, más allá de su simple fórmula Ag2O, abarca organizaciones estructurales complejas y una rica variedad de sólidos. Sin embargo, el Ag2O es quizás, junto al Ag2O3, el más representativo de los óxidos de la plata.
Estructura del óxido de plata
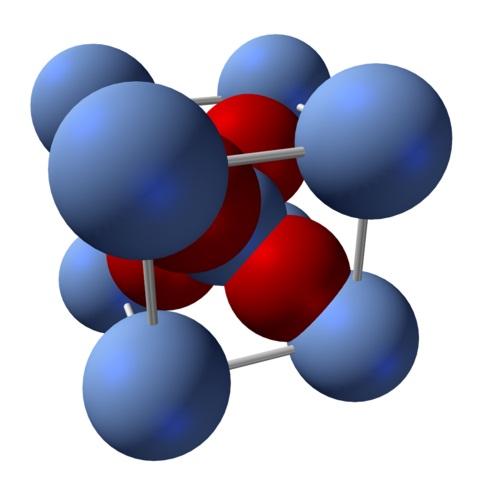
El óxido de plata es un sólido iónico. Por esta razón no puede haber enlaces covalentes Ag-O ni Ag=O en su estructura, pues de haberlos, las propiedades de este óxido cambiarían drásticamente. Se trata de iones Ag+ y O2- en una proporción 2:1, experimentando una atracción electrostática.
La estructura del óxido de plata viene determinada en consecuencia por el modo en que las fuerzas iónicas disponen en el espacio los iones Ag+ y O2-.
En la imagen superior, por ejemplo, se tiene una celda unitaria para un sistema cristalino cúbico: los cationes Ag+ son las esferas azul plateadas, y los O2- las esferas rojizas.
Si se cuenta el número de esferas, se hallará que hay, a simple vista, nueve esferas azules plateados y cuatro rojas. No obstante, solo se toma en consideración los fragmentos de las esferas contenidos dentro del cubo. De contar estos, siendo fracciones de las esferas totales, debe cumplirse la proporción 2:1 para el Ag2O.
Repitiendo la unidad estructural del tetraedro AgO4 rodeado de otros cuatro Ag+, se construye todo el sólido de color negro (obviando los huecos o irregularidades que pueden tener estos arreglos cristalinos).
Cambios con el número de valencia
Centrándose ahora no en el tetraedro AgO4 sino en la línea AgOAg (observar los vértices del cubo superior), se tendrá que el sólido de óxido de plata consta, desde otra perspectiva, de múltiples capas de iones dispuestos linealmente (aunque inclinados). Todo esto como resultado de la geometría “molecular” alrededor del Ag+.
La plata trabaja predominantemente con valencia +1, ya que al perder un electrón su configuración electrónica resultante es [Kr]4d10, la cual es muy estable. Otras valencias, como Ag2+ y Ag3+ son menos estables porque pierden electrones de orbitales d casi llenos por completo.
El ion Ag3+, no obstante, es relativamente menos inestable comparado a Ag2+. De hecho, puede coexistir en compañía del Ag+ enriqueciendo químicamente la estructura.
Su configuración electrónica es [Kr]4d8, con electrones desapareados de tal forma que le otorga cierta estabilidad.
A diferencia de las geometrías lineales en torno a los iones Ag+, se ha encontrado que la de los iones Ag3+ es plano cuadrado. Por lo tanto, un óxido de plata con iones Ag3+ consistiría de capas compuestas por cuadrados de AgO4 (no tetraedros) unidos electrostáticamente por líneas AgOAg. Tal es el caso del Ag4O4 o Ag2O∙Ag2O3 con estructura monoclínica.
Propiedades físicas y químicas
Algunas de sus propiedades físicas y químicas reportadas por los momentos son las siguientes:
- Peso molecular: 231,735 g/mol.
- Apariencia: sólido negro marrón en forma de polvo. Es inodoro, y mezclado con agua le confiere un sabor metálico.
- Densidad: 7,14 g/mL.
- Punto de fusión: 277-300 °C. Ciertamente, se funde en plata sólida, es decir, se descompone probablemente antes de formar el óxido líquido.
- Kps: 1,52∙10-8 en agua a 20 °C. Es un compuesto apenas soluble en agua.
- Solubilidad: si se observa detenidamente la imagen de su estructura, se encontrará que las esferas de Ag2+ y O2- no discrepan casi en tamaño. Esto trae como consecuencia que solo moléculas pequeñas puedan traspasar el interior de red cristalina, haciéndolo insoluble en casi todos los solventes, a excepción de aquellos donde reacciona, como las bases y los ácidos.
- Carácter covalente: aunque se ha dicho en reiteradas oportunidades que el óxido de plata es un compuesto iónico, ciertas propiedades, como su bajo punto de fusión, contradicen esta afirmación.
- Descomposición; al principio se hizo mención de que su formación es termodinámicamente reversible, por lo que absorbe calor para regresar a su estado metálico. Todo esto puede expresarse mediante dos ecuaciones químicas para tales reacciones: 4Ag(s) + O2(g) => 2Ag2O(s) + Q, y 2Ag2O(s) + Q => 4Ag(s) + O2(g). Donde Q representa al calor en la ecuación. Esto explica por qué el fuego quemando la superficie de la copa de plata oxidada le regresa su brillo plateado. Por lo tanto, es difícil suponer que haya Ag2O(l) porque se descompondría al instante por el calor, a menos que se eleve demasiado la presión para obtener dicho líquido negro marrón.
Nomenclatura
Cuando se introdujo la posibilidad de iones Ag2+ y Ag3+ además del común y predominante Ag+, el término óxido de plata comienza a parecer insuficiente para referirse al Ag2O.
Esto se debe a que el ion Ag+ es más abundante que los otros, por lo que se toma el Ag2O como único óxido, lo cual no es correcto del todo.
Si se considera el Ag2+ como prácticamente inexistente dada su inestabilidad, se tendrá entonces solamente los iones con valencias +1 y +3; es decir, Ag(I) y Ag(III).
Valencias I y III
Al ser el Ag(I) el de menor valencia, se le nombra adicionando el sufijo -oso a su nombre argentum. Así, el Ag2O es: óxido argentoso o, de acuerdo a la nomenclatura sistemática, monóxido de diplata.
Si se ignora completamente al Ag(III), entonces su nomenclatura tradicional debe ser: óxido argéntico en lugar de óxido argentoso.
Por otro lado, el Ag(III), al ser la mayor valencia, se le adiciona el sufijo -ico a su nombre. Así, el Ag2O3 es: óxido argéntico (2 iones Ag3+ con tres O2-). Asimismo, su nombre de acuerdo a la nomenclatura sistemática sería: trióxido de diplata.
Si se observa la estructura del Ag2O3, se puede presumir que es producto de una oxidación por ozono, O3, en lugar de oxígeno. Por lo tanto, su carácter covalente debe ser mayor al tratarse de compuesto covalente con enlaces Ag-O-O-O-Ag o Ag-O3-Ag.
Nomenclatura sistemática para óxidos complejos de plata
El AgO, escrito también como Ag4O4 o Ag2O∙Ag2O3, es un óxido de plata (I, III), ya que posee ambas valencias +1 y +3. Su nombre de acuerdo a la nomenclatura sistemática sería: tetraóxido de tetraplata.
Esta nomenclatura es de gran ayuda cuando se trata de otros óxidos de plata estequiométricamente más complejos. Por ejemplo, supóngase los dos sólidos 2Ag2O∙Ag2O3 y Ag2O∙3Ag2O3.
Escribiendo el primero de manera más apropiada sería: Ag6O5 (contando y sumando los átomos de Ag y O). Su nombre sería entonces pentóxido de hexaplata. Nótese que este óxido tiene una composición de plata menos rica que el Ag2O (6:5 < 2:1).
Mientras que escribiendo de otra manera el segundo sólido, sería: Ag8O10. Su nombre sería decaóxido de octaplata (con una proporción 8:10 o 4:5). Este hipotético óxido de plata estaría “muy oxidado”.
Usos
Los estudios en busca de nuevos y sofisticados usos para el óxido de plata se siguen realizando actualmente. Algunos de sus usos se listan a continuación:
- Se disuelve en amoníaco, nitrato de amonio y agua para formar el reactivo de Tollens. Este reactivo es una herramienta útil en los análisis cualitativos dentro de los laboratorios de química orgánica. Permite determinar la presencia de aldehídos en una muestra, siendo como respuesta positiva la formación de un “espejo de plata” en el tubo de ensayo.
- Junto con el zinc metálico conforma las baterías primarias de zinc-óxido de plata. Este es quizás uno de sus usos más comunes y hogareños.
- Sirve como purificador de gases, absorbiendo por ejemplo CO₂. Al calentársele, libera los gases atrapados y puede reutilizarse varias veces.
- Debido a las propiedades antimicrobianas de la plata, su óxido tiene utilidad en estudios de bioanálisis y purificación de los suelos.
- Es un agente oxidante suave capaz de oxidar los aldehídos a ácidos carboxílicos. Asimismo, se utiliza en la reacción de Hofmann (de aminas terciarias) y participa en otras reacciones orgánicas, ya sea como reactivo o catalizador.
Referencias
- Bergstresser, M. Silver Oxide: Formula, Decomposition & Formation. Recuperado de study.com.
- Sullivan, R. Decomposition of silver oxide. Recuperado de chemdemos.uoregon.edu.
- Flint, D. Uses of Silver Oxide Batteries. Recuperado de sciencing.com.