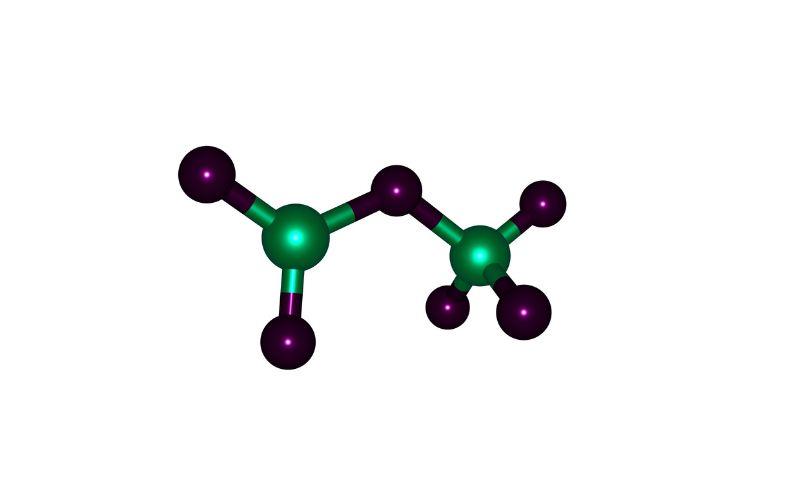
¿Qué es el óxido perclórico?
El óxido perclórico, también llamado óxido de cloro (VII), anhídrido perclórico o heptaóxido de dicloro, es un compuesto químico inorgánico de fórmula Cl2O7, formado por átomos de cloro y oxígeno.
Es uno de los óxidos de cloro más estables y reacciona con agua para producir ácido perclórico:
Cl2O7 + H₂O D 2HClO4
El compuesto se obtiene mediante la cuidadosa deshidratación del ácido perclórico con pentóxido de fósforo a -10 °C.
2HClO4 + P2O5 ” Cl2O7 + 2HPO3
El compuesto se destila para separarlo del ácido metafosfórico con mucha precaución, dada su naturaleza explosiva. También puede formarse por iluminación en mezclas de cloro y ozono.
Propiedades físicas y químicas del óxido perclórico
– El óxido de cloro (VII) es un líquido incoloro, volátil y aceitoso.
– Su peso molecular es de 182,9 g/mol, su densidad es de 1.900 kg/m³ y los puntos de fusión y de ebullición son -91,57 °C y 82 °C, respectivamente.
– Es espontáneamente explosivo al impacto o en contacto con la flama, y especialmente en presencia de sus productos de descomposición.
– El heptaóxido de cloro se disuelve en tetracloruro de carbono a temperatura ambiente y reacciona con agua para formar ácido perclórico. Estalla al contacto con el yodo.
– En condiciones normales es más estable, aunque con menos poder oxidante que los otros óxidos de cloro. Por ejemplo, no ataca el azufre, fósforo o papel cuando está frío.
– El heptaóxido de dicloro es un óxido fuertemente ácido, y en solución forma un equilibrio con el ácido perclórico. Forma percloratos en presencia de hidróxidos de metales alcalinos.
– Su descomposición térmica se produce por la disociación monomolecular del trióxido de cloro y radical.
Riesgos
El óxido perclórico es un compuesto inestable. Se descompone lentamente al almacenarse, con la producción de productos de descomposición coloreados que son óxidos de cloro más bajos.
Es espontáneamente explosivo, especialmente en presencia de sus productos de descomposición, incompatible con agentes reductores, ácidos y bases fuertes.
Aunque es el óxido de cloro más estable, Cl2O7, es un oxidante fuerte, así como un explosivo que puede ser apagado con llama o choque mecánico, o por contacto con el yodo.
Sin embargo, es menos oxidante que los otros óxidos de cloro, y no ataca el azufre, el fósforo o el papel cuando está frío. Tiene los mismos efectos sobre el cuerpo humano que el cloro elemental, y requiere las mismas precauciones.
La ingestión causa quemaduras severas en la boca, el esófago y el estómago. El vapor es muy tóxico por inhalación.
En caso de contacto con los ojos se debe verificar si se está usando lentes de contacto y removerlos inmediatamente. Se debe enjuagar los ojos con agua corriente durante al menos 15 minutos, manteniendo los párpados abiertos. Se puede utilizar agua fría, sin administrar ungüento para los ojos.
Si el producto químico entra en contacto con la ropa, retírela lo más rápido posible, protegiendo sus propias manos y cuerpo. Coloque a la víctima bajo una ducha de seguridad.
Si el producto químico se acumula en la piel expuesta de la víctima, como las manos, se lava suave y cuidadosamente la piel contaminada con agua corriente y jabón no abrasivo.
Se puede usar agua fría. Si la irritación persiste, busque atención médica. Lave la ropa contaminada antes de volver a utilizarla.
En caso de inhalación, se debe dejar reposar a la víctima en un área bien ventilada. Si la inhalación es grave, se debe evacuar a la víctima a una zona segura tan pronto como sea posible.
Afloje la ropa apretada, como cuello de camisa, cinturones o corbata. Si a la víctima le resulta difícil respirar, se debe administrar oxígeno.
Si la víctima no está respirando, se realiza una resucitación boca a boca. Siempre tomando en cuenta que puede ser peligroso para la persona que proporciona ayuda dar reanimación boca a boca cuando el material inhalado es tóxico, infeccioso o corrosivo.
En todos los casos se debe buscar atención médica inmediata.
Usos
– El óxido perclórico no tiene aplicaciones prácticas. Podría usarse como agente oxidante o para la producción de ácido perclórico, pero su naturaleza explosiva hace difícil su manejo.
– El heptaóxido de dicloro se puede emplear como reactivo para la producción de percloratos o para el estudio con diferentes reacciones.
– En el trabajo de Kurt Baum se han estudiado las reacciones del óxido perclórico con olefinas, alcoholes, ioduros de alquilo y perclorato de acilo con éster, obteniéndose halogenaciones y oxidaciones.
– En el caso de los alcoles, produce alquil-percloratos reaccionando con alcoholes simples como el etilenglicol, 1, 4-butadienol, 2, 2, 2-trifluoroetanol, 2, 2-dinitropropanol. Reacciona con el 2-propanol para dar isopropil perclorato. 2-hexanol y 3-hexanol dan percloratos sin arreglos y sus respectivas cetonas.
– El propeno reacciona con el heptaóxido de dicloro en tetracloruro de carbono para dar isopropil perclorato (32%) y 1cloro, 2-propilperclorato (17%). El compuesto reacciona con el cis-buteno para dar 3-clorobutil perclorato (30%) y 3-ceto, 2-butil perclorato (7%).
– El heptaóxido de dicloro reacciona con aminas primarias y secundarias en solución de tetracloruro de carbono para dar N-percloratos:
2 RNH2 + Cl2O7 → 2 RNHClO3 + H₂O
2 R2NH + Cl2O7 → 2 R2NClO3 + H₂O
– También reacciona con alquenos para dar percloratos de alquilo. Por ejemplo, reacciona con propeno en solución de tetracloruro de carbono para producir perclorato de isopropilo y perclorato de 1-cloro-2-propilo.
Referencias
- Egon Wiberg, N. W. (2001). Inorganic Chemistry. Academic Press: Londres.
- (2009). Dichlorine heptaoxide. Retrieved from ChEBI: ebi.ac.uk.