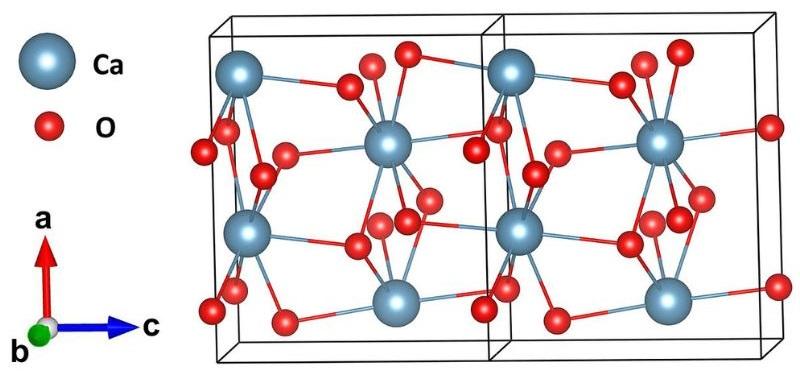
¿Qué es el peróxido de calcio?
El peróxido de calcio, también conocido como dióxido de calcio, es un compuesto químico de fórmula CaO2. Se produce con la interacción de la disolución de una sal o hidróxido de calcio y peróxido de sodio con la posterior cristalización.
El peróxido de calcio es producido por precipitación del compuesto octahidratado a partir de una solución acuosa, seguido de deshidratación a temperaturas superiores a 100 °C.
El peróxido de calcio se descompone para liberar oxígeno cuando está en contacto con el material hidratado. CaO2 es uno de los peróxidos inorgánicos más estables a la temperatura y se descompone lentamente en aire húmedo.
Una suspensión acuosa de 1: 100 tiene un pH de aproximadamente 12. Excepto por su capacidad estable de liberación de oxígeno, CaO2 tiene funciones similares de otros peróxidos: blanqueamiento, desinfección y desodorización. Además, es destacable señalar que CaO2 es respetuoso con el medio ambiente debido a sus propiedades.
Propiedades físicas y químicas del peróxido de calcio
- Apariencia: es un polvo blanco o amarillento, sin aroma o sabor característico.
- Peso molecular: 72,0768 g/mol.
- Densidad: 2,91 g/ml.
- Punto de fusión: 200 °C y se descompone por encima de los 355 °C.
- Solubilidad: ligeramente soluble en agua formando peróxido de hidrógeno.
- pKa: 12,5.
- Reacciones: tiene riesgo de explosión si se mezcla con materia orgánica finamente dividida. El compuesto no es combustible en sí, sino que acelera la combustión de material combustible. Esto se debe a que las mezclas de material combustible y el peróxido pueden inflamarse por fricción o contacto con la humedad.
Reactividad y riesgos del peróxido de calcio
A pesar de que es un compuesto relativamente estable en comparación con otros peróxidos, se clasifica como un compuesto explosivo y un fuerte agente oxidante.
El contacto con el peróxido de calcio puede irritar severamente y quemar la piel y los ojos. La exposición puede irritar los ojos, la nariz y la garganta.
La exposición prolongada puede dañar la piel. Los niveles más altos de peróxido de calcio pueden irritar los pulmones y causar tos o falta de aire.
Mayores exposiciones pueden causar una acumulación de líquido en los pulmones (edema pulmonar), lo que puede provocar la muerte.
En caso de contacto con los ojos, se debe revisar y quitar los lentes de contacto. Posteriormente, lavar los ojos con abundante agua fría durante al menos 15 minutos.
En caso de contacto con la piel, se debe enjuagar inmediatamente el área afectada con abundante agua durante al menos 15 minutos mientras se quita la ropa contaminada y los zapatos. Cubrir la piel irritada con un emoliente. Lavar la ropa y zapatos antes de volver a usarlos. Si el contacto es grave, lavar con jabón desinfectante y cubrir la piel contaminada con una crema antibacteriana.
En caso de inhalación, se debe trasladar a la víctima a un lugar fresco. Si no respira, administrar respiración artificial.
Si el compuesto se ingiere, hay que inducir el vómito a menos que lo indique el personal médico. Se aconseja beber agua en grandes cantidades para conseguir la dilución del compuesto. Se debe aflojar la ropa apretada, como cuello de camisa, cinturón o corbata.
En todos los casos se debe obtener atención médica inmediatamente.
Usos del peróxido de calcio
- Uso en la remediación del suelo. Su aplicación agrícola es la más frecuente. El hecho de que el peróxido de calcio libere oxígeno cuando está en contacto con el agua significa que puede emplearse como una forma de rejuvenecer el suelo agotado. Normalmente, después de la agricultura intensiva o cuando el suelo está inundado, los nutrientes y el oxígeno del suelo se pierden, por lo que es estéril. En tal escenario, se deben utilizar varios fertilizantes artificiales para agregar minerales y nutrientes, además de otras intervenciones para hacerla viable otra vez. El peróxido de calcio es fundamental para este proceso, ya que se utiliza para aumentar el contenido de oxígeno del suelo.
- Otros usos. El hecho de que el peróxido de calcio pueda liberar peróxido de hidrógeno cuando se combina con ácidos significa que puede emplearse como un agente blanqueador. Es ampliamente utilizado de esta manera en muchas industrias del papel. La producción de peróxido de hidrógeno por este compuesto también lo hace útil en la desodorización y el blanqueo de productos capilares y textiles.
- Salud. Puede usarse como antiséptico.
- Alimentación. El peróxido de calcio se utiliza en la cocción como una ayuda de procesamiento en la mezcla de masa de pan. El compuesto se descompone en oxígeno una vez que entra en contacto con el agua. Esto oxida y refuerza los enlaces cruzados disulfuro y no disulfuro en gluten.
- Restauración ambiental. El hecho de que el peróxido de calcio pueda actuar como fuente de oxígeno significa que es útil en muchos escenarios ecológicos. Por ejemplo, hay muchos cuerpos de agua, como lagos y estanques, que se han vuelto no viables debido a la contaminación y otros factores relacionados. En tal escenario, el peróxido de calcio se puede utilizar para rejuvenecer estos cuerpos de agua. El oxígeno liberado por la reacción entre el agua y el compuesto restaura el contenido de oxígeno del agua.
- Uso industrial. El papel del peróxido de calcio en la producción de plásticos es crítico para los procesos de catálisis y reticulación de los diferentes compuestos que se emplean en la polimerización de plásticos para hacerlos duros. El peróxido de calcio también se usa como iniciador de estos procesos.
Referencias
- CALCIUM PEROXIDE. Recuperado de cameochemicals.noaa.gov.
- Calcium Peroxide. Recuperado de bakerpedia.com.
- Calcium Peroxide. Recuperado de chinacjchem.com.
- Calcium peroxide. Recuperado de ebi.ac.uk.
- Calcium Peroxide—CALGRO™. Recuperado de kingsfieldinc.