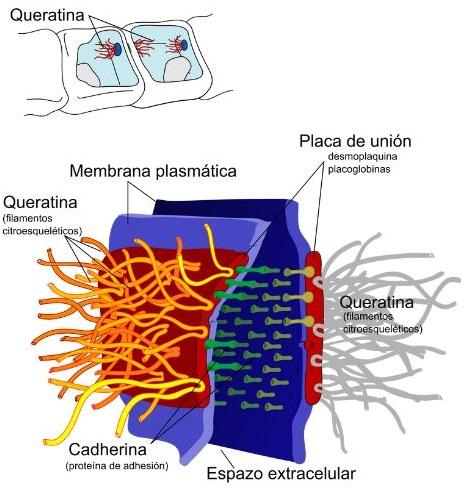
¿Qué es la queratina?
La queratina es una proteína fibrosa insoluble que forma parte estructural de las células que constituyen las capas más externas de la epidermis de los vertebrados y de órganos y estructuras como plumas, pelos, uñas, cuernos, picos y pezuñas. Tiene formas muy variadas y es poco reactiva, químicamente hablando.
Su estructura fue descrita por primera vez por los científicos Linus Pauling y Robert Corey en 1951, mientras analizaban la estructura del pelo animal.
Después del colágeno, es una de las proteínas más importantes de los animales y representa la mayor parte del peso seco del pelo, lana, uñas, garras y pezuñas, plumas, cuernos y de parte sustancial de la capa externa de la piel.
Los elementos, o partes “queratinizadas”, de los animales pueden tener morfologías muy diferentes que dependen, en gran medida, de la función que ejercen en cada organismo en particular.
La queratina es una proteína con características que le otorgan gran eficiencia mecánica en cuanto a tensión y a compresión. Es producida por un tipo especial de células denominadas queratinocitos, que usualmente mueren después de producirla.
En los humanos hay más de 30 genes codificantes para estas proteínas y pertenecen a una familia que evolucionó por varias rondas de duplicación genética.
Tipos de queratina y su estructura
Existen, esencialmente, dos tipos de queratinas: las α y las β. Se distinguen por poseer una estructura básica compuesta primordialmente por cadenas polipeptídicas que pueden enrollarse como hélices alfa (α-queratinas) o unirse paralelamente como las láminas β-plegadas (β-queratinas).
α-queratinas
Es el más estudiado y se sabe que los mamíferos tienen al menos 30 variantes distintas de este tipo de queratina. En estos animales, las α-queratinas forman parte de uñas, pelo, cuernos, cascos, púas y epidermis.
Al igual que el colágeno, estas proteínas contienen en su estructura una abundante proporción de aminoácidos pequeños, como glicina y alanina, que hacen posible el establecimiento de las hélices alfa. La estructura molecular de una α-queratina se compone de tres regiones diferentes: (1) las fibrillas cristalinas o las hélices, (2) los dominios terminales de los filamentos y (3) la matriz.
Las hélices son dos y forman un dímero que se asemeja a una espiral enroscada que se mantiene unida gracias a los enlaces o puentes disulfuro (S-S). Cada una de las hélices tiene aproximadamente 3.6 residuos aminoacídicos en cada giro que da y se compone de más o menos 310 aminoácidos.
Estas espirales enroscadas se pueden asociar luego para formar una estructura conocida como protofilamento o protofibrilla, que tiene la capacidad de ensamblarse con otros de su mismo tipo.
Los protofilamentos poseen extremos N- y C-terminales no helicoidales ricos en residuos de cisteína, y están unidos a la región central o matriz. Estas moléculas se polimerizan para formar los filamentos intermedios, con un diámetro cercano a los 7 nm.
Se distinguen dos tipos de filamentos intermedios compuestos por queratina: los filamentos intermedios acídicos (tipo I) y los básicos (tipo II). Están embebidos en una matriz proteica y la forma en la que se ordenan influye directamente en las propiedades mecánicas de la estructura que conforman.
En los filamentos tipo I, las hélices se conectan entre sí por medio de tres “conectores helicoidales”, conocidos como L1, L12 y L2, y que se piensa aportan flexibilidad al dominio helicoidal. En los filamentos tipo II existen, además, dos subdominios que se encuentran entre los dominios helicoidales.
Ejemplo de una estructura con α-queratinas: el pelo
Si se analiza la estructura de un pelo típico, tiene un diámetro aproximado de 20 micras y está compuesto de células muertas que contienen macrofibrillas empaquetadas orientadas de forma paralela (una al lado de la otra).

Las macrofibrillas se componen de microfibrillas, de menor diámetro, y están unidas unas con otras a través de una sustancia proteica amorfa con altos contenidos de azufre.
Estas microfibrillas son grupos de protofibrillas más pequeñas con un patrón de organización 9+2, que quiere decir que nueve protofibrillas rodean dos protofibrillas centrales. Todas estas estructuras están compuestas esencialmente por α-queratina.
Queratinas blandas y queratinas duras
Dependiendo del contenido de azufre, las α-queratinas pueden clasificarse como queratinas blandas o duras. Ello tiene que ver con la fuerza de resistencia mecánica que imponen los enlaces disulfuro en la estructura proteica.
En el grupo de las queratinas duras, se incluyen las que forman parte del pelo, los cuernos y las uñas, y las queratinas blandas están representadas por los filamentos que están en la piel y los callos.
Los enlaces disulfuro pueden eliminarse mediante la aplicación de algún agente reductor, por lo que las estructuras compuestas por queratina no son fácilmente digeribles por los animales, a menos que estos posean intestinos ricos en mercaptanos, como el caso de algunos insectos.
β-queratinas
Las β-queratinas son mucho más fuertes que las α-queratinas y se hallan en los reptiles y las aves como parte de garras, escamas, plumas y picos. En los gecos, las microvellosidades que hay en sus patas (setas) también están compuestas por queratina.
Su estructura molecular está compuesta por láminas β-plegadas, formadas por cadenas polipeptídicas antiparalelas que se unen entre sí a través de enlaces o puentes de hidrógeno. Estas cadenas, una al lado de la otra, forman pequeñas superficies rígidas y planas, ligeramente plegadas.
Localización y funciones de la queratina
Las funciones de la queratina se relacionan, sobre todo, con el tipo de estructura que construye y el lugar del cuerpo del animal donde se encuentra.
Como otras proteínas fibrosas, esta confiere estabilidad y rigidez estructural a las células, ya que pertenece a la gran familia de proteínas conocida como filamentos intermedios, que son proteínas del citoesqueleto.
- En la protección y cobertura. La epidermis es la capa superior de la piel de los animales superiores que posee una gran red de filamentos intermedios formados por queratina. Tiene entre 30 micras y 1 nm de espesor en los humanos. La epidermis funciona como barrera protectora contra diferentes tipos de estrés mecánico y químico y es sintetizada por un tipo especial de células llamadas queratinocitos. Además de la epidermis, existe una capa aún más externa que se muda constantemente, y se conoce como estrato córneo, que cumple funciones similares. Espinas, escamas y púas también son empleadas por diversos animales para su propia protección contra depredadores y otros agresores.
- En la defensa y otras funciones. Los cuernos son estructuras muy fuertes y resistentes y los animales que los tienen los emplean como órganos de defensa y cortejo. Están formados por un centro óseo compuesto por hueso “esponjoso”, recubierto por piel, que se proyecta desde la zona posterior del cráneo. Las garras y las uñas, además de sus funciones en la alimentación y sujeción, también les sirven a los animales como “armas” de defensa contra atacantes y depredadores. En esta función entran los picos de las aves y los dientes de animales no mandibulados.
- En el movimiento. Los cascos de muchos animales rumiantes y ungulados (caballos, asnos, alces, etc.) están compuestos por queratina, son muy resistentes y están diseñados para proteger las patas y colaborar en el movimiento. Las plumas, que también son empleadas por los pájaros para desplazarse, están compuestas por β-queratina. Estas estructuras, además, tienen funciones en el camuflaje, en el cortejo, en el aislamiento térmico y en la impermeabilidad.

- En la industria. La industria textil es una de las principales explotadoras de las estructuras queratinizadas, antropocéntricamente hablando. La lana y el pelo de muchos animales tiene importancia a nivel industrial, pues con ellos se manufacturan diversas prendas que son útiles a los humanos desde diversos puntos de vista. También se fabrican productos cosméticos para suavizar el cabello.
Referencias
- Koolman, J., & Roehm, K. Color Atlas of Biochemistry (2nd ed.). Thieme.
- Mathews, C., van Holde, K., & Ahern, K. Biochemistry (3th ed.). Pearson.
- Nelson, D. L., & Cox, M. M. Lehninger Principios de Bioquímica. Ediciones Omega (5th ed.).
- Pauling, L., & Corey, R. The Structure of Hair, Muscle, and Related Proteins. Chemistry.
- Wang, B., Yang, W., McKittrick, J., & Meyers, M. A. Keratin: Structure, mechanical properties, occurrence in biological organisms, and efforts at bioinspiration. Progress in Materials Science.