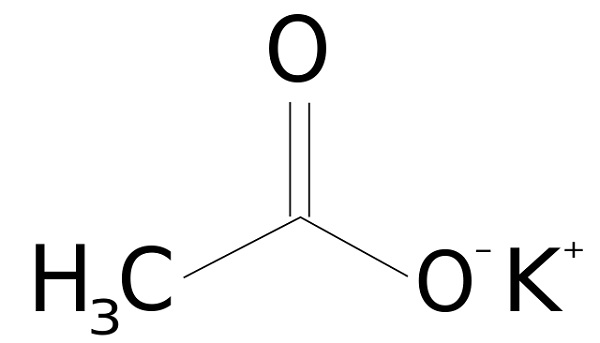
El acetato de potasio es un compuesto orgánico formado por un ion potasio K+ y un ion acetato CH3COO–. Su fórmula química es CH3COOK, o KCH3COO, o también C2H3KO2. Se trata de un sólido cristalino incoloro o blanco, muy soluble en agua.
Se emplea para regular la acidez de ciertos alimentos procesados industrialmente. Por su gran afinidad con el agua se utiliza en los laboratorios o en ciertos procesos para absorber el agua de otros compuestos, como por ejemplo para deshidratar alcohol.

El acetato de potasio participa en algunas reacciones químicas como acelerador de estas y en la síntesis de compuestos orgánicos. Permite también aumentar la formación de anticuerpos (sustancias naturales que combaten infecciones) en métodos industriales para producirlos.
Sus propiedades a muy bajas temperaturas lo convierten en un buen candidato para ser empleado en mezclas para fundir hielo en carreteras de concreto en climas muy fríos. Según fuentes consultadas se utiliza también en equipos para combatir incendios y en montajes para observar células en microscopios.
[toc]
Estructura
El acetato de potasio está formado por un catión potasio K+ y un anión acetato CH3COO–. Este último es la base conjugada del ácido acético CH3COOH. El ion acetato CH3COO– está formado por un metilo -CH3 unido a un carboxilato -COO–.
La unión entre ambos iones es electrostática o iónica, es decir, la unión entre un ion positivo y uno negativo.
Nomenclatura
- Acetato de potasio
- Etanoato de potasio
- Sal de potasio del ácido acético
- AcOK
- KOAc
Propiedades
Estado físico
Sólido incoloro o blanco cristalino.
Peso molecular
98,14 g/mol
Punto de fusión
292 ºC
Densidad
1,6 g/cm3
Solubilidad
Muy soluble en agua: 256 g/100 mL a 20 °C.
pH
Una solución acuosa al 5% de acetato de potasio posee un pH de 7,5-9,0.
Otras propiedades
En ocasiones posee un débil olor a vinagre. En solución al 10% no ataca el aluminio a temperatura ambiente pero a 60-70 °C el metal se oscurece y sufre picaduras.
A concentraciones del 20% o más ocurre ataque superficial al aluminio a cualquier temperatura.
El acetato de potasio (AcOK) es altamente soluble en agua. Posee un hidrato: el KCH3COO.1,5H2O, el cual es el sólido que se obtiene al cristalizarlo desde las soluciones acuosas de AcOK.
Comportamiento al calentarse
Si se somete a calentamiento el acetato de potasio (AcOK) hidratado (KCH3COO.1,5H2O ) al llegar a 40 °C comienza a perder el agua de hidratación.
KCH3COO.1,5H2O → KCH3COO + 1,5H2O↑
Si se calienta el acetato de potasio anhidro (sin agua: KCH3COO), al llegar a 340 °C comienza a descomponerse formando carbonato de potasio K2CO3 según la siguiente reacción:
2 KCH3COO + 4 O2 → K2CO3 + 3 H2O + 3 CO2↑
Obtención
Se puede preparar mediante la acción del hidróxido de potasio KOH sobre varios compuestos, como por ejemplo el ácido acético CH3COOH, el anhídrido acético (CH3CO)2O y el acetato de amonio CH3COONH4.
KOH + CH3COOH → CH3COOK + H2O
También se puede obtener haciendo reaccionar carbonato de potasio K2CO3 o bicarbonato de potasio KHCO3 con ácido acético CH3COOH.
KHCO3 + CH3COOH → CH3COOK + H2O + CO2↑
El acetato de potasio se puede cristalizar de una solución acuosa para obtenerlo con alta pureza.
Usos
En varias aplicaciones
El acetato de potasio se emplea en la industria de los alimentos procesados como regulador de la acidez. Es utilizado como desecante en métodos químicos para medir la permeabilidad al vapor de agua de algunas telas.
Sirve como agente deshidratante del etanol en la producción de este alcohol partiendo de lignocelulosa, un material derivado de la madera.
Se usa para producir antibióticos y se utiliza ampliamente en equipos para el combate de incendios.
En la industria de los polímeros
Se utiliza para reciclar poliuretanos pues sirve para catalizar o acelerar las reacciones de hidrólisis y glicólisis de dichos polímeros para que se conviertan en alcoholes y aminas.
Además se utiliza en la producción de resinas orgánicas de silicona.
En laboratorios de investigación científica y médica
El acetato de potasio de alta pureza se emplea en los laboratorios como reactivo en química analítica. También para realizar investigaciones medicocientíficas.
En laboratorios de histopatología sirve para asegurar un medio con pH neutro en los montajes para microscopio.

Es utilizado para la síntesis de compuestos orgánicos heterocíclicos, los cuales son compuestos con ciclos de diferente tamaño.
Ciertos microelectrodos que sirven para estudiar las propiedades eléctricas de las células, se rellenan con una solución concentrada de acetato de potasio.
En la producción industrial de anticuerpos
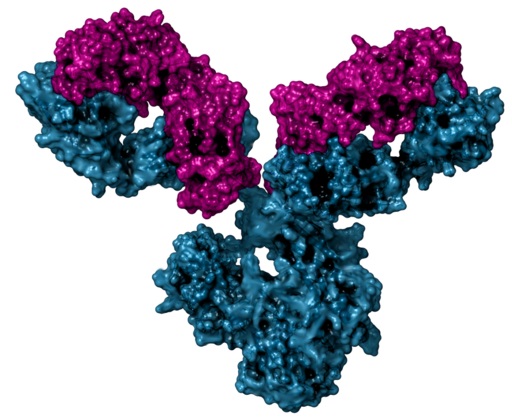
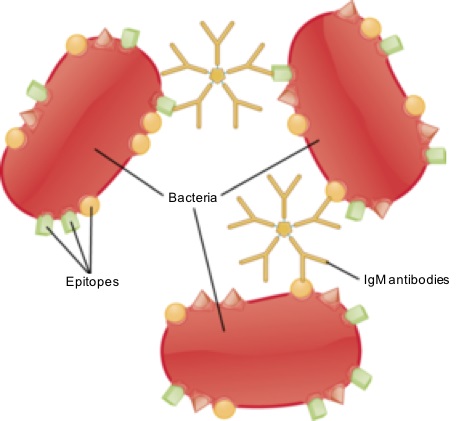
El acetato de potasio sirve para la producción a gran escala de anticuerpos monoclonales (que son los que provienen de una misma célula madre) en cultivos celulares. Permite estimular la síntesis o formación de los anticuerpos.
Los anticuerpos son sustancias producidos por algunas células de la sangre para combatir infecciones de virus o bacterias.
En mezclas antihielo
El acetato de potasio ha sido utilizado en mezclas antihielo (traducción del inglés anti-icing) con la finalidad de emplearlas para fundir hielo de carreteras y pavimentos de cemento y así permitir el uso seguro de estos.

La selección del acetato de potasio (AcOK) para esta aplicación se debe a que una solución acuosa al 50% en peso de AcOK es un eutéctico y posee un punto de fusión de -62 °C. Eso significa que aún a temperaturas tan bajas como -62 °C la solución permanece fundida.
Un eutéctico es una mezcla homogénea de componentes que tiene el menor punto de fusión de todas las mezclas posibles de estos, incluyendo el de los componentes puros.
Cómo funciona como antihielo
El acetato de potasio (AcOK) tiene una muy buena capacidad para fundir el hielo.
A -5 °C es capaz de fundir 11,5 Kg de hielo por cada Kg de AcOK. Esta propiedad va disminuyendo al disminuir la temperatura, pero aun a -50 °C tiene la habilidad de fundir 1,3 Kg de hielo por cada Kg de AcOH.
A -5 °C esta capacidad es comparable a la del cloruro de sodio o sal de mesa (NaCl), mientras que a partir de -30 °C la supera con creces.

Sin embargo, en las pruebas realizadas con el AcOK junto con otros compuestos se observó cierto grado de corrosión de las superficies de cemento, por lo que se planteó agregar anticorrosivos a las mezclas antihielo.
Por otra parte la mezcla de acetato de potasio (CH3COOK) con formiato de potasio (HCOOK) resulta un excelente antihielo y no requiere anticorrosivo.
Referencias
- Baker, F.J. et al. (1976). Staining Procedures. Aqueous mountants. In Introduction to Medical Laboratory Technology (Fifth Edition). Recuperado de sciencedirect.com.
- Hassan, A.A. et al. (2018). Indazoles: Synthesis and Bond-Forming Heterocyclization. In Advances in Heterocyclic Chemistry. Recuperado de sciencedirect.com.
- U.S. National Library of Medicine. (2019). Potassium acetate. Recuperado de pubchem.ncbi.nlm.nih.gov.
- Das, A. and Alagirusamy, R. (2010). Moisture transmission. Desiccant inverted cup method. In Science in Clothing Comfort. Recuperado de sciencedirect.com.
- Vargel, C. (2004). Carboxilic Acids and their Derivatives. Acetates. In Corrosion of Aluminum. Recuperado de sciencedirect.com.
- Cuevas, J. (2014). Electrophysiological Recording Techniques. Intracellular Recording Techniques. In Reference Module in Biomedical Sciences. Recuperado de sciencedirect.com.
- Fink, J.K. (2018). Poly(urethane)s. Recycling. Solvolysis. In Reactive Polymers: Fundamentals and Applications (Third Edition). Recuperado de sciencedirect.com.
- Fong, W. et al. (1997). Optimization of monoclonal antibody production: combined effects of potassium acetate and perfusion in a stirred tank bioreactor. Cytotechnology 24: 47-54. Recuperado de link.springer.com.
- Danilov, V.P. et al. (2012). Low-Temperature Anti-Icing Reagents in Aqueous Salt Systems Containing Acetates and Formiates. Theoretical Foundations of Chemical Engineering, 2012, Vol 46, No. 5, pp. 528-535. Recuperado de link.springer.com.
- Fakeev, A.A.et al. (2012). Research and Development of Method for Potassium Acetate of High Purity. Journal of Applied Chemistry, 2012, Vol. 85, No.12, pp. 1807-1813. Recuperado de link.springer.com.