¿Qué es la autofagia?
La autofagia es un proceso catabólico de degradación que ocurre de manera conservada en los lisosomas de todas las células eucariotas (y las vacuolas de las levaduras). El vocablo se utiliza para referirse a la degradación de los componentes del citosol o las partes de la célula que son “obsoletas”, o que han dejado de funcionar correctamente.
El término autofagia fue acuñado en 1963, en la Universidad Rockefeller por Christian de Duve, quien también observó y describió los procesos de endocitosis celular. Literalmente, la palabra autofagia significa “consumirse a uno mismo”, aunque algunos autores lo describen como “autocanibalismo”.
La autofagia es capaz de remover orgánulos intracelulares completos y grandes complejos o agregados proteicos de forma no selectiva.
A pesar de esta fagocitosis no selectiva, diferentes investigaciones han demostrado que la autofagia tiene numerosas implicaciones fisiológicas y patológicas. Se activa durante los periodos de adaptación a la inanición, durante el desarrollo, para la eliminación de microorganismos invasores, durante la muerte celular programada, para la eliminación de tumores, la presentación de antígenos, etc.
Características de la autofagia
– Mediación. Es un proceso mediado por un orgánulo citoplasmático conocido como lisosoma.
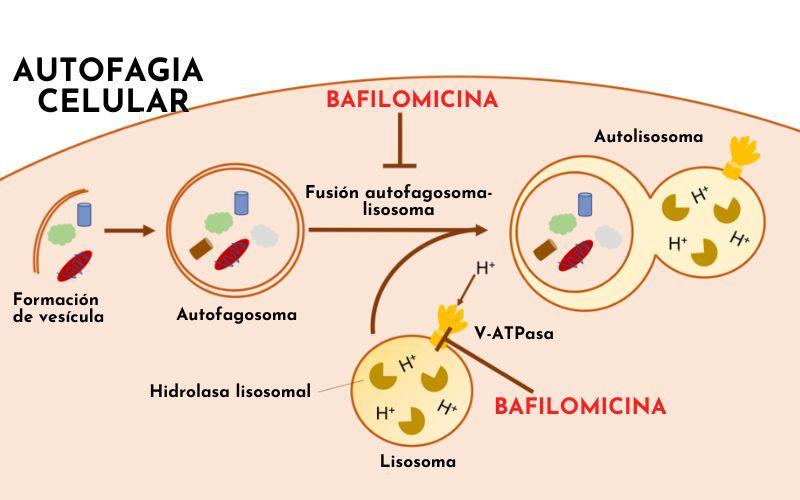
– Pasos. Comienza con la encapsulación del orgánulo que será degradado por una membrana doble, formando un cuerpo membranoso conocido como autofagosoma. La membrana del autofagosoma se funde, posteriormente, con la membrana lisosomal o con un endosoma tardío.
– Funciones en el organismo. Cada uno de estos pasos entre el secuestro, la degradación y la liberación de los aminoácidos u otros componentes para su reciclaje ejerce diferentes funciones en distintos contextos celulares, lo que hace que la autofagia sea un sistema altamente multifuncional.
– Proceso conservado evolutivamente. Es un proceso evolutivamente conservado que se halla en la mayoría de los organismos eucariotas, desde levaduras hasta mamíferos.
– Control. También resulta un proceso muy controlado, puesto que solo los componentes celulares marcados son dirigidos hacia esta vía de degradación, y el marcaje ocurre, generalmente, durante los procesos de remodelación celular. Por ejemplo, cuando una célula hepática establece una respuesta de desintoxicación en respuesta a drogas liposolubles, su retículo endoplásmico liso prolifera considerablemente, y cuando el estímulo generado por la droga disminuye, el exceso de retículo endoplásmico liso es removido del espacio citosólico por autofagia.
– Inducción de la autofagia. Uno de los eventos que más comúnmente desencadena los procesos autofágicos es la inanición. En las levaduras, por ejemplo, la falta de nitrógeno es el estímulo más eficiente, lo que también es válido para las células vegetales. A pesar de que no se entiende completamente, las células poseen sensores especiales para determinar cuándo un nutriente o aminoácido esencial está en muy bajos niveles, y desencadena todo el proceso de reciclaje a través de los lisosomas.
Tipos de autofagia
Existen tres tipos principales de autofagia entre los eucariotas: la macroautofagia, la microautofagia y la autofagia mediada por chaperonas. A menos que se especifique, el término autofagia hace referencia a la macroautofagia.
- Macroautofagia. Este tipo depende de la formación de novo de unas vesículas fagocíticas conocidas como autofagosomas. La formación de estas vesículas es independiente de la formación de “yemas” de membrana, pues se forman por expansión. En las levaduras, la formación de los autofagosomas comienza en un sitio particular conocido como el PAS, mientras que en los mamíferos ocurre un muchos sitios diferentes del citosol, probablemente vinculados con el retículo endoplásmico mediante unas estructuras conocidas como omegasomas. El tamaño de los autofagosomas es muy variable y depende del organismo y del tipo de molécula u orgánulo que se fagocita. Puede variar desde 0.4-0.9 μm de diámetro en levaduras hasta 0.5-1.5 μm en mamíferos. Cuando las membranas del autofagosoma y el lisosoma se funden, el contenido de estos se mezcla y entonces comienza la digestión de los sustratos blanco de la autofagia. Este orgánulo se conoce como autolisosoma. Para algunos autores, la macroautofagia puede subclasificarse, a su vez, en autofagia inducida y basal. La macroautofagia inducida es empleada para producir aminoácidos luego de un período prolongado de inanición. La basal se refiere al mecanismo constitutivo (siempre activo) esencial para el recambio de los distintos componentes citosólicos y los orgánulos intracelulares.
- Microautofagia. Es el proceso en el cual el contenido citoplásmico es introducido al lisosoma a través de invaginaciones que se producen en la membrana de dicho orgánulo. Una vez introducidas en el lisosoma, las vesículas producidas por estas invaginaciones flotan libremente en el lumen hasta que son lisadas y su contenido liberado y degradado por enzimas específicas.
- Autofagia mediada por chaperonas. Este tipo solo ha sido reportado para las células de mamíferos. A diferencia de la macroautofagia y la microautofagia, donde se fagocitan inespecíficamente algunas porciones citosólicas, la autofagia mediada por chaperonas es bastante específica, pues depende de la presencia de unas secuencias pentapeptídicas particulares en los sustratos que serán fagocitados. Algunos investigadores han determinado que este motivo pentapéptido está relacionado con la secuencia KFERQ y que el mismo se encuentra en más del 30% de las proteínas citosólicas. Se denomina “mediada por chaperonas” porque unas proteínas chaperonas se encargan de mantener expuesto este motivo conservado para facilitar su reconocimiento y evitar el plegamiento de la proteína sobre el mismo. Las proteínas con esta etiqueta son translocadas al lumen lisosomal y degradadas allí. Muchos de los sustratos de la degradación son enzimas glucolíticas, factores de transcripción y sus inhibidores, proteínas de unión a calcio o a lípidos, subunidades de proteosomas y algunas proteínas implicadas con el tráfico vesicular. Así como los otros dos tipos de autofagia, la autofagia mediada por chaperonas es un proceso regulado en muchos niveles, desde el reconocimiento de las etiquetas hasta el transporte y la degradación de los sustratos en el interior de los lisosomas.
Funciones de la autofagia
- Reciclaje de componentes celulares. Es un proceso de reciclaje donde las células degradan y reciclan componentes celulares no deseados o dañados, como proteínas mal plegadas, orgánulos disfuncionales o agregados proteicos, y le permite a la célula mantener su homeostasis y conservar recursos.
- Eliminación de patógenos intracelulares. Desempeña un papel importante en la defensa celular contra infecciones intracelulares. Este proceso, conocido como autofagia selectiva de patógenos (xenofagia), ayuda a eliminar virus, bacterias y otros patógenos que hayan invadido la célula.
- Supervivencia celular bajo estrés. Se activa en respuesta a condiciones de estrés celular, como inanición, hipoxia, estrés oxidativo o presencia de toxinas. Al reciclar componentes celulares y proporcionar nutrientes adicionales, la autofagia ayuda a las células a adaptarse y sobrevivir en condiciones adversas.
- Regulación del crecimiento y desarrollo celular. Participa en la regulación del tamaño y la proliferación celular, pues el adecuado equilibrio autofágico es imprescindible para el desarrollo normal de los tejidos y la prevención de enfermedades como el cáncer.
- Longevidad y envejecimiento. Se ha sugerido que también puede influir en la longevidad y el proceso de envejecimiento. Su activación puede promover la longevidad al mantener la salud celular y prevenir la acumulación de daño celular asociado al envejecimiento.
Estudios de Yoshinori Ohsumi sobre la autofagia
Yoshinori Ohsumi, investigador japonés ganador en 2016 del Nobel de fisiología y medicina, describió los mecanismos moleculares de la autofagia en levaduras mientras estudiaba el destino metabólico de muchas proteínas y las vacuolas de estos organismos unicelulares.
En sus trabajos, no solo identificó las proteínas y las rutas implicadas en el proceso, sino que demostró cómo está regulada la ruta de la autofagia gracias a la acción de proteínas capaces de “censar” diferentes estados metabólicos.
Sus trabajos comenzaron con observaciones microscópicas precisas de las vacuolas durante eventos de intensa degradación. Las vacuolas son como los sitios de almacenamiento de la “basura” y los desechos celulares de las levaduras.
Mediante la observación de levaduras con genotipos mutantes defectivos para distintos genes relacionados o hipotéticamente relacionados con la autofagia (conocidos como genes ATG), el investigador pudo describir el sistema autofágico de levaduras a nivel genético.
Posteriormente, coon su grupo de investigadores, determinó las principales características genéticas de las proteínas codificadas por estos genes e hicieron aportes significativos sobre su interacción y la formación de los complejos responsables del inicio y la ejecución de la autofagia en levaduras.
Gracias a los trabajos de Ohsumi, hoy en día comprendemos mejor los aspectos moleculares de la autofagia, y sus importantes implicaciones en el correcto funcionamiento de las células y los órganos que nos componen.
Referencias
- Alberts, B., Johnson, A., Lewis, J., Morgan, D., Raff, M., Roberts, K., & Walter, P. Molecular Biology of the Cell (6th ed.). Garland Science.
- Klionsky, D.J., & Emr, S.D. Autophagy as a regulated pathway of cellular degradation. Science.
- Mizushima, N. Autophagy: process and function. Genes & Development.
- Mizushima, N., Komatsu, M. Autophagy: Renovation of cells and tissues. Cell.
- Rabinowitz, J.D., & White, E. Autophagy and metabolism. Science.