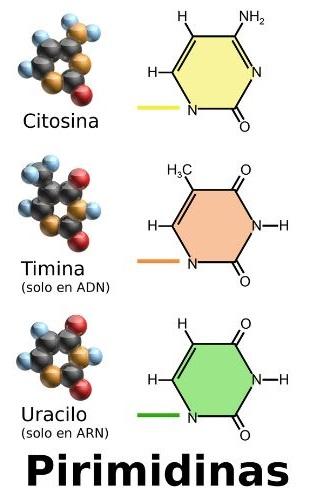
¿Qué es la citosina?
La citosina es una base nitrogenada tipo pirimidina, que sirve para la biosíntesis de citidín-5′-monofosfato y de desoxicitidín-5′-monofosfato. Estos compuestos sirven para la biosíntesis, respectivamente, del ácido desoxirribonucleico (ADN) y del ácido ribonucleico (ARN). El ADN almacena la información genética y el ARN tiene diversas funciones.
En los seres vivos, la citosina no se encuentra de forma libre, sino que comúnmente forma ribonucleótidos o desoxirribonucleótidos. Ambos tipos de compuesto poseen un grupo fosfato, una ribosa y una base nitrogenada.
El carbono 2 de la ribosa tiene un grupo oxhidrilo (-OH) en los ribonucleótidos, y un átomo de hidrógeno (-H) en los desoxirribonucleótidos. Dependiendo del número de grupos fosfato presentes, existe citidín-5′-monofosfato (CMP), citidín-5′-difosfato (CDP) y citidín-5′-trifosfato (CTP).
Los equivalentes desoxigenados se llaman desoxicitidin-5′-monofosfato (dCMP), desoxicitidin-5′-difosfato (dCDP), y desoxicitidin-5′-trifosfato (dCTP).
La citosina, en sus diversas formas, participa en diferentes funciones, como la biosíntesis de ADN y ARN, la biosíntesis de glicoproteínas y la regulación de la expresión del gen.
Estructura y propiedades de la citosina
- Fórmula. La citosina, 4-amino-2-hidroxipirimidina, posee la fórmula empírica C4H5N3O
- Peso molecular. 111,10 g/mol.
- Aspecto. Como un polvo blanco.
- Estructura molecular. Es un anillo heterocíclico, aromático y planar. La longitud de onda de absorbancia máxima (ʎmax) se encuentra a 260 nm.
- Punto de fusión. Supera los 300 ºC.
- Reacciones. Para formar un nucleótido, la citosina se une covalentemente, a través del nitrógeno 1, mediante un enlace N-beta-glicosídico al carbono 1′ de la ribosa. El carbono 5′ es esterificado con un grupo fosfato.
Biosíntesis de la citosina
La biosíntesis de nucleótidos de pirimidinas tiene una vía común, que consiste en seis pasos catalizados por enzimas.
- Primer paso. La vía comienza con la biosíntesis de carbamoil-fosfato. En los procariotas hay una sola enzima: la carbamoil fosfato sintasa. Esta se encarga de la síntesis de pirimidinas y glutamina. En los eucariotas, hay carbamoil fosfato sintasa I y II, que se encargan, respectivamente, de la biosíntesis de glutamina y pirimidinas.
- Segundo. Consiste en la formación de N-carbamoilaspartato, a partir de carboil fosfato y aspartato, reacción catalizada por la aspartato transcabamoilasa (ATCasa).
- Tercero. Síntesis de L-dihidrorotato, que produce el cierre del anillo de pirimidina. Este paso es catalizado por la dihidrootasa.
- Cuarto. Formación de orotato, reacción redox catalizada por la dihidroorotato deshidrogenasa.
- Quinto. Formación de orotidilato (OMP) usando fosforibosil pirofosfato (PRPP) como sustrato, y la orotato fosforibosil transferasa como catalizador.
- Sexto. Formación de uridilato (uridin-5′-monofosfato, UMP), reacción catalizada por una OMP-descarboxilasa.
Los pasos siguientes consisten en la fosforilación del UMP, catalizada por quinasas, para formar UTP, y la transferencia de un grupo amino desde la glutamina al UTP para formar CTP, reacción catalizada por CTP sintetasa.
- Regulación de la biosíntesis. En los mamíferos, la regulación tiene lugar a nivel de la carbamoil fosfato sintasa II, una enzima que se encuentra en el citosol, mientras que la carbamoil fosfato sintasa I es mitocondrial. La carbamoil fosfato sintasa II es regulada mediante retroalimentación negativa. Sus reguladores, el UTP y el PRPP, son, respectivamente, inhibidor y activador de esta enzima. En los tejidos no hepáticos, la carbamoil fosfato sintasa II es la única fuente de carbamoil fosfato. Mientras que en el hígado, bajo condiciones de exceso de amoníaco, la carbamoil fosfato sintasa I produce, en la mitocondria, carbamoil fosfato, el cual es transportado hacia el citosol, desde donde ingresa a la vía de biosíntesis de las pirimidinas. Otro punto de regulación es la OMP-descarboxilasa, la cual es regulada mediante inhibición competitiva. El producto de su reación, UMP, compite con el OMP por el sitio de unión en la OMP-descarboxilasa.
- Las pirimidinas, como la citosina, son recicladas. El reciclaje de las pirimidinas tiene como función la reutilización de las pirimidinas sin necesidad de realizar biosíntesis de novo, y evitar la vía degradativa. La reacción de reciclaje es catalizada por la pirimidina fosforribosiltransferasa. La reacción general es la siguiente:
Pirimidina + PRPP -> pirimidina nucleosido 5′-monofosfato + PPi
En los vertebrados, la pirimidina fosforribosiltransferasa se encuentra en los eritrocitos. Las pirimidinas sustrato de esta enzima son uracilo, timina y orotato. La citosina es reciclada de forma indirecta a partir de uridin-5′-monofosfato.
Funciones de la citosina
- En la biosíntesis del ADN. Durante la replicación del ADN, la información es copiada en el ADN mediante una ADN polimerasa. La biosíntesis de ARN necesita de desoxinucleótidos trifosfato (dNTP), a saber: desoxitimidin trifosfato (dTTP), desoxicitidin trifosfato (dCTP), desoxiadenin trifosfato (dATP) y desoxiguanin trifosfato (dGTP). La reacción es:
(ADN)n residuos + dNTP -> (ADN)n+1 residuo + PPi
La hidrólisis del pirofosfato inorgánico (PPi) proporciona la energía para la biosíntesis del ARN.
- En la estabilización de la estructura del ADN. En la doble hélice de ADN, una purina de una cadena, está unida a la pirimidina de la cadena opuesta, mediante enlaces de hidrógeno. Así, la citosina está siempre unida a la guanina mediante tres enlaces de hidrógeno: la adenina está unida a la timina mediante dos enlaces de hidrógeno. Los enlaces de hidrógeno se rompen cuando una solución de ADN nativo purificado, a pH 7, es sometida a temperaturas superiores a 80 ºC. Esto ocasiona que la doble hélice de ADN forme dos cadenas separadas. Este proceso se conoce como desnaturalización. La temperatura a la cual se desnaturaliza el 50% del ADN se conoce como temperatura de fusión (Tm). Las moléculas de ADN cuya proporción de guanina y citosina es mayor respecto a la de timina y adenina tienen valores de Tm más grandes que aquéllas cuya proporción de bases es inversa. Lo anteriormente descrito constituye la prueba experimental de que un mayor número de enlaces de hidrógeno estabiliza mejor las moléculas de ADN nativo.
- De las regiones ricas en citosina en el ADN. Recientemente, se encontró que el ADN del núcleo de células humanas puede adoptar estructuras de motivos intercalados (iM). Estas estructuras se producen en regiones ricas en citosina. La estructura iM consiste en cuatro cadenas de ADN, a diferencia del ADN de doble hélice clásico que tiene dos cadenas. Más específicamente, dos cadenas dúplex paralelas están intercaladas en una orientación antiparalela, y son mantenidas juntas por un par de citosinas hemiprotonadas (C:C+). En el genoma humano, las estructuras iM se encuentran en regiones como los promotores y los telómeros. El número de estructuras iM es mayor durante la fase G1/S del ciclo celular, en la cual la transcripción es alta. Estas regiones son sitios de reconocimiento de proteínas implicadas en la activación de la maquinaria transcripcional. Por otra parte, en las regiones ricas en pares de bases de guanina (C) consecutivas, el ADN tiende a adoptar la forma de hélice A, en condiciones deshidratantes. Esta forma es típica del ARN y de las bandas mixtas dobles de ADN-ARN durante la transcripción y la replicación, y en ciertos momentos cuando el ADN está unido a proteínas. Se ha demostrado que las regiones con bases consecutivas de citosina crean un parche electropositivo en la hendidura mayor del ADN. Por ello, se cree que estas regiones se unen a proteínas, lo cual predispone ciertas regiones genómicas a la fragilidad genética.
- En la biosíntesis del ARN. Durante la transcripción, la información contenida en el ADN es copiada en el ARN mediante una ARN polimerasa. La biosíntesis de ARN necesita de nucleósidos trifosfato (NTP), a saber: citidina trifosfato (CTP), uridina trifosfato (UTP), adenina trifosfato (ATP) y guanina trifosfato (GTP). La reacción es:
(ARN)n residuos + NTP -> (ARN)n+1 residuo + PPi
La hidrólisis del pirofosfato inorgánico (PPi) proporciona la energía para la biosíntesis del ARN.
- En la biosíntesis de glicoproteínas. La transferencia secuencial de hexosas para formar los oligosacáridos, O-ligados a las proteínas, sucede a partir de precursores nucleótidos. En los vertebrados, el último paso de la biosíntesis de oligosacáridos O-ligados consiste en la adición de dos residuos de ácido siálico (N-acetilneuramínico) a partir de un precursor de citidin-5′-monofosfato (CMP). Esta reacción se produce en el saco trans del Golgi.
La citosina y los tratamientos quimioterapéuticos contra el cáncer
El ácido tetrahidrofolato (FH4) es una fuente de grupos -CH3, y es necesario para la biosíntesis de dTMP a partir de dUMP. Se forma además FH2. La reducción de FH2 a FH4 requiere de una reductasa del folato y del NADPH. Algunos inhibidores de la reductasa del folato, como aminopterina y metotrexato, son empleados en tratamientos contra el cáncer.
El metotrexato es un inhibidor competitivo. La reductasa del folato se une con 100 veces más afinidad a este inhibidor que a su sustrato. La aminopterina actúa de forma similar.
La inhibición de la reductasa del folato dificulta de forma indirecta la biosíntesis de dTMP, y por ende la de dCTP. La inhibición directa sucede mediante los inhibidores de la enzima sintetasa del timidilato, que cataliza de dTMP a partir se dUMP. Estos inhibidores son 5-fluorouracilo y la 5-fluoro-2-desoxiuridina.
Por ejemplo, 5-fluoroacilo no es por sí mismo un inhibidor sino que primero se convierte, en la vía de reciclaje, en desoxiuridin mofosfato d(FdUMP), el cual se une a la sintetasa del timidilato y la inhibe.
Las sustancias análogas a la glutamina, azaserina y acivicina, inhiben la glutamina amidotransferasa. La azarina fue una de las primeras sustancias descubiertas que actúan como inactivador suicida.
Referencias
- Bohinski, R. Bioquímica. Addison-Wesley Iberoamericana.
- Devlin, T.M. Bioquímica. Editorial Reverté.
- Nelson, D. L., Cox, M. M. Lehninger–Principles of biochemistry. W.H. Freeman.
- Voet, D. and Voet, J. Biochemistry. John Wiley and Sons.