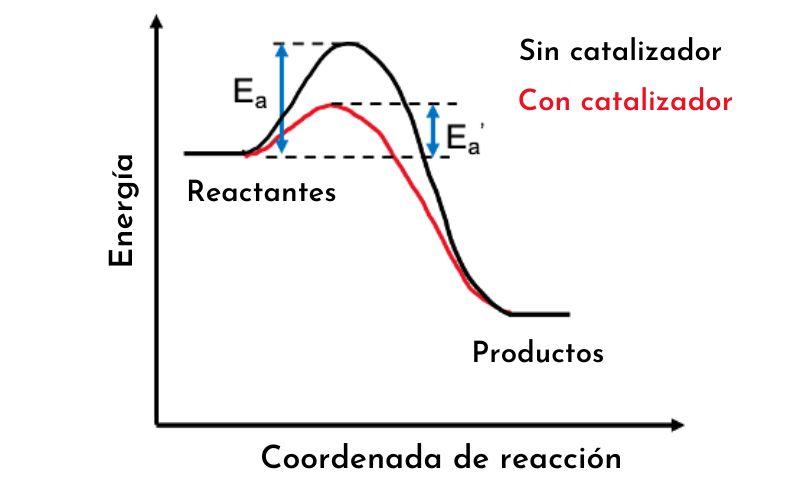
¿Qué es un diagrama energético?
Un diagrama energético es una gráfica de energía que ilustra el proceso que ocurre a lo largo de una reacción. Los diagramas energéticos también se definen como la visualización de una configuración electrónica en orbitales: cada representación es un electrón de un orbital con una flecha.
Por ejemplo, en un diagrama energético, las flechas que apuntan en dirección superior representan un electrón con un giro positivo. A su vez, las flechas que apuntan hacia abajo, se encargan de representar a un electrón con giro negativo.
Existen dos tipos de diagramas energéticos. Los diagramas de termodinámica o química orgánica, los cuales muestran la cantidad de energía generada o gastada a lo largo de una reacción, comenzando desde que los elementos se encuentran como reactivos, pasando por un estado de transición, hasta los productos.
Y los diagramas de química inorgánica, que sirven para demostrar los orbitales moleculares, según el nivel de energía que tengan los átomos.
Características de los diagramas energéticos
– Son diagramas especializados, que requieren de preparación.
– Cada representación que aparece en un diagrama, es un electrón de un orbital con una flecha.
– Sirven para medir diversos estados energéticos (termodinámicos) de la materia, como volumen y presión.
– Se pueden utilizar en el área de medicina, como fisiología cardiovascular, fisiología respiratoria o fisiología termodinámica.
– Constituyen una ayuda para la medición de la energía producida por un elemento, y, por lo tanto, tienen aplicación en la mecánica cuántica, porque muestran los niveles energéticos atómicos.
Tipos de diagramas energéticos
Diagramas de termodinámica
Los diagramas termodinámicos se utilizan para representar los estados termodinámicos de una materia (típicamente fluidos) y las consecuencias de la manipulación de este material.
Por ejemplo, un diagrama de temperatura entrópica puede usarse para demostrar el comportamiento de un fluido a medida que cambia por un compresor.
Los diagramas de Sankey son diagramas energéticos en los cuales el grosor de las flechas son mostradas proporcionalmente a la cantidad de flujo.
Este diagrama representa todo el flujo primario de energía de una fábrica. El grosor de las bandas es directamente proporcional a la energía de producción, uso y pérdidas.
Las fuentes primarias de energía son el gas, la electricidad y carbón/aceite, y representan el ingreso de energía al lado izquierdo del diagrama.
También se pueden visualizar los gastos de energía, el flujo material a nivel regional o nacional, y el desglose del costo de un elemento o servicios.
Estos diagramas ponen un énfasis visual en las transferencias grandes de energía o flujos dentro de un sistema.
Y son muy útiles a la hora de localizar contribuciones dominantes en un flujo general. A menudo estos diagramas muestran cantidades conservadas dentro de los límites de un sistema definido.
Diagrama P-V
Se emplea para describir cambios correspondientes a las medidas de volumen y presión en el sistema. Son comúnmente usados en la termodinámica, fisiología cardiovascular y fisiología respiratoria.
Los diagramas P-V originalmente eran llamados diagramas indicadores. Fueron desarrollados en el siglo XVIII como herramientas para comprender la eficiencia de los motores de vapor.
Un diagrama P-V muestra el cambio en presión P con respecto al volumen de V de algún proceso o procesos.
En la termodinámica, estos procesos forman un ciclo, de manera que cuando el ciclo culmine no haya ningún cambio en el estado del sistema, como por ejemplo, en un aparato que retorna a su presión y volumen inicial.
Diagrama T-S
Se usa en la termodinámica para visualizar los cambios de temperatura y entropía específica durante un proceso o ciclo termodinámico.
Es muy útil y una herramienta muy común en el área, particularmente porque ayuda a visualizar la transferencia de calor durante un proceso.
Para procesos reversibles o ideales, el área debajo de la curva T-S de un proceso es el calor transferido al sistema durante ese proceso.
Un proceso isentrópico se grafica como una línea vertical en un diagrama T-S, mientras que un proceso isotérmico se grafica como una línea horizontal.
Diagramas de química inorgánica
Sirven para representar o esquematizar los orbitales moleculares relacionados con los átomos y su nivel de energía.
Diagrama de energía potencial del etano
Las distintas conformaciones del etano no tienen la misma energía, ya que tienen una repulsión electrónica distinta entre hidrógenos.
A medida que se gira la molécula, partiendo de una conformación ya alternada, la distancia entre los átomos de hidrógeno de los grupos particulares de metilo comienzan a reducirse. La energía potencial de ese sistema va a aumentar hasta que llegue a una conformación eclipsada.
Se pueden representar gráficamente los diferentes tipos de energía entre las conformaciones varias. En el diagrama del etano se observa cómo las conformaciones eclipsadas son los máximos de energía. Por otro lado, las alternadas serían los mínimos.
Ejemplos de diagramas energéticos
Diagrama T-S
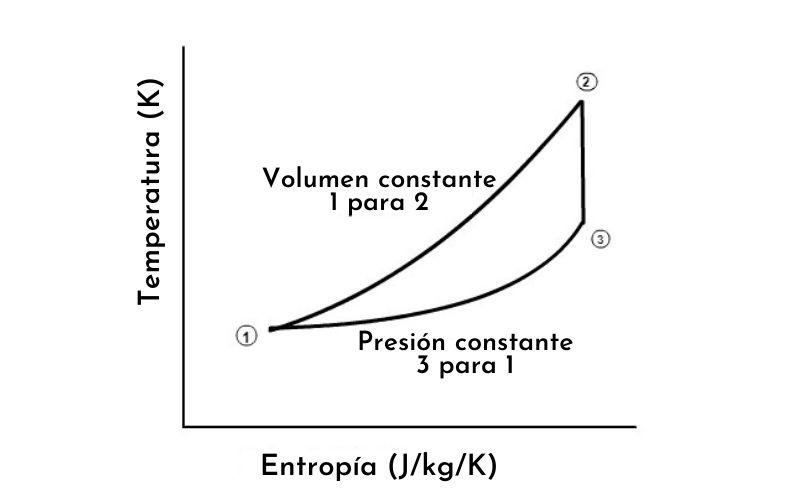
Diagrama P-V
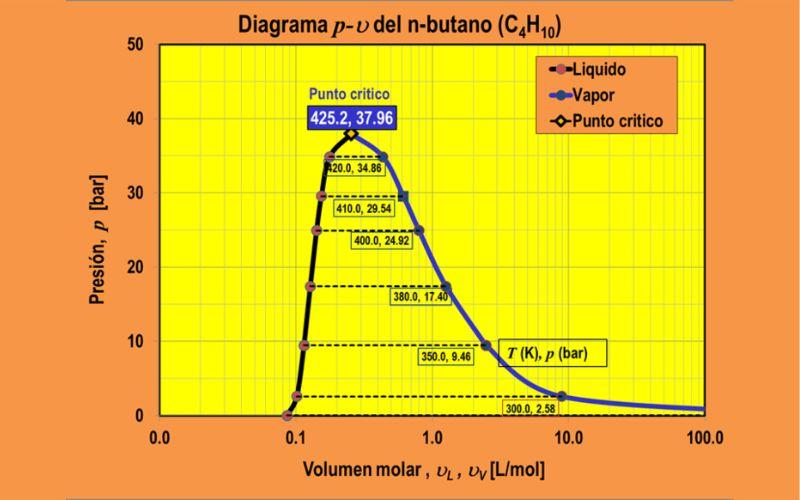
Es un diagrama P-V del n-butano.
Diagrama del etano
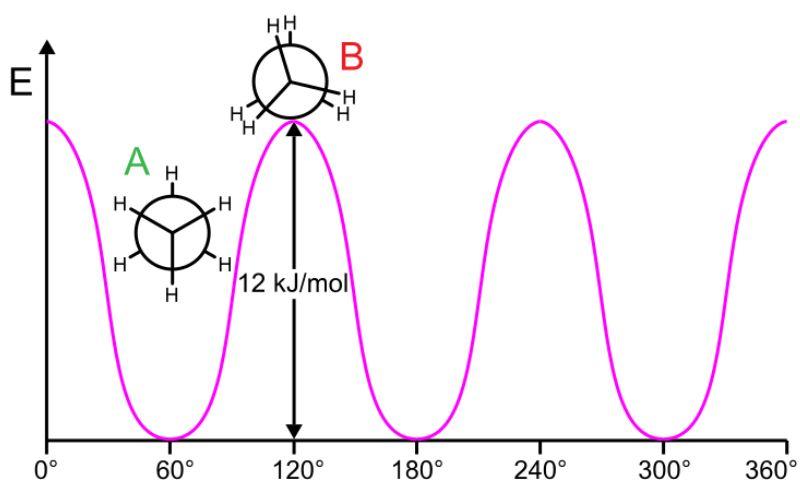
Este diagrama muestra las proyecciones de Newman de las conformaciones del etano y sus diferencias energéticas relativas (no energías totales). Cuando el etano gira alrededor de uno de sus enlaces covalentes, se forman estas conformaciones. El ángulo torsional/diédrico se muestra en el eje x.
A: escalonado / B: eclipsado
Referencias
- T-S diagram. Recuperado de en.wikipedia.org
- Sankey diagram. Recuperado de en.wikipedia.org