¿Qué es un emulsificante?
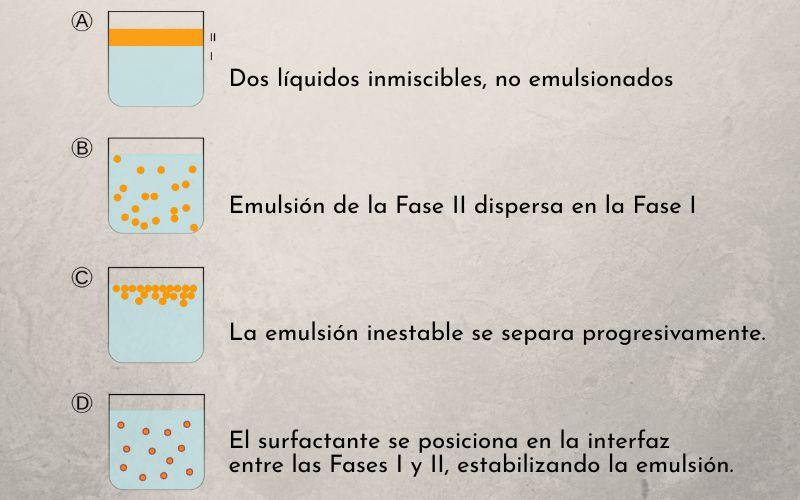
Un emulsificante, o emulsionante, es una sustancia que mezcla y estabiliza dos líquidos inmiscibles (que no se mezclan) para formar una emulsión homogénea.
El ejemplo clásico para entender lo que significa un emulsificante es el de un vaso con aceite y agua. El aceite se quedará arriba, con menor densidad, mientras que el agua se situará abajo. Ambos líquidos son inmiscibles, ya que sus afinidades intermoleculares difieren entre sí; el agua es polar, y el aceite apolar.
No obstante, si a la mezcla heterogénea y bifásica agua (w)-aceite (o) se le adiciona una yema de huevo, agitándose fuertemente, se formará una emulsión de agua en aceite (w/o), si el aceite se encuentra disperso y en menor proporción; o aceite en agua (o/w), si ahora es el agua la que se halla dispersa. Así pues, la yema de huevo sería el emulsificante.
De lo anterior, agregando además otros aditivos, obtenemos la mayonesa. Como la mayonesa, otros productos alimenticios como la margarina, mantequilla de maní, leche, salsas de tomate, aderezos, etc., se elaboran gracias a la adición de un emulsificante.
Proceso de emulsión
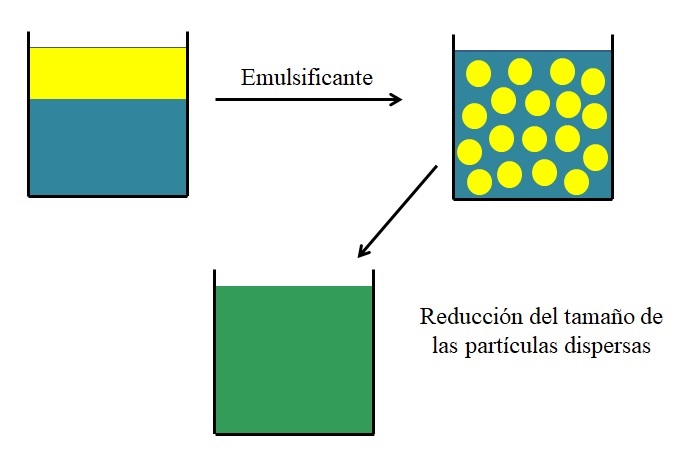
El emulsificante permite que se forme una emulsión a partir de dos líquidos o mezclas inmiscibles. Las emulsiones w/o y o/w son los dos casos más importantes. En la imagen de arriba se muestra de manera simplificada lo ya explicado.
Nótese que tenemos dos líquidos: uno azulado y otro amarillo, que componen una mezcla heterogénea bifásica. Son inmiscibles, por lo que no coalescen para originar una mezcla homogénea. Sin embargo, al agregarse el emulsificante (ya sea sólido o líquido), este interviene de tal modo que se forman glóbulos o partículas dispersas del líquido amarillo.
Si las partículas amarillas lograran coalescer, tendríamos de nuevo una fase amarilla como en el inicio. Mientras más pequeñas sean dichas partículas, la mezcla resultante tendrá una textura más suave y uniforme. Por lo tanto, a partir de esta mezcla hipotética veríamos una mezcla de color verde; pero que al microscopio se visualizarían sin dificultades las partículas amarillas.
Es aquí donde entran los estabilizadores, compuestos que se encargan de evitar la coalescencia de las partículas dispersas, y alargan todavía más la homogeneidad de la emulsión. Es decir, no se “cortará” en dos fases.
Aspectos moleculares de la emulsión
Molecularmente, el proceso de emulsión es bastante dinámico y existen varias teorías que intentan explicar la acción del emulsificante. No obstante, todas ellas comparten algo en común, y es el hecho de que el emulsificante debe tratarse de una o más moléculas anfifílicas (o anfipáticas), o sea, aquellas que poseen tanto carácter apolar como polar.
La molécula anfifílica puede compararse con una chupeta: la cabeza es polar, hidrofílica; mientras que la varilla o cola es apolar, hidrofóbica. Dos líquidos son inmiscibles porque en esencia su diferencia de polaridad es muy grande. El emulsificante interactúa con ambos líquidos al mismo tiempo.
Su cabeza polar se orienta en dirección del líquido polar. Por otra parte, la cola apolar busca interaccionar con el líquido apolar. Dependiendo del líquido o fase predominante, las moléculas anfifílicas tienden a formar micelas, digamos, cápsulas, dentro de las cuales se encierran moléculas del líquido dispersado.
Por ejemplo, los glóbulos amarillos vendrían a estar rodeados de las moléculas anfifílicas del emulsificante, cuya parte externa interacciona con la fase o líquido continuo (de mayor proporción, el azul), y repele asimismo a los otros glóbulos. No obstante, las micelas se mueven, lo que provocará que tarde o temprano terminarán separándose y dando lugar a la aparición de la fase amarilla.
Aplicaciones de los emulsificantes

Sin los emulsificantes no sería posible la elaboración de las emulsiones, las cuales son de enorme importancia en la industria alimenticia y farmacéutica. Si bien la formulación de tales productos incorpora también agentes espesantes y estabilizadores, los emulsificantes ayudan a que las mezclas desarrollen cuerpo y textura.
Las viscosidades de las emulsiones obtenidas pueden ser mayores que las de los líquidos inmiscibles originales. La mayonesa demuestra este punto. Pero la viscosidad final también puede ser menor, siendo más suave la mezcla resultante. Así pues, los emulsificantes son claves en la consistencia de los alimentos y, por ende, en sus sabores.
Productos que requieren emulsificantes
Entre algunos de los productos alimenticios que requieren de emulsificantes están:
- La leche, siendo una emulsión o/w, capaz de actuar a su vez como un emulsionante gracias a su contenido proteico.
- Mantequilla y margarina, ambas emulsiones w/o.
- Pan, para su endurecimiento y frescura.
- Aderezos.
- Chocolates, donde modifican su viscosidad durante su elaboración industrial en barras o moldes.
- Helados, pues las proteínas de la leche estabilizan la combinación de grasas y agua, además de que la adición de emulsificantes extras las reagrupa (desestabilizan parcialmente) para que la mezcla pueda incorporar aire.
- Galletas.
- Cremas faciales.
- Lápiz labial.
- Ungüentos.
- Quesos.
- Tortas.
Ejemplos de emulsificantes
Se hizo mención de que las moléculas de los emulsionantes deben ser en principio anfifílicas. Los surfactantes, por otro lado, poseen también esta característica. Sin embargo, esto no implica que una molécula anfifílica sea un surfactante (como sucede con las proteínas).
Por lo tanto, los surfactantes son una buena opción al momento de escoger un emulsificante; aunque haya sales que desempeñan la misma función. La viabilidad de utilizarse cualquiera de ellos dependerá de la formulación y las propiedades químicas del producto.
Asimismo, no todos los emulsionantes son anfifílicos, pues puede ser que interaccionen con los componentes de una mezcla (proteínas, grasas, azúcares, etc.), logrando así la homogeneización del conjunto. Por eso, y para finalizar, se enlistarán algunos ejemplos de emulsionantes:
- Ésteres de ácidos grasos.
- Monoglicéridos.
- Diglicéridos.
- Lecitina (encontrada en la yema de huevo).
- Goma arábiga.
- Pectina.
- Almidón oxidado.
- Gelatina.
- Polietilenglicol.
- Maltitol.
- Citrato de calcio.
- Lactatos de sodio y potasio.
- Alginato de sodio.
- Agar.
- Goma karaya.
- Celulosas.
- Alcoholes etoxilados.
- Estearoil lactilato de sodio y calcio.
- Polisorbatos 20, 40, 60 y 80 (food grade).
- Lactitol.
Como puede apreciarse, son muchos los emulsificantes disponibles, y cada uno tiene una funcionalidad, ya sea para alimentos, cremas, jarabes, detergentes, lociones, etc.
Referencias
- Whitten, Davis, Peck & Stanley. Química (8va ed.). CENGAGE Learning.
- Emulsion. Recuperado de en.wikipedia.org.
- Emulsifier. Recuperado de britannica.com.
- Emulsifiers. Recuperado de specialtyfoodingredients.eu.
- Emulsifiers in ice cream. Recuperado de icecreamscience.com.