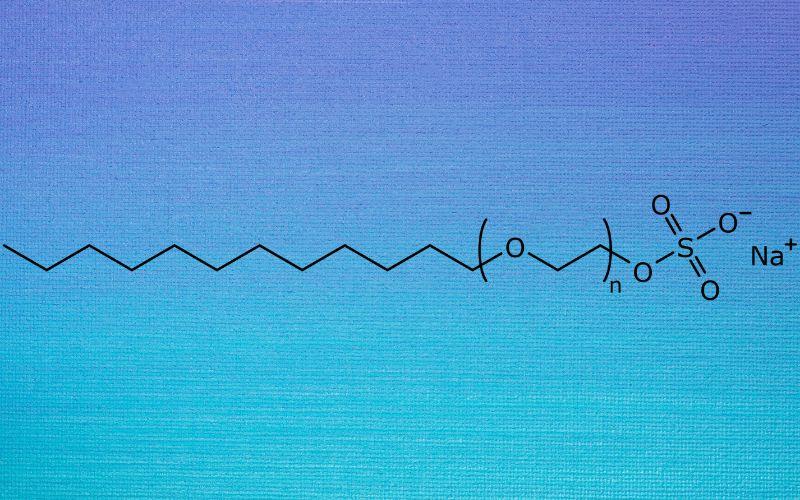
¿Qué es el lauril sulfato de sodio?
El lauril sulfato de sodio es una sal orgánica formada por la unión del ion sodio Na+ y el ion lauril sulfato n-C11H23CH2OSO3–. Su fórmula química es CH3-(CH2)10-CH2-O-SO3–Na+. Se le conoce también como dodecil sulfato de sodio porque la cadena hidrocarbonada posee 12 átomos de carbono. Es un componente de los productos para hacer baños de burbujas.
Es un compuesto que actúa sobre la superficie que está entre dos fases, por ejemplo, entre líquido y gas, o entre agua y aceite. Esto hace que pueda actuar como detergente, pues se une a las gotitas de aceite o grasa, o pequeñas porciones de sucio, y las separa del agua en forma de una partícula flotante, que luego es fácilmente enjuagada.
También sirve como dispersante de ingredientes en productos alimenticios, mejorando su textura, y se emplea en champús para mascotas porque repele pulgas y garrapatas. Además, actúa como humectante en medicamentos para animales y se utiliza en agricultura, en pinturas, en plásticos y en investigaciones de química y biología.
Hay estudios que indican que rompe las membranas que envuelven algunos virus y bacterias, trabajando en algunos casos como agente antimicrobiano.
Estructura del lauril sulfato de sodio
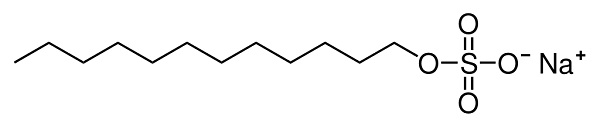
Es un compuesto orgánico iónico formado por un catión sodio Na+ y un anión dodecil sulfato n-C11H23CH2OSO3–. Se coloca la n en su fórmula compacta para indicar que es una cadena lineal (no ramificada).
El anión dodecilsulfato posee una cadena hidrocarbonada lineal de 12 átomos de carbono unida a un sulfato -OSO3– por el oxígeno, por lo que tiene una sola carga negativa.
Nomenclatura del lauril sulfato de sodio
- Lauril sulfato de sodio.
- Dodecil sulfato de sodio.
- SLS (siglas del inglés Sodium Lauryl Sulphate).
Propiedades del lauril sulfato de sodio
- Estado físico. Sólido blanco o color crema en forma de cristales, escamas o polvo.
- Peso molecular. 288,38 g/mol.
- Punto de fusión. 205,5 °C.
- Peso específico. Mayor que 1,1 a 20 °C.
- Solubilidad. Es moderadamente soluble en agua: 15 g/100 mL a 20 °C.
- Otras propiedades. Es un surfactante o tensioactivo iónico, es decir, ejerce un efecto sobre la superficie que separa dos fases inmiscibles. Es un surfactante aniónico porque la parte que realiza la acción de tensioactivo es el anión lauril-sulfato C11H23CH2OSO3– y no el sodio Na+. Es un compuesto anfifílico, esto significa que una parte de la molécula tiene afinidad por el agua (es hidrofílica) y otra posee similitud o atracción por aceites y grasas y repele el agua (es hidrofóbica). La porción hidrofílica es donde se encuentra la carga negativa del anión, es decir, los oxígenos del grupo OSO3– de la molécula. La fracción hidrofóbica es la cadena hidrocarbonada o C11H23CH2–. Es fácilmente biodegradable y solo débilmente tóxico.
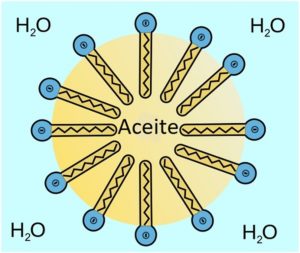
- Mecanismo de acción como surfactante. La acción que realiza como tensioactivo es modificar o cambiar la tensión superficial, especialmente en soluciones acuosas. Esto le permite emulsionar grasas y aceites. El mecanismo de acción consiste en que se ubica en la superficie de contacto entre ambos líquidos, donde disminuye la tensión superficial. Para hacer esto, la cabeza o parte hidrofílica OSO3– se coloca en contacto con el agua y la cola o porción hidrofóbica C11H23CH2– se sitúa dentro del aceite o grasa.
Obtención del lauril sulfato de sodio
Se deriva del aceite de coco o de palma, entre otros. De estos, se obtiene el ácido laurílico, que es un ácido graso. Este se somete a un proceso de reducción (lo contrario de oxidación) para obtener el alcohol laurílico.
Para obtener el lauril sulfato de sodio se hace reaccionar el alcohol laurílico con ácido sulfúrico H2SO4 y se obtiene sulfato ácido de laurilo. Luego este último, por ser un ácido, se neutraliza con hidróxido de sodio NaOH.
n-C11H23CH2OH (alcohol laurílico) + H2SO4 → n-C11H23CH2OSO3H (sulfato ácido de laurilo).
n-C11H23CH2OSO3H + NaOH → n-C11H23CH2OSO3–Na+ (lauril sulfato de sodio).
Usos del lauril sulfato de sodio
- En limpieza. Es uno de los principales componentes de los líquidos para lavar platos. También es esencial en los dentífricos o pasta de dientes, pues actúa en la formación de espuma, es humectante y dispersante en estos y muchos otros productos de limpieza.
- En cosméticos. Se usa en lociones, champús, geles, baños de burbujas, bases de ungüentos, cremas y decolorantes de cabello, entre otros artículos.
- En la industria alimenticia. Se emplea con mucha frecuencia en la industria alimenticia, por ejemplo, en pastas y cremas para permitir una buena dispersión de los ingredientes, y en jugos de frutas, entre otros alimentos. Mejora la textura de ciertos alimentos horneados. Aumenta la estabilidad y alarga la vida del alimento en el estante.
- En aplicaciones veterinarias. Actúa como repelente de pulgas y garrapatas, por lo que se usa en champús para perros y gatos. Sirve también como agente humectante en algunos antibióticos y antimicrobiales de administración oral o tópica (uso externo) para animales. Tiene aplicación en medicamentos antihelmínticos.
- En productos farmacéuticos. Tiene amplia aplicación en la industria farmacéutica por sus propiedades surfactantes. Funciona como emulsionante, dispersante, humectante, entre muchas otras acciones. Además, posee la característica de actuar como vehículo de transporte en diversos medicamentos, por ejemplo, en aquellos fármacos que se desea penetren a través de la mucosa bucal.
- En medicina. Algunas fuentes reportan que el lauril sulfato de sodio posee acción antiviral contra algunos virus y bacterias. Por ejemplo, actúa contra el virus de HIV, contra el herpes simple tipo 2 y contra el virus de papiloma humano. Además, ejerce acción microbicida contra la clamidia. Su potente actividad desnaturalizante de proteínas inhibe la actividad infecciosa de los virus solubilizando el envoltorio viral mediante su desorganización. Su actividad microbicida funciona contra algunos tipos de virus envueltos y no-envueltos. El lauril sulfato de sodio se ha utilizado en la preparación de muestras de sangre para el conteo de glóbulos rojos.
- En diversas aplicaciones
- En la industria metalúrgica: en la electrodeposición de metales, especialmente de cinc y níquel.
- En agricultura: como microbicida, fungicida, bactericida y como emulsionante en insecticidas.
- En pinturas y agentes de remoción: como emulsionante y penetrante en lacas, barnices y removedores de pintura.
- En la industria de plásticos y gomas: como aditivo de plásticos y látex. Mejora la fuerza de tensión de ciertos polímeros. En la polimerización por emulsión.
- En combustibles para cohetes: como agente antiespumante.
- En laboratorios de investigación química y biológica. Sirve como herramienta de investigación en bioquímica. Es muy utilizado por su capacidad de desbaratar o desordenar membranas de microorganismos. Sus habilidades para desorganizar la estructura de los tejidos y de inhibir la actividad de ciertas enzimas hacen que los bioquímicos lo empleen como componente clave de muchos de los reactivos usados para purificar los ácidos del núcleo de las células, como ARN y ADN, o ácidos nucleicos. Las membranas de los microorganismos están formadas principalmente por proteínas y lípidos (grasas). Por ser un detergente con carga negativa, el lauril sulfato de sodio se adsorbe o adhiere fuertemente sobre la estructura de las proteínas, neutralizando todas las cargas positivas. Forma así asociaciones hidrofóbicas internas, confiriendo a cada proteína la misma carga negativa neta global. Esta es la razón por la que se usa en la separación electroforética de proteínas y lípidos, pues al poseer carga negativa, las proteínas se movilizan de forma diferente frente a un campo eléctrico. También se usa para determinar la fuerza relativa del gluten en muestras de harina o trigo molido. El gluten es un tipo de proteína presente en el trigo. Las partículas de gluten se hidratan gracias al lauril sulfato de sodio y sedimentan. A mayor volumen de sedimento, mayor es la fuerza de las proteínas de gluten en la muestra. Se emplea también en la caracterización de compuestos de amonio cuaternario NH4+. Además, se usa como compuesto surfactante de referencia en pruebas de toxicidad para especies acuáticas y mamíferos.
- En la industria del petróleo. El dodecil sulfato de sodio se utiliza como antiemulsionante en la técnica de extracción del petróleo por fractura hidráulica (del inglés hydraulic fracking) de formaciones rocosas ricas en este. Sirve para evitar la formación de emulsiones en el fluido de fractura.
Referencias
- Sodium dodecyl sulfate. Recuperado de pubchem.ncbi.nlm.nih.gov.
- Farrell Jr., R.E. Resilient Ribonucleases. Sodium dodecyl sulfate. In RNA Methodologies (Fourth Edition). Recuperado de sciencedirect.com.
- Kirk-Othmer. Encyclopedia of Chemical Technology. Fourth Edition. John Wiley & Sons.
- Wheat and Flour Testing. In Wheat Flour. Recuperado de sciencedirect.com.
- Franz-Montan, M. Nanostructured systems for transbuccal drug delivery. In Nanostructures for Oral Medicine. Recuperado de sciencedirect.