¿Qué es la LDH?
La LDH, lactato deshidrogenasa, ácido láctico deshidrogenasa o lactato deshidrogenasa NAD-dependiente, es una enzima perteneciente al grupo de las oxidorreductasas que está prácticamente en todos los tejidos animales, vegetales y en muchos microorganismos, como bacterias, levaduras y arqueas.
Las enzimas de este tipo se denotan con el número EC 1.1.1.27 del comité de nomenclatura enzimática, y se encargan de la reacción que convierte el lactato a piruvato (por oxidación) y viceversa (por reducción), oxidando o reduciendo dinucleótidos de nicotinamida adenina (NAD+ y NADH) en el proceso conocido como fermentación láctica.
A diferencia de la fermentación alcohólica, que ocurre solo en algunos microorganismos como las levaduras y que emplea el piruvato glucolítico para la producción de etanol, la fermentación láctica sucede en muchos organismos y tejidos del cuerpo de diferentes seres vivos.
Esta importante enzima para el metabolismo celular fue cristalizada a partir de músculo esquelético de ratas en los años 40 y, hasta la fecha, las mejor caracterizadas son la del músculo esquelético y del tejido cardíaco en mamíferos.
En los animales “superiores”, la enzima emplea el isómero L del lactato (L-lactato) para la producción de piruvato, pero algunos animales “inferiores” y bacterias producen D-lactato a partir del piruvato obtenido por glucólisis.
La lactato deshidrogenasa suele expresarse mayoritariamente en tejidos o células bajo condiciones anaeróbicas (poco oxígeno) que, en los seres humanos, por ejemplo, pueden caracterizar condiciones patológicas como cáncer, afecciones hepáticas o cardíacas.
Sin embargo, la conversión del piruvato en lactato es propia de los músculos durante el ejercicio y la córnea del ojo, que es pobremente oxigenada.
Funciones de la LDH
- Glicólisis. Está involucrada en la glicólisis, proceso metabólico en el que la glucosa se descompone para producir energía en forma de adenosina trifosfato (ATP). En la glicólisis, la LDH cataliza la conversión del ácido pirúvico en lactato bajo ciertas condiciones, regenerando el cofactor necesario para la continuación de la glicólisis.
- Regulación del equilibrio de los niveles de lactato y piruvato. Resulta fundamental para mantener el equilibrio entre el lactato y el piruvato en el organismo. Esta regulación es importante para garantizar que las células obtengan la energía necesaria y evitar la acumulación tóxica de lactato en el tejido.
- Regeneración de cofactores. Regenera el cofactor nicotinamida adenina dinucleótido (NAD+) durante la conversión de piruvato en lactato. El NAD+ es esencial para mantener la glicólisis funcionando, ya que actúa como un aceptor de electrones en muchas reacciones metabólicas.
- Metabolismo anaeróbico. Resulta importante en el metabolismo anaeróbico, donde se produce energía en ausencia de oxígeno. En estas condiciones, la glicólisis anaeróbica es esencial para proporcionar rápidamente energía a las células, como durante actividades físicas intensas.
- Detoxificación del lactato. Convierte el lactato en piruvato en un proceso conocido como vía de la lactato deshidrogenasa inversa. Esto es importante para eliminar el lactato acumulado en los tejidos y prevenir la acidosis láctica, que puede ser perjudicial para el organismo.
- Marcador de lesión celular. En algunas situaciones, como lesiones o enfermedades que afectan las células, la LDH puede liberarse al torrente sanguíneo. Por lo tanto, se utiliza a menudo como un marcador de daño celular en pruebas sanguíneas para diagnosticar afecciones médicas.
- Participación en la síntesis de ácido láctico. En algunos tejidos, también está involucrada en la síntesis de ácido láctico, que se utiliza en ciertas reacciones bioquímicas.
Características de la LDH
- Ubicuidad. Se encuentra en una amplia variedad de tejidos y tipos celulares en el cuerpo humano, incluyendo el músculo esquelético, el corazón, el hígado, los riñones, los glóbulos rojos y otros tejidos.
- Catalización de reacciones. Cataliza la conversión del ácido láctico a ácido pirúvico y viceversa. Esta reacción es reversible y fundamental en el metabolismo anaeróbico y la glicólisis, donde se produce energía en forma de adenosina trifosfato (ATP).
- Cofactor NAD+. Requiere la presencia de un cofactor, el nicotinamida adenina dinucleótido (NAD+), para llevar a cabo su función. El NAD+ actúa como un aceptor de electrones en la reacción de conversión de lactato a piruvato.
- Formas isoenzimáticas. Se presenta en forma de isoenzimas, que son variantes de la enzima con diferente distribución de tejidos y propiedades cinéticas. En los seres humanos, existen cinco isoenzimas principales, denominadas LDH-1, LDH-2, LDH-3, LDH-4 y LDH-5. Estas isoenzimas se hallan en diferentes proporciones en diversos tejidos.
- Medición en pruebas sanguíneas. Los niveles de LDH en la sangre pueden medirse en pruebas clínicas y se utilizan como marcadores de daño celular o lesión tisular en diversas afecciones médicas.
- Función en el metabolismo anaeróbico. Es esencial en situaciones de ejercicio intenso o falta de oxígeno para producir energía.
- Regulación de la homeostasis del lactato. Contribuye a mantener un equilibrio apropiado entre el ácido láctico y el ácido pirúvico en el organismo, evitando la acumulación tóxica de lactato.
Determinación de la LDH
- Por espectrofotometría. La actividad lactato deshidrogenasa de origen animal es determinada espectrofotométricamente in vitro mediante mediciones de cambio de coloración gracias al proceso de oxidorreducción que sucede durante la reacción de conversión de piruvato a lactato. Las mediciones se realizan a 340 nm con un espectrofotómetro y se determina la tasa de disminución de densidad óptica debida a la oxidación o “desaparición” del NADH, que es convertido a NAD+. La medición enzimática debe realizarse en óptimas condiciones de pH y concentración de sustratos para la enzima, de manera que no se corra el riesgo de subestimar la cantidad presente en las muestras por déficit de sustratos o por condiciones extremas de acidez o basicidad. La reacción determinada es como sigue:
Piruvato + NADH + H+ → Lactato + NAD+
- Por inmunohistoquímica. Otro método, quizá algo más moderno, tiene que ver con el uso de herramientas inmunológicas, es decir, con el uso de anticuerpos. Estos métodos aprovechan la afinidad entre la unión de un antígeno con un anticuerpo generado específicamente contra este y son muy útiles para la determinación rápida de la presencia o ausencia de enzimas como la LDH en un tejido particular. Dependiendo de la finalidad, los anticuerpos empleados deberán ser específicos para la detección de alguna de las isoenzimas o para cualquier proteína con actividad lactato deshidrogenasa.
¿Para qué determinar lactato deshidrogenasa?
La determinación de esta enzima se realiza con diferentes propósitos, pero principalmente para el diagnóstico clínico de algunas condiciones, entre las que destacan el infarto de miocardio y el cáncer.
A nivel celular, la liberación de la lactato deshidrogenasa ha sido considerada como uno de los parámetros para determinar la ocurrencia de procesos necróticos o apoptóticos, puesto que la membrana plasmática se hace permeable.
Los productos de la reacción que cataliza también pueden ser determinados en un tejido para determinar si en el mismo predomina un metabolismo anaeróbico por algún motivo particular.
Reacción de la LDH
La enzima lactato deshidrogenasa cataliza la conversión de lactato en piruvato de forma NAD+ dependiente, o viceversa, lo que se da gracias a la transferencia de un ion hidruro (H–) desde el piruvato al lactato, o desde el NADH hacia el piruvato oxidado.
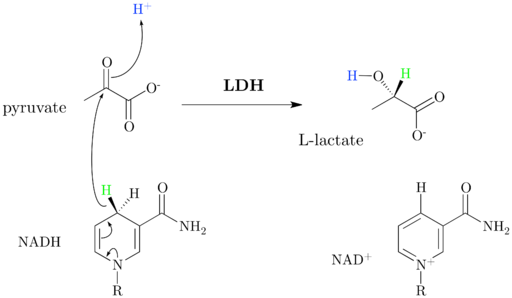
El NAD+ posee una unidad de ADP y otro grupo nucleotídico derivado del ácido nicotínico, denominado niacina o vitamina B3, y esta coenzima participa en múltiples reacciones de gran importancia biológica.
Es importante resaltar que el equilibrio en dicha reacción está desplazado hacia el lado correspondiente al lactato y se ha demostrado que la enzima también es capaz de oxidar otros ácidos (S)-2-hidroximonocarboxílicos y emplear, aunque menos eficientemente, NADP+ como sustrato.
Dependiendo de la región corporal que se considere y, al mismo tiempo, de sus características metabólicas en relación con la presencia o ausencia de oxígeno, los tejidos producen cantidades diferentes de lactato, el producto de la reacción catalizada por la LDH.
Si se considera, por ejemplo, un glóbulo rojo que carece de mitocondrias que puedan metabolizar el piruvato producido durante la glucólisis a CO2 y agua, entonces podría decirse que estas son las principales células productoras de lactato en el cuerpo humano, puesto que todo el piruvato es convertido a lactato por acción de la lactato deshidrogenasa.
En cambio, si se consideran las células del hígado y las del músculo esquelético, estas son responsables de la producción de una mínima cantidad de lactato, en vista de que este es metabolizado rápidamente.
Valores normales de la LDH
La concentración de lactato deshidrogenasa en el suero sanguíneo es producto de la expresión de varias isoenzimas en el hígado, el corazón, el músculo esquelético, los eritrocitos y tumores, entre otros.
En el suero sanguíneo, los rangos normales de actividad de la lactato deshidrogenasa están entre las 260 y las 850 U/ml (unidades por mililitro), con un valor promedio de 470±130 U/ml. Entretanto, los hemolizados sanguíneos tienen una actividad LDH que varía entre 16.000 y 67.000 U/ml, lo que equivale a un promedio de 34.000±12.000 U/ml.
¿Qué significa tener LDH alta?
La cuantificación de la concentración de lactato deshidrogenasa en el suero sanguíneo tiene un importante valor en el diagnóstico de algunas enfermedades cardíacas, hepáticas, sanguíneas y cánceres.
Elevadas cifras de actividad LDH se han encontrado en pacientes con infartos al miocardio (tanto experimentales como clínicos), así como en pacientes cancerosos, concretamente en mujeres con cáncer endometrial, de ovarios, de seno y de útero.
Dependiendo de la isoenzima particular que se halle en “exceso” o en alta concentración, la cuantificación de las isoenzimas de la lactato deshidrogenasa la emplean muchos médicos tratantes para determinar lesiones en los tejidos (graves o crónicas).
Referencias
- Chung, F., Tsujubo, H., Bhattacharyya, U., Sharief, F., & Li, S. Genomic organization of human lactate dehydrogenase-A gene. Biochemical Journal.
- De Becker, D. Lactic acidosis. Intensive Care MEd.
- Fox, S. I. Human Physiology (9th ed.). McGraw-Hill Press.
- Rawn, J. D. Biochemistry. Neil Patterson Publishers.