El nitrato de zinc es un compuesto inorgánico formado por los elementos zinc (Zn), nitrógeno (N) y oxígeno (O). El estado de oxidación del cinc es de +2, el del nitrógeno es +5, y el del oxígeno es -2.
Su fórmula química es Zn(NO3)2. Es un sólido incoloro cristalino que tiende a absorber agua del medio ambiente. Se puede obtener tratando el metal cinc con ácido nítrico diluido. Es un compuesto fuertemente oxidante.

Sirve como acelerador de reacciones de química orgánica y permite obtener polímeros compuestos con propiedades de conducción de la electricidad. Se utiliza para formar capas de materiales útiles en electrónica.
Forma parte de algunos fertilizantes líquidos y de ciertos herbicidas de liberación lenta. Ayuda en la preparación de óxidos complejos mejorando su densidad y conductividad eléctrica.
Ha sido probado con éxito en la obtención de estructuras que sirven de base para regeneración y crecimiento de tejido óseo, mejorando este proceso y resultando efectivo como antibacteriano.
Aunque no es combustible, puede acelerar el quemado de sustancias que sí lo son, como carbón o materiales orgánicos. Es irritante de piel, ojos y mucosas, y es muy tóxico para la vida acuática.
[toc]
Estructura
El nitrato de cinc es un compuesto iónico. Posee un catión bivalente (Zn2+) y dos aniones monovalentes (NO3–). El anión nitrato es un ion poliatómico formado por un átomo de nitrógeno en su estado de oxidación +5 unido de forma covalente a tres átomos de oxígeno con valencia de -2.
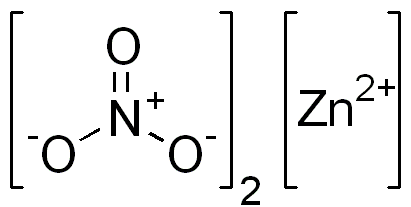
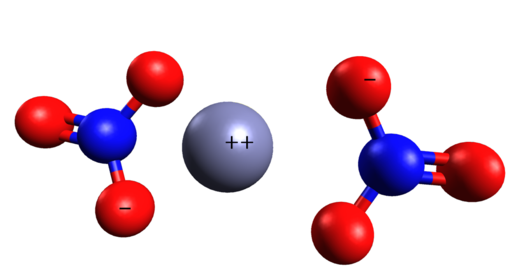
La imagen a continuación muestra la estructura espacial de este compuesto. La esfera central gris es el cinc, las esferas azules son de nitrógeno y las esferas rojas representan oxígeno.
Nomenclatura
- Nitrato de cinc
- Dinitrato de cinc
Propiedades
Estado físico
Sólido incoloro o blanco cristalino.
Peso molecular
189,40 g/mol
Punto de fusión
Aproximadamente 110 ºC.
Punto de ebullición
Aproximadamente 125 ºC.
Densidad
2,065 g/cm3
Solubilidad
Soluble en agua: 120 g/100 g H2O a 25 °C. Soluble en alcohol.
pH
Sus soluciones acuosas son ácidas. Una solución al 5% posee un pH de aproximadamente 5.
Propiedades químicas
Por ser un nitrato este compuesto es un oxidante fuerte. Reacciona violentamente con carbón, cobre, sulfuros metálicos, materia orgánica, fósforo y azufre. Si se rocía sobre carbón caliente explota.
Por otra parte es higroscópico y absorbe agua del ambiente. Si se somete a calentamiento forma óxido de cinc, dióxido de nitrógeno y oxígeno:
2 Zn(NO3)2 + calor → 2 ZnO + 4 NO2↑ + O2↑
En soluciones alcalinas, como las de NaOH, el cinc de este compuesto forma su hidróxido y otras especies complejas:
Zn(NO3)2 + 2 OH– → Zn(OH)2 + 2 NO3–
Zn(OH)2 + 2 OH– → [Zn(OH)4]2-
Obtención
Se puede obtener tratando cinc u óxido de cinc con ácido nítrico diluido. Se forma gas hidrógeno en esta reacción.
Zn + 2 HNO3 → Zn(NO3)2 + H2↑
Usos
En catálisis de reacciones
Se usa como catalizador en la obtención de otros compuestos químicos como resinas y polímeros. Es un catalizador ácido.

Otro caso de aceleración de reacciones es el sistema catalítico de Zn(NO3)2/VOC2O4, que permite la oxidación de α-hidroxiésteres a α-cetoésteres con un 99% de conversión incluso a presión y temperatura ambientales.
En polímeros compuestos
Se han desarrollado películas de polimetilmetacrilato y Zn(NO3)2 con propiedades de conductividad eléctrica que los hacen candidatos apropiados para ser usados en supercondensadores y computadores de alta velocidad.
En cementos de oxisales
Con soluciones acuosas de nitrato de cinc y polvo de óxido de cinc se obtienen materiales que pertenecen a la clase de cementos generados por una reacción ácido-base.
Estos presentan una razonable resistencia a disolverse en ácidos diluidos y álcalis, desarrollando una resistencia a la compresión comparable a la de otros cementos como los de oxicloruros de cinc.
Dicha propiedad aumenta al incrementarse la relación ZnO/Zn(NO3)2, y al subir la concentración de Zn(NO3)2 en la solución. Los cementos obtenidos son completamente amorfos, es decir, no poseen cristales.

En recubrimientos y nanomateriales de óxido de cinc
El Zn(NO3)2 se emplea para la deposición electrolítica de capas muy delgadas de óxido de cinc (ZnO) sobre diversos sustratos. También se preparan nanoestructuras de este óxido sobre las superficies.

El ZnO es un material de gran interés debido a la multitud de aplicaciones en el campo de la optoelectrónica, además posee propiedades de semiconductor y se usa en sensores y transductores.
En herbicidas
El nitrato de cinc se ha utilizado junto con algunos compuestos orgánicos para disminuir la velocidad de liberación de ciertos herbicidas en agua. La liberación lenta de estos productos permite que estén disponibles por más tiempo y se requieran menos aplicaciones.
En la manufactura de ánodos
Estimula el proceso de sinterización y mejora la densidad de ciertos óxidos que sirven para fabricar ánodos para celdas de combustible. La sinterización es la obtención de un material sólido mediante el calentamiento y compresión de un polvo sin llegar a su fusión.
Los materiales en los que se han realizado las pruebas son óxidos complejos de estroncio, iridio, hierro y titanio. La presencia de cinc aumenta significativamente la conductividad eléctrica de estos.
Otras aplicaciones
Se utiliza en la obtención de fármacos. Actúa como mordiente en la aplicación de tintas y colorantes. Sirve como coagulante de látex. Es una fuente de cinc y nitrógeno en fertilizantes líquidos.
Potencial uso en ingeniería de tejidos óseos
Este compuesto se ha usado como aditivo en la elaboración de armaduras o entramados para la regeneración de fibras óseas, pues permite mejorar la resistencia mecánica de estas estructuras.
Se ha observado que el andamio que contiene cinc no es tóxico para las células osteoprogenitoras, soporta la actividad de los osteoblastos que son las células que fabrican hueso y mejora su adhesión y proliferación.
Favorece la formación de apatita que es el mineral que forma los huesos y además ejerce un efecto antibacterial.
Riesgos
Es un material con potencial riesgo de incendio y explosión.
No es combustible pero acelera el quemado de materiales combustibles. Si una gran cantidad de este compuesto está involucrada en un incendio o si el material combustible está finamente dividido, puede ocurrir una explosión.
Al ser sometido a fuerte calor se producen gases tóxicos de óxidos de nitrógeno. Y si la exposición se realiza de forma prolongada puede explotar.
Es irritante para la piel, puede producir daños serios en los ojos, irritación en tracto respiratorio, resulta tóxico por ingestión y causa daño en el tracto digestivo.
Muy tóxico para la vida acuática con efectos que perduran.
Referencias
- Ju, Y. et al. (2019). Novel Effect of Zinc Nitrate/Vanadyl Oxalate for Selective Catalytic Oxidation of ALFA-Hydroxy Esters to ALFA-Keto Esters with Molecular Oxygen: An In Situ ATR-IR Study. Molecules 2019, 24, 1281. Recuperado de mdpi.com.
- Mohd S., S.N. et al. (2020). Controlled release formulation of zinc hydroxide nitrate intercalated with sodium dodecylsulphate and bispyribac anions: A novel herbicide nanocomposite for paddy cultivation. Arabian Journal of Chemistry 13, 4513-4527 (2020). Recuperado de sciencedirect.
- Mani, M.P. et al. (2019). Enriched Mechanical Strength and Bone Mineralisation of Electrospun Biomimetic Scaffold Laden with Ylang Ylang Oil and Zinc Nitrate for Bone Tissue Engineering. Polymers 2019, 11, 1323. Recuperado de mdpi.com.
- Kim, K.I. et al. (2018). Effects of zinc nitrate as a sintering aid on the electrochemical characteristics of Sr0,92Y0,08TiO3-DELTA and Sr0,92Y0,08Ti0,6Fe0,4O3-DELTA Ceramics International, 44(4): 4262-4270 (2018). Recuperado de sciencedirect.com.
- Prasad, B.E. et al. (2012). Electrodeposition of ZnO coating from aqueous Zn(NO3)2 baths: effect of Zn concentration, deposition temperature, and time on orientation. J Solid State Electrochem 16, 3715-3722 (2012). Recuperado de link.springer.com.
- Bahadur, H. and Srivastava, A.K. (2007). Morphologies of Sol-Gel Derived Thin Films of ZnO Using Different Precursor Materials and their Nanostructures. Nanoscale Res Lett (2007) 2: 469-475. Recuperado de link.springer.com.
- Nicholson, J.W. and Tibaldi, J.P. (1992). Formation and properties of cement prepared from zinc oxide and aqueous solutions of zinc nitrate. J Mater Sci 27, 2420-2422 (1992). Recuperado de link.springer.com.
- Lide, D.R. (editor) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Press.
- Maji, P. et al. (2015). Effect of Zn(NO3)2 filler on the dielectric permittivity and electrical modulus of PMMA. Bull Mater Sci 38, 417-424 (2015). Recuperado de link.springer.com.
- U.S. National Library of Medicine. (2019). Zinc nitrate. Recuperado de pubchem.ncbi.nlm.nih.gov.
- Byju’s. (2020). Zinc nitrate – Zn(NO3)2. Recuperado de byjus.com.
- American Elements. Zinc nitrate. Recuperado de americanelements.com.
- Cotton, F. Albert and Wilkinson, Geoffrey. (1980). Advanced Inorganic Chemistry. Fourth Edition. John Wiley & Sons.