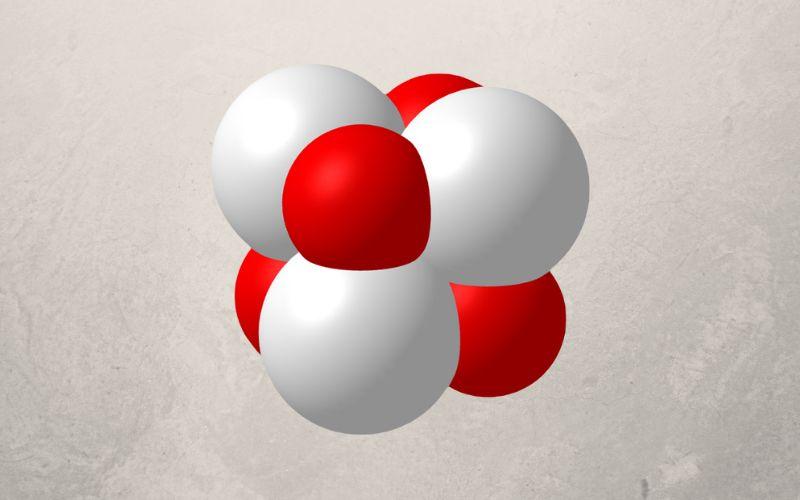
¿Qué es el óxido de bario?
El óxido de bario es un sólido inorgánico formado por un átomo de bario (Ba) y un átomo de oxígeno (O). Su fórmula química es BaO. Es un sólido cristalino blanco higroscópico, es decir, absorbe humedad del aire, pero al hacerlo reacciona con esta.
La rápida reacción del óxido de bario con el agua hace que se use en laboratorios de análisis químico para desecar, o sea, eliminar agua de solventes orgánicos (compuestos líquidos que sirven para disolver otras sustancias).
El BaO se comporta como una base fuerte, por lo tanto, reacciona con muchos tipos de ácidos. Por ejemplo, reacciona fácilmente con el dióxido de carbono CO₂ del aire para formar carbonato de bario BaCO3.
Sirve en la fabricación de los polímeros para cables de electricidad y como ingrediente para resinas para sellar orificios de dientes después de curarlos.
El óxido de bario también se emplea en la industria de la cerámica, tanto para recubrirla con vidriado como para fabricarla. Además, se utiliza en mezclas de cemento para incrementar la resistencia a la compresión del producto final.
Estructura del óxido de bario
El óxido de bario está formado por un catión Ba2+ y un anión oxígeno O2–.
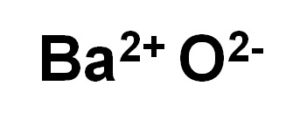
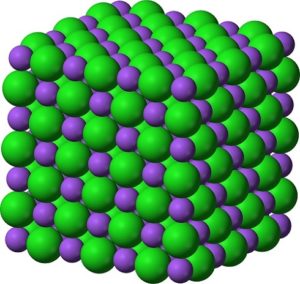
En sus cristales, el BaO forma redes iónicas cúbicas del tipo cloruro de sodio.
La configuración electrónica del ion bario es: [Xe] 6s0, pues ha perdido los dos electrones de la capa 6s. Esta configuración es muy estable.
Nomenclatura del óxido de bario
- Óxido de bario.
- Monóxido de bario.
Propiedades físicas del óxido de bario
- Estado físico. Sólido cristalino color blanco amarillento.
- Peso molecular. 153,33 g/mol.
- Punto de fusión. 1923 °C.
- Punto de ebullición. Aproximadamente 2000 °C.
- Densidad. 5,72 g/cm3
- Solubilidad. Poco soluble en agua: 3,8 g/100 mL a 20 °C.
Propiedades químicas del óxido de bario
El BaO reacciona rápidamente con el agua desprendiendo calor y formando una solución corrosiva de hidróxido de bario, Ba(OH)2, que es el hidróxido más soluble entre los hidróxidos de metales alcalinotérreos.
BaO + H₂O → Ba(OH)2
El BaO es una base fuerte. Reacciona de forma exotérmica (es decir, con desprendimiento de calor) con todo tipo de ácidos.
Con CO₂ el BaO reacciona para formar carbonato de bario BaCO3.
BaO + CO₂ → BaCO3
El BaO es higroscópico, por lo que si se deja expuesto al ambiente se une poco a poco a la humedad del aire, formando Ba(OH)2 el cual se combina con el dióxido de carbono CO₂ del aire para dar carbonato de bario BaCO3.
Cuando se calienta el monóxido de bario BaO en presencia de aire, se combina con el oxígeno formando peróxido de bario BaO2. La reacción es reversible.
2 BaO + O2 ⇔ 2 BaO2
En presencia de agua puede reaccionar con aluminio, Al, o con cinc, Zn, formando los óxidos o hidróxidos de dichos metales y generando gas hidrógeno H2.
Puede iniciar la polimerización de compuestos orgánicos susceptibles de polimerizar, como los epóxidos.
Riesgos del óxido de bario
Puede ser tóxico por ingestión. No debe entrar en contacto con la piel. Es irritante de los ojos, piel y tracto respiratorio. Puede ser dañino para el sistema nervioso. Es capaz de causar bajos niveles de potasio, lo que resulta en desórdenes cardíacos y musculares.
Obtención del óxido de bario
El BaO se puede obtener calentando el carbonato de bario BaCO3 con carbón. Se forma el BaO y se desprende gas de monóxido de carbono CO.
BaCO3 + C → BaO + 2 CO↑
Usos del óxido de bario
- Como desecante de solventes orgánicos. Por su facilidad para reaccionar con agua, el BaO se ha usado desde mediados del siglo pasado como desecante para gasolina y solventes orgánicos básicos o neutros. Es muy activo secando a su alrededor, toma la humedad con mucha rapidez, con evolución de bastante calor, formando hidróxido de bario Ba(OH)2 el cual es estable hasta unos 1000 °C. Por ello el BaO se puede emplear a altas temperaturas. Además, tiene una alta capacidad de absorción de agua. Por cada molécula de BaO se puede absorber una de agua, y el Ba(OH)2 resultante también puede absorber cierta cantidad de agua. Es adecuado para los laboratorios de química analítica. No es pegajoso. Se puede usar en desecadores (grandes recipientes de vidrio con tapa donde se mantiene el ambiente interno seco). El BaO mantiene seca la miniatmósfera del desecador. Estos desecadores sirven para colocar sustancias o reactivos y así evitar que absorban agua del ambiente. También sirve para secar gases básicos, como el amoníaco NH3.

- En lámparas de descarga. El BaO se coloca en los electrodos de las lámparas de descarga como material emisor de electrones. Las lámparas de descarga están formadas por un tubo de vidrio, cuarzo u otro material adecuado, contienen un gas inerte y, en la mayoría de los casos, un vapor de metal. El vapor metálico puede ser de sodio o de mercurio. En el interior del tubo ocurren descargas eléctricas debido a que posee un electrodo positivo y uno negativo. El BaO se coloca en los electrodos de la lámpara. Los electrones que emite chocan con los átomos del vapor del metal y les transmite energía. Al pasar una corriente eléctrica a través de este gas o vapor se produce luz visible o radiación ultravioleta (UV).

- En la fabricación de cerámica. El BaO se utiliza en composiciones de recubrimiento vidriado de cerámica. Sin embargo, también ha sido probado como aditivo en la preparación de vitrocerámica. El BaO mejora de forma efectiva las características mecánicas y la resistencia química de este tipo de cerámica. Tiene una fuerte influencia en las propiedades térmicas y la composición de la fase cristalina de los materiales obtenidos.
- En la preparación de mezclas de cemento. Se ha probado el BaO como componente del cemento de fosfoaluminato. Este tipo de cemento es útil en ambientes marinos, ya que no tiene la misma tendencia a hidratarse que otros tipos de cemento, por lo que no sufre formación de poros ni expansiones. Sin embargo, los cementos de fosfoaluminato requieren ser fortalecidos en su desempeño mecánico para poder soportar las corrientes marinas y golpes de trozos flotantes de hielo presentes en el océano. La adición de BaO al cemento de fosfoaluminato modifica la estructura mineral de dicho material, mejora la estructura de los poros y aumenta considerablemente la fuerza compresiva de la pasta del cemento. En otras palabras, el BaO mejora la resistencia a la compresión de este tipo de cemento.
- Diversas aplicaciones. Se emplea como ingrediente para proporcionar opacidad en resinas dentales para el relleno de orificios en los dientes, realizado por odontólogos. También se utiliza como agente de nucleación para la preparación de polímeros de fluoruro de polivinilideno que se usan para aislar cables de electricidad.
Referencias
- Partyka, J. Effect of addition of BaO on sintering of glass-ceramic materials from SiO2-Al2O3-Na2O-K2O-CaO/MgO system. J. Therm. Anal Calorim. Recuperado de link.springer.com.
- Zhang, P. Effect of BaO on mineral structure and hydration behavior of phosphoaluminate cement. J. Therm. Anal Calorim. Recuperado de link.springer.com.
- Barium oxide. Recuperado de pubchem.ncbi.nlm.nih.gov.
- Smith, N.A. Lighting. Principle. In Electrical Engineer’s Reference Book (Sixteenth Edition). Recuperado de sciencedirect.com.
- Ebnesajjad, S. Fluoropolymer Foams. Foaming PVDF. In Melt Processible Fluoroplastics. Recuperado de sciencedirect.com.