¿Qué es el permanganato de sodio?
El permanganato de sodio es un compuesto químico de fórmula NaMnO4. Está disponible principalmente en forma monohidratada. Esta sal es higroscópica y tiene un bajo punto de fusión.
Tiene las mismas propiedades que el permanganato de potasio (KMnO4), aunque el permanganato de sodio es aproximadamente 15 veces más soluble en agua. A pesar de esto, el permanganato de potasio es comúnmente más utilizado, puesto que sus costos de producción son menores.
Se disuelve fácilmente en agua para dar soluciones de color púrpura profundo, cuya evaporación da cristales prismáticos de color púrpura-negro brillante del monohidrato NaMnO4 · H₂O. La sal de potasio no forma un hidrato. Debido a su naturaleza higroscópica, es menos útil en química analítica que su contrapartida de potasio.
Se puede preparar por la reacción de dióxido de manganeso con hipoclorito de sodio e hidróxido de sodio o carbonato de sodio de la siguiente manera:
2MnO2 + 3NaClO + 2NaOH → 2NaMnO4 + 3NaCl + H₂O
2MnO2 + 3NaClO + Na2CO3 → 2NaMnO4 + 3NaCl + CO₂
Usando carbonato de sodio, el rendimiento es menor y la reacción debe ser calentada para obtener el producto.
Propiedades físicas y químicas del permanganato de sodio
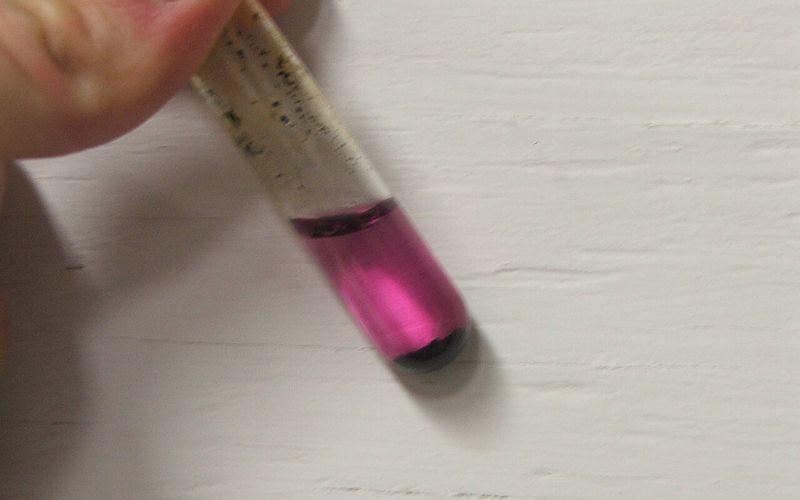
- Apariencia física. El permanganato de sodio se parece al permanganato de potasio. Son cristales prismáticos o esferas de color púrpura que en solución acuosa forman un líquido de color que va de rosa a púrpura, dependiendo de la concentración. Su apariencia se muestra en la figura 2.

- Peso molecular (forma anhidra): 141,9254 g/mol. Forma monohidratada: 159,94 g/mol.
- Punto de fusión: 36 °C. Forma monohidratada: 170 °C.
- Densidad: 1,972 g/ml.
- Solubilidad: es muy soluble en agua, pudiéndose disolver 900 g por cada litro a temperatura ambiente.
Reactividad y peligros del permanganato de sodio
El permanganato de sodio no es combustible, pero acelera la combustión de materiales combustibles. Si el material combustible está finamente dividido, la mezcla puede ser explosiva.
Puede encenderse espontáneamente en contacto con materiales combustibles líquidos. El contacto con ácido sulfúrico puede causar incendios o explosiones.
El ácido acético o el anhídrido acético pueden explotar con permanganatos si no se mantienen fríos. Las explosiones pueden ocurrir cuando los permanganatos que han sido tratados con ácido sulfúrico entran en contacto con benceno, disulfuro de carbono, éter dietílico, alcohol etílico, petróleo o materia orgánica.
Estas sustancias aceleran la quema cuando se involucran en un incendio. Algunos pueden descomponerse explosivamente cuando se calientan o se involucran en un incendio. Puede explotar por calor o contaminación.
Algunos reaccionarán explosivamente con hidrocarburos (combustibles). Puede encender combustibles (madera, papel, aceite, ropa, etc.). Los contenedores pueden explotar cuando se calientan. El escurrimiento puede crear peligro de incendio o explosión.
El permanganato de potasio reacciona con el agua para producir dióxido de manganeso, hidróxido de potasio y oxígeno. El hidróxido de potasio es un fuerte corrosivo. En casos severos, pueden producirse efectos sistémicos, incluyendo coagulación intravascular, hepatitis, pancreatitis y fallos.
La ingestión crónica puede causar parestesias, temblores debido a la toxicidad del manganeso. La neurotoxicidad del manganeso es el resultado del agotamiento de la dopamina y de las neurotoxinas, dopamina quinona y peróxido.
El permanganato de sodio daña el tejido ocular al contacto, produciendo quemaduras. Puede ser irritante al contacto con la piel, dejando manchas púrpura en ella. En caso de inhalación puede causar daños al tracto respiratorio.
Si el compuesto entra en contacto con la piel, se debe enjuagar con abundante agua durante al menos 15 minutos mientras se retira la ropa contaminada y los zapatos.
En caso de ingestión, no se debe inducir el vómito. Se debe aflojar la ropa apretada, como cuellos de camisa, cinturón o corbata. Si la víctima no respira, se debe dar resucitación boca a boca.
En caso de inhalación, se debe retirar a la víctima del lugar de exposición y trasladarse a un sitio fresco. Si esta no respira, se debe administrar respiración artificial. Si le es difícil respirar se debe administrar oxígeno.
En todos los casos se debe obtener atención médica inmediata.
Usos del permanganato de sodio
- Limpieza y desinfección. El permanganato de sodio, al igual que el compuesto de potasio, es un antiséptico desinfectante y bactericida. Sus usos incluyen resinas blanqueadoras, ceras, grasas, paja, algodón, seda y otras fibras y gamuza.
- Industriales. También se utiliza como desinfectante, desodorante, desinfectante químico en fotografía, y reactivo en química orgánica sintética.
- Usos ilícitos. Incluyen la producción de drogas de abuso y de aborto por aplicación tópica a la pared vaginal. Históricamente, las soluciones de permanganato se han utilizado como irrigante uretral y el lavado de líquido para el envenenamiento.
- Como oxidante. Actúa como un agente oxidante en la oxidación de o-tolueno sulfonamida para producir sacarina y purificación de tolueno amida. También es un antídoto de la morfina y el fósforo, y reacciones sintéticas orgánicas / farmacéuticas.
- Tratamiento de aguas. Se ha utilizado en el tratamiento del agua y la rehabilitación del suelo debido a que es capaz de degradar el BTEX (benceno, tolueno, etilbenceno y xileno), los fenoles, los hidrocarburos aromáticos policíclicos (HAP), los etenos clorados y los explosivos, y eliminar el sulfuro de hidrógeno.
- Grabado de plásticos. Debido a la alta solubilidad en agua, se prefiere el permanganato sódico para aplicaciones que requieren altas concentraciones de iones permanganato, como el grabado de partes de plástico de la placa de circuito impreso.
- Otros usos. Incluyen el agente de tratamiento de superficie metálica y la formulación de limpieza de metales, etc. También puede sustituir el permanganato de potasio en algunas aplicaciones, puesto que es el ion permanganato el que es el agente oxidante. Sin embargo, dado que el permanganato de sodio existe en forma monohidratada, este no se puede usar para aplicaciones analíticas como titulaciones redox.
Referencias
- Material data safety sheet sodium permanganate. Recuperado de dogee.org.
- Material Safety Data Sheet Sodium permanganate monohydrate. Recuperado de sciencelab.com.
- SODIUM PERMANGANATE. Recuperado de toxnet.nlm.nih.gov.
- SODIUM PERMANGANATE. Recuperado de cameochemicals.noaa.gov.
- Sodium Permanganate Aqueous Solution (NaMnO4). Recuperado de en.changyuancorp.com.