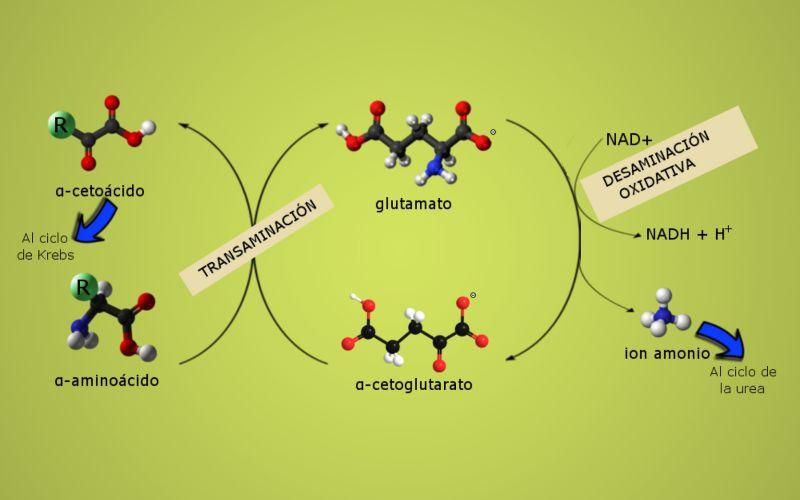
¿Qué es la transaminación?
La transaminación es un proceso químico fundamental en el metabolismo de aminoácidos, donde un grupo amino (-NH2) se transfiere de un aminoácido a un alfa-cetoácido para crear un nuevo aminoácido y un nuevo cetoácido, catalizados por enzimas llamadas transaminasas o aminotransferasas.
La reacción general de transaminación implica el intercambio entre un aminoácido y un α-cetoácido cualquiera, donde el intercambio de un grupo amino rinde la versión cetoácida del primer aminoácido sustrato y la versión aminoacídica del primer α-cetoácido sustrato.
El grupo amino intercambiado usualmente es el amino alfa, es decir, el que participa en la formación de los enlaces peptídicos y que define la estructura de los aminoácidos, aunque también pueden ocurrir reacciones que involucran otros grupos amino presentes en posiciones diferentes.
Con excepción de la lisina, la treonina, la prolina y la hidroxiprolina, todos los aminoácidos participan en reacciones de transaminación, aunque para la histidina, la serina, la metionina y la fenilalanina se han descrito transaminasas, pero sus rutas metabólicas no implican este tipo de reacciones.
Las reacciones de transaminación entre aminoácidos y α-cetoácidos fueron descubiertas en 1937 por Braunstein y Kritzmann, y desde entonces han sido objeto de intensos estudios, pues ocurren en muchos tejidos de organismos diferentes y con distintos propósitos.
En los seres humanos, por ejemplo, las transaminasas están ampliamente distribuidas en los tejidos corporales y son particularmente activas en el tejido muscular cardiaco, en el hígado, en el tejido muscular esquelético y en los riñones.
Mecanismo de reacción de la transaminación
Las reacciones de transaminación implican más o menos el mismo mecanismo. Como se comentó anteriormente, estas reacciones ocurren como un intercambio reversible de un grupo amino entre un aminoácido y un α-cetoácido (desaminado), produciendo el α-cetoácido del aminoácido donador y el aminoácido del α-cetoácido receptor.
Estas reacciones dependen de un compuesto conocido como piridoxal fosfato, un derivado de la vitamina B6 que participa como un transportador de grupos amino y que se une a las enzimas transaminasas por medio de la formación de una base de Schiff entre el grupo aldehído de esta molécula y el ε-amino de un residuo de lisina en el sitio activo de la enzima.
La unión entre el piridoxal fosfato y el residuo de lisina en el sitio activo no es covalente, sino que se da a través de la interacción electrostática entre la carga positiva del nitrógeno en la lisina y la carga negativa en el grupo fosfato del piridoxal.
En el transcurso de la reacción, el aminoácido que funciona como sustrato desplaza el grupo ε-amino del residuo de lisina en el sitio activo que participa en la base de Schiff con el piridoxal.
Mientras tanto, un par de electrones del carbono alfa del aminoácido son removidos y transferidos hacia el anillo de piridina que compone al piridoxal fosfato (con carga positiva) y luego son “entregados” al α-cetoácido que funciona como segundo sustrato.
De esta manera, el piridoxal fosfato no solo participa en la transferencia o el transporte de los grupos amino entre los aminoácidos y los α-cetoácidos que son sustrato de las transaminasas, sino que también actúa como “sumidero” de electrones, facilitando la disociación del hidrógeno alfa del aminoácido.
En resumen, el primer sustrato, un aminoácido, transfiere su grupo amino al piridoxal fosfato, desde donde se transfiere subsecuentemente hacia el segundo sustrato, un α-cetoácido, formando, en el ínterin, un compuesto intermediario conocido como piridoxamina fosfato.
Funciones de la transaminación
- Interconversión de aminoácidos. Permite transformar un aminoácido en otro. Facilita la síntesis de aminoácidos no esenciales a partir de esqueletos carbonados.
- Transferencia del grupo amino. Transfiere el grupo -NH₂ de un aminoácido a un α-cetoácido. El aminoácido donador se convierte en su cetoácido correspondiente. El cetoácido receptor se convierte en un nuevo aminoácido.
- Integración del metabolismo de aminoácidos y carbohidratos. Conecta el metabolismo proteico con el ciclo de Krebs. Los cetoácidos resultantes pueden entrar en rutas energéticas (gluconeogénesis o producción de ATP).
- Canalización del nitrógeno hacia el glutamato. La mayoría de los grupos amino se transfieren al α-cetoglutarato, formando glutamato. El glutamato actúa como colector central de nitrógeno en el organismo.
- Paso previo a la eliminación del nitrógeno. Es un paso clave antes de la desaminación oxidativa y del ciclo de la urea. Facilita la eliminación del nitrógeno de forma segura.
- Reacciones reversibles. Permite tanto la degradación como la síntesis de aminoácidos según las necesidades metabólicas.
- Importancia clínica. Las enzimas implicadas (transaminasas o aminotransferasas), como ALT (GPT) y AST (GOT), son marcadores de daño hepático cuando se elevan en sangre.
Ejemplos de transaminación
Las reacciones de transaminación más comunes se relacionan con los aminoácidos alanina, ácido glutámico y ácido aspártico.
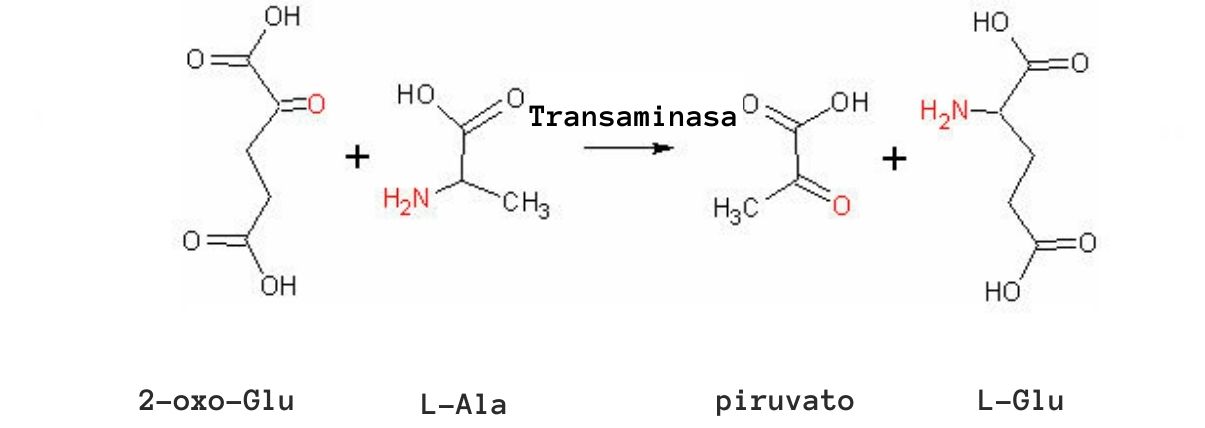
Algunas enzimas aminotransferasas pueden, además del piridoxal fosfato, emplear al piruvato como “coenzima”, como es el caso de la glutamato-piruvato transaminasa, que cataliza la siguiente reacción:
glutamato + piruvato ↔ alanina + α-Cetoglutarato
Las células musculares dependen de esta reacción para producir alanina a partir de piruvato y para obtener energía a través del ciclo de Krebs por medio del α-cetoglutarato. En dichas células la utilización de la alanina como fuente de energía depende de la eliminación de los grupos amino como iones de amonio en el hígado, a través del ciclo de la urea.
Otra reacción de transaminación muy importante en diferentes especies es la catalizada por la enzima aspartato aminotransferasa:
L-Aspartato + α-Cetoglutarato ↔ Oxalacetato + L-Glutamato
Finalmente, pero no menos importante, la reacción de transaminación del ácido γ-aminobutírico (GABA), un aminoácido no proteico esencial para el sistema nervioso central que funciona como neurotransmisor inhibitorio. La reacción es catalizada por una γ-aminobutírico transaminasa y es más o menos como sigue:
α-Cetoglutarato + ácido 4-aminobutanoico ↔ Glutamato + Semialdehído succínico
El semialdehído succínico es convertido en ácido succínico mediante una reacción de oxidación y este último puede ingresar al ciclo de Krebs para la producción de energía.