¿Qué es la lactoferrina?
La lactoferrina, apolactoferrina o lactotransferrina, es una proteína multifuncional clave en el sistema inmune, presente en la leche materna y otros fluidos. Tiene la capacidad de unirse y transferir iones de hierro (Fe3+). Está relacionada con la proteína plasmática de unión a hierro conocida como “transferrina”.
Fue aislada en 1939 por Sorensen y Sorensen a partir de leche bovina y, casi 30 años después, en 1960, Johannson determinó su presencia en la leche humana (su nombre deriva de su clasificación como la proteína de unión a hierro más abundante de la leche).
Investigaciones posteriores identificaron la lactoferrina en otras secreciones de glándulas exocrinas como la bilis, el jugo pancreático y las secreciones del intestino delgado, así como en los gránulos secundarios de los neutrófilos, células plasmáticas pertenecientes al sistema inmune.
Esta proteína se halla también en las lágrimas, la saliva, el semen, los fluidos vaginales, las secreciones bronquiales y nasales y en la orina, aunque es particularmente abundante en la leche (es la segunda proteína en mayor concentración después de la caseína) y el calostro.
Aunque inicialmente se consideraba simplemente una proteína con actividad bacteriostática de la leche, se trata de una proteína con gran variedad de funciones biológicas, aunque no todas tienen que ver con su capacidad de transferencia de iones de hierro.
Estructura de la lactoferrina
- Peso, carga e isoelectricidad. La lactoferrina es una glucoproteína de alrededor de 80 kDa de peso molecular, compuesta por 703 residuos aminoacídicos cuya secuencia tiene gran homología entre especies diferentes. Es una proteína básica, cargada positivamente y con un punto isoeléctrico entre 8 y 8.5.
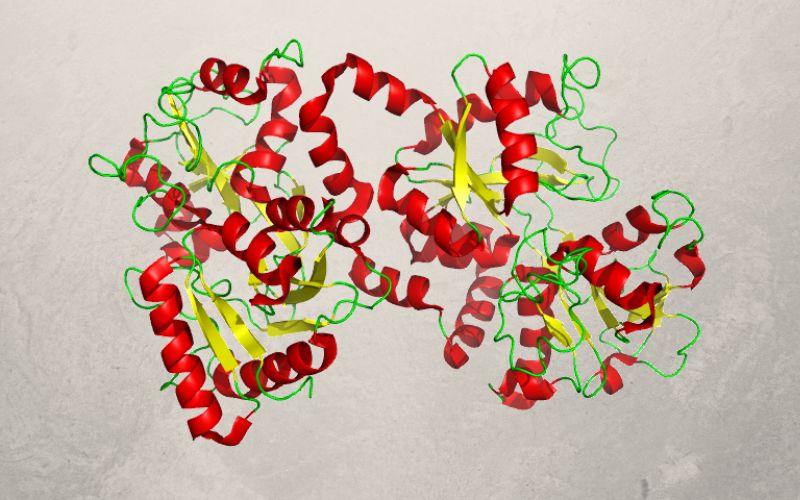
- Lóbulo N y lóbulo C. Está formada por una sola cadena polipeptídica que está plegada para formar dos lóbulos simétricos denominados lóbulo N (residuos 1-332) y lóbulo C (residuos 344-703), que comparten entre el 33 y el 41% de homología entre sí. Tanto el lóbulo N como el lóbulo C están formados por láminas β-plegadas y hélices alfa, las cuales constituyen dos dominios por lóbulo, el dominio I y el dominio II (C1, C2, N1 y N2). Ambos lóbulos están conectados a través de una región “bisagra”, compuesta por una hélice alfa entre los residuos 333 y 343, lo que le proporciona una mayor flexibilidad molecular a la proteína. Los análisis de la secuencia aminoacídica de esta proteína revelan gran cantidad de sitios potenciales para la glicosilación. El grado de glicosilación es muy variable y determina la resistencia frente a la actividad de proteasas o a pH considerablemente bajos. El sacárido más común en su porción carbohidratada es la manosa, con más o menos un 3% de azúcares hexosas y 1% de hexosaminas. Cada lóbulo de la lactoferrina es capaz de unirse reversiblemente a dos iones metálicos, bien sean de hierro (Fe2+, Fe3+), de cobre (Cu2+), de zinc (Zn2+), de cobalto (Co3+) o de manganeso (Mn2+), en sinergia con un ion bicarbonato.
- Otras moléculas. También puede unirse, aunque con menor afinidad, a otras moléculas como lipopolisacáridos, glucosaminoglicanos, ADN y heparina. Cuando la proteína está unida a dos iones de hierro, se conoce como hololactoferrina, mientras que cuando está en su forma “libre”, se denomina apolactoferrina y, cuando solo está unida a un átomo de hierro, se conoce como lactoferrina monoférrica. La apolactoferrina tiene una conformación abierta, mientras que la hololactoferrina tiene una configuración cerrada, por lo que es más resistente a la proteólisis.
- Otras formas de lactoferrina. Algunos autores describen la existencia de tres isoformas de lactoferrina: la α, la β y la γ. La forma lactoferrina-α es descrita como aquella con la capacidad de unión al hierro y sin actividad ribonucleasa. Las formas lactoferrina-β y lactoferrina-γ tienen actividad ribonucleasa, pero no son capaces de unirse a iones metálicos.
Funciones de la lactoferrina
- Actividad antimicrobiana. Inhibe el crecimiento de bacterias al secuestrar el hierro, un nutriente esencial para muchos microorganismos. Tiene acción directa contra bacterias, virus, hongos y parásitos, dañando sus membranas.
- Refuerzo del sistema inmunológico. Estimula la actividad de células defensivas como linfocitos, macrófagos y neutrófilos. Ayuda a regular la respuesta inflamatoria, evitando reacciones excesivas.
- Acción antiviral. Impide la entrada de ciertos virus a las células al bloquear los receptores celulares. Es efectiva contra virus como herpes, rotavirus, hepatitis C, entre otros.
- Actividad antiinflamatoria. Reduce la producción de mediadores proinflamatorios. Contribuye al equilibrio del sistema inmune, especialmente en infecciones intestinales.
- Protección de la mucosa intestinal. Favorece el crecimiento de bacterias beneficiosas (efecto prebiótico). Ayuda a mantener la integridad de la barrera intestinal.
- Facilita la absorción del hierro. Aunque se une al hierro, lo hace de forma que mejora su biodisponibilidad, especialmente en lactantes.
- Posible efecto antitumoral. Estudios sugieren que puede inhibir el crecimiento de células tumorales y favorecer la apoptosis (aún en investigación).

- Usos farmacológicos. La lactoferrina puede ser obtenida directamente al ser purificada a partir de la leche de vaca, pero otros sistemas modernos se basan en su producción como proteína recombinante en distintos organismos de fácil, rápido y económico crecimiento. Como compuesto activo de algunos fármacos, esta proteína es empleada para el tratamiento de úlceras estomacales e intestinales, así como de diarrea y hepatitis C. Es empleada contra infecciones de origen bacteriano y viral y, además, se utiliza como estimulante del sistema inmune para la prevención de algunas patologías como el cáncer.
Fuentes de lactoferrina en el cuerpo humano
La expresión de esta proteína puede detectarse inicialmente en los estadios de dos y cuatro células del desarrollo embrionario y luego en la etapa de blastocisto, hasta el momento de la implantación.
Posteriormente, se evidencia en los neutrófilos y en las células epiteliales de los sistemas digestivo y reproductivo en formación.
La síntesis de esta proteína es ejecutada en los epitelios mieloides y secretorios. En un ser humano adulto, los mayores niveles de expresión de lactoferrina son detectados en la leche materna y en el calostro.
También puede hallarse en muchas secreciones mucosas como los fluidos uterinos, seminales y vaginales, en la saliva, la bilis, el jugo pancreático, las secreciones del intestino delgado, las secreciones nasales y las lágrimas. Se ha determinado que los niveles de esta proteína cambian durante el embarazo y durante el ciclo menstrual.
En el 2000 se determinó la producción de lactoferrina en los riñones, donde es expresada y secretada a través de los túbulos colectores y puede ser reabsorbida en la porción distal de los mismos.
La mayor parte de la lactoferrina plasmática en los seres humanos adultos proviene de los neutrófilos, donde se almacena en gránulos secundarios específicos y en gránulos terciarios (aunque en menor concentración).
Referencias
- Adlerova, L., Bartoskova, A., Faldyna, M. Lactoferrin: a review. Veterinarni Medicina.
- Berlutti, F., Pantanella, F., Natalizi, T., Frioni, A., Paesano, R., Polimeni, A., Valenti, P. Antiviral properties of lactoferrin—a natural immunity molecule. Molecules.
- Brock, J. Lactoferrin: a multifunctional immunoregulatory protein? Immunology today.
- Brock, J.H. The physiology of lactoferrin. Biochemistry and Cell Biology.
- Sanchez, L., Calvo, M., Brock, J.H. Biological role of lactoferrin. Archives of disease in childhood.