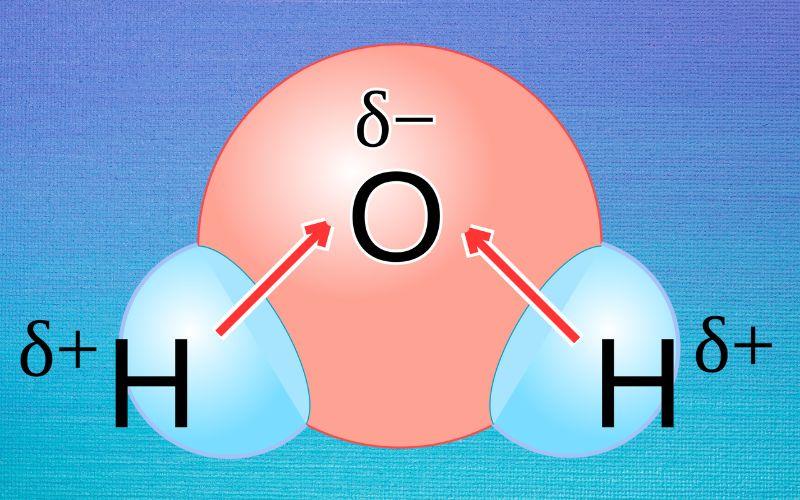
¿Qué es un enlace covalente polar?
Un enlace covalente polar es el que se forma entre dos átomos que comparten electrones de forma desigual por diferencias en su electronegatividad. Eso genera que las cargas se separen, con un átomo desarrollando una carga parcial positiva, y el otro una carga parcial negativa.
Se dice que es covalente porque en teoría hay una compartición equitativa de un par electrónico entre los dos átomos enlazados; como se representa gráficamente en la imagen inferior, los dos electrones se comparten por igual. El átomo E· dona un electrón, mientras ·X aporta el segundo electrón para formar el enlace covalente E:X o E-X.
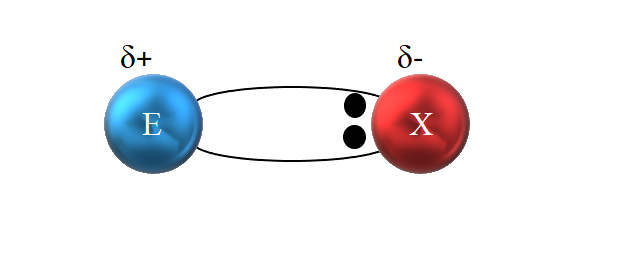
No obstante, tal como se ve en la misma imagen, los dos electrones no están situados en el centro de E y X, indicando que “circulan” con la misma frecuencia entre ambos átomos, sino que están más cerca de X que de E. Esto significa que X ha atraído el par de electrones hacia sí debido a su mayor electronegatividad.
Al estar los electrones del enlace más cerca de X que de E, en torno a X se crea una región de alta densidad electrónica, δ-, mientras que en E aparece una región pobre en electrones, δ+. Por lo tanto, se tiene una polarización de las cargas eléctricas: un enlace covalente polar.
Características del enlace covalente polar
– Grados de polaridad. Los enlaces covalentes son abundantes en la naturaleza. Prácticamente, están presentes en todas las moléculas heterogéneas y en los compuestos químicos, ya que, a fin de cuentas, se forma cuando dos átomos diferentes E y X se enlazan. Sin embargo, hay enlaces covalentes más polares que otros, y para averiguarlo se debe recurrir a las electronegatividades. Cuánto más electronegativo sea X, y menos electronegativo sea E (electropositivo), entonces el enlace covalente resultante será más polar. El modo convencional para calcular dicha polaridad es mediante la fórmula:
χX – χE
Donde χ es la electronegatividad de cada átomo de acuerdo a la escala de Pauling. Si esta sustracción tiene valores comprendidos entre 0,5 y 2, entonces será un enlace polar. Por lo tanto, es posible comparar el grado de polaridad entre varios enlaces E-X. En caso de que el valor obtenido sea más alto que 2, se habla de un enlace iónico, E+X– y no Eδ+-Xδ-. No obstante, la polaridad del enlace E-X no es absoluta, pues depende de los entornos moleculares. Es decir, en una molécula -E-X-, donde E y X forman enlaces covalentes con otros átomos, estos últimos influyen directamente en dicho grado de polaridad.
– Elementos químicos que los originan. Si bien E y X pueden tratarse de cualquier elemento, no todos originan enlaces covalentes polares. Por ejemplo, si E es un metal altamente electropositivo, como los alcalinos (Li, Na, K, Rb y Cs), y X un halógeno (F, Cl, Br y I), tenderán a formar compuestos iónicos (Na+Cl–) y no moléculas (Na-Cl). Por eso, los enlaces covalentes polares suelen encontrarse entre dos elementos no metálicos, y en menor grado, entre elementos no metálicos y algunos metales de transición. Viendo el bloque p de la tabla periódica, se tiene muchas opciones para formar este tipo de enlaces químicos.
– Carácter polar y iónico. En las moléculas grandes no tiene mucha importancia pensar qué tan polar es un enlace, pues estas son altamente covalentes, y llama más la atención la distribución de sus cargas eléctricas (dónde están las regiones ricas o pobres de electrones) que definir el grado de covalencia de sus enlaces internos. No obstante, con las moléculas diatómicas o pequeñas, dicha polaridad Eδ+-Xδ- es bastante relativa. Esto no es problema con las moléculas formadas entre elementos no metálicos, pero cuando participan metales de transición o metaloides, ya no se habla solamente de un enlace covalente polar, sino de un enlace covalente con cierto carácter iónico. Y en el caso de los metales de transición, de un enlace covalente de coordinación dada la naturaleza del mismo.
Ejemplos de enlace covalente polar
C-O
El enlace covalente entre el carbono y oxígeno es polar, debido a que el primero es menos electronegativo (χC = 2,55) que el segundo (χO = 3,44). Por lo tanto, cuando veamos los enlaces C-O, C=O o C-O–, sabremos que se trata de enlaces polares.
H-X
Los halogenuros de hidrógeno, HX, son ejemplos ideales para comprender el enlace polar en sus moléculas diatómicas. Teniendo la electronegatividad del hidrógeno (χH = 2,2), podemos estimar qué tan polares son estos halogenuros entre sí:
-HF (H-F), χF (3,98) – χH (2,2) = 1,78
-HCl (H-Cl), χCl (3,16) – χH (2,2) = 0,96
-HBr (H-Br), χBr (2,96) – χH (2,2) = 0,76
-HI (H-I), χI (2,66) – χH (2,2) = 0,46
Nótese que de acuerdo a estos cálculos, el enlace H-F es el más polar de todos. Ahora, cuál es su carácter iónico expresado como porcentaje, es otro tema. Este resultado no es de extrañar debido a que el flúor es el elemento más electronegativo de todos.
Al descender la electronegatividad desde el cloro hasta el yodo, de igual modo se vuelven menos polares los enlaces H-Cl, H-Br y H-I. El enlace H-I debería ser apolar, pero en realidad es polar y además muy “quebradizo”: se rompe con facilidad.
O-H
El enlace polar O-H quizás sea el más importante de todos, gracias a él existe la vida, pues colabora con el momento dipolar del agua. Si calculamos la diferencia entre las electronegatividades del oxígeno e hidrógenos tendremos:
χO (3,44) – χH (2,2) = 1,24
No obstante, la molécula de agua, H₂O, tiene dos de estos enlaces, H-O-H. Esto, y la geometría angular de la molécula y su asimetría, la vuelven un compuesto altamente polar. De hecho, es el ejemplo clásico de enlace covalente polar.
N-H
El enlace N-H está presente en los grupos aminos de las proteínas. Repitiendo el mismo cálculo tenemos:
χN (3,04) – χH (2,2) = 0,84
Esto refleja que el enlace N-H es menos polar que O-H (1,24) y F-H (1,78).
Fe-O
El enlace Fe-O es importante porque se encuentran sus óxidos en los minerales de hierro. Veamos si es más polar que H-O:
χO (3,44) – χFe (1,83) = 1,61
De aquí se supone, acertadamente, que el enlace Fe-O es más polar que el enlace H-O (1,24); o lo que es igual a decir que Fe-O tiene mayor carácter iónico que H-O.
Estos cálculos sirven para figurar los grados de polaridad entre varios enlaces, pero no bastan para dictaminar si un compuesto es iónico, covalente, o su carácter iónico.
Referencias
- Whitten, Davis, Peck & Stanley. Química (8va ed.). CENGAGE Learning.
- Shiver & Atkins. Química Inorgánica (Cuarta edición). McGraw Hill.
- Helmenstine, A.M. Polar Bond Definition and Examples (Polar Covalent Bond). Recuperado de thoughtco.com.
- Chemical polarity. Recuperado de en.wikipedia.org.
- Properties of Polar Covalent Bonds. Recuperado de chem.libretexts.org.