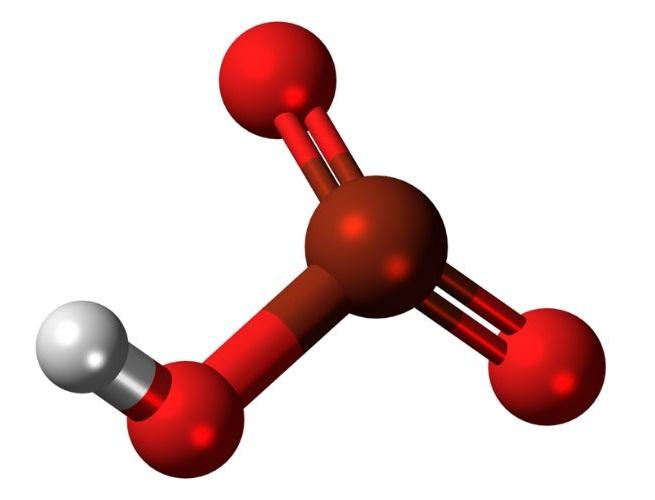
¿Qué es el ácido brómico?
El ácido brómico, también conocido como bromato de hidrógeno o ácido brómico (V), es un compuesto químico de fórmula HBrO3. Se trata de un oxácido de bromo con una estructura análoga al ácido clórico. El compuesto es un ácido muy fuerte.
Para preparar ácido brómico, un bromato soluble se disuelve usualmente en agua y se añade una sal de bario soluble. Precipita bromato de bario poco soluble.
El bromato de bario puede entonces disolverse en agua y acidificarse con ácido sulfúrico para precipitar el sulfato de bario básicamente insoluble y dejar atrás el ácido brómico:
2KBrO3(aq) + BaCl2(aq) —> Ba(BrO3)2(s) + 2KCl(aq)
Ba(BrO3)2(aq) + H2SO4(aq) —> 2HBrO3 + BaSO4
El compuesto también puede producirse por la descomposición de pentacloruro de bromo en solución alcalina, según la reacción:
BrCl5 + 3 H₂O → HBrO3 + 5 HCl
El ácido brómico es un fuerte agente oxidante. El ion bromato puede oxidarse adicionalmente con flúor elemental o difluoruro de xenón en presencia de base, la oxidación acompañada de pequeñas explosiones y el tubo de teflón atrapado en el fuego.
Propiedades físicas y químicas del ácido brómico
- Apariencia: el ácido brómico existe únicamente en solución incolora (hasta un 50% p/v) que se torna amarillenta en contacto con el aire.
- Peso molecular: 128,91 g/mol y se descompone a 100 °C.
- pKa: -2.
- Estabilidad: al ser un compuesto inestable, sus propiedades físico-químicas fueron obtenidas mediante cálculos computacionales.
- Punto de fusión: 206,04 °C.
- Punto de ebullición: 517,26 °C.
- Solubilidad: en agua es de 1 x 106 mg/l a 25 °C.
- Reacciones: el compuesto es un fuerte agente oxidante. Al mezclarlo con etanol o éter se descompone formando ácido acético en una reacción exotérmica. Es fundamental para la elaboración de las sales de bromato (BrO3-) que se preparan haciendo reaccionar los carbonatos u óxidos de los metales con ácido brómico.
Reactividad y peligros del ácido brómico
El ácido brómico es un compuesto inestable descomponiéndose a bromo elemental. Al ser un ácido fuerte, es extremadamente peligroso en caso de contacto con la piel (corrosivo e irritante), de contacto con los ojos (irritante) y en caso de ingestión. Muy peligroso también, en caso de inhalación.
Una sobreexposición severa puede producir daño pulmonar, asfixia, pérdida del conocimiento o muerte. La exposición prolongada puede causar quemaduras en la piel y ulceraciones. La sobreexposición por inhalación puede causar irritación respiratoria.
La sustancia es tóxica para los riñones, los pulmones y las membranas mucosas. La exposición repetida o prolongada a la sustancia puede producir daños en estos órganos.
- En caso de contacto con los ojos. Verificar si se están usando lentes de contacto y retirarlas inmediatamente. Se deben enjuagar los ojos con agua corriente durante al menos 15 minutos, manteniendo los párpados abiertos. Se puede usar agua fría. No se debe utilizar ungüento para los ojos.
- En caso de contacto con la piel. Si el producto químico entra en contacto con la ropa, retirarla lo más rápido posible, protegiendo las propias manos y cuerpo. Colocar a la víctima bajo una ducha de seguridad. Si el producto químico se acumula en la piel expuesta de la víctima, como las manos, se lava suave y cuidadosamente la piel contaminada con agua corriente y jabón no abrasivo. Se puede emplear agua fría. Si la irritación persiste, buscar atención médica. Lavar la ropa contaminada antes de volver a usarla. Si el contacto con la piel es grave, se debe lavar con un jabón desinfectante y cubrir la piel contaminada con una crema antibacteriana.
- En caso de inhalación. Es aconsejable dejar reposar a la víctima en un área bien ventilada. Si la inhalación es grave, se debe evacuar a la víctima a una zona segura tan pronto como sea posible. Aflojar la ropa apretada, como cuello de camisa, cinturones o corbata. Si a la víctima le resulta difícil respirar, se debe administrar oxígeno. Si la víctima no está respirando, se realiza una resucitación boca a boca. Siempre tomando en cuenta que puede ser peligroso para la persona que proporciona ayuda dar reanimación boca a boca cuando el material inhalado es tóxico, infeccioso o corrosivo. En caso de ingestión, no inducir el vómito. Aflojar la ropa apretada, como cuellos de camisa, cinturones o corbatas. Si la víctima no está respirando, realizar reanimación boca a boca.
En todos los casos se debe buscar atención médica inmediata.
Usos del ácido brómico
- Agente oxidante. El ácido brómico es usado como un poderoso agente oxidante en reacciones de laboratorio. Es usado para producir compuestos químicos como iodatos, ácido clórico, ácido tetraihónico, entre otros.
- Producción de bromatos. Se usa para producir bromatos, como el bromato de hierro, de plomo, de manganeso, de mercurio, entre otros.
- Reacción de Belousov-Zhabotinsky. El ácido brómico actúa como un intermediario importante en la reacción de Bélousov-Zhabotinsky. Esta reacción es un ejemplo de relojes químico e ilustra una reacción de no equilibrio termodinámico. La reacción de oscilación es catalizada por cerio y está inherentemente conectada a la química de los oxoácidos de bromo HBrOx. El creciente interés en los sistemas químicos no lineales ha proporcionado fuertes incentivos para estudiar la química del bromo. En la reacción de Belousov-Zhabotinsky, los compuestos de bromo implicados son el ácido hipobromoso HOBr, el ácido bromoso HOBrO y ácido brómico HBrO3 (3). Este tipo de reacciones son importantes para la química teórica. En ellas se muestran que las reacciones químicas no tienen que ser dominadas por el comportamiento termodinámico de equilibrio.
Referencias
- Bromic Acid. Recuperado de chemyq.com.
- Bromic acid. Recuperado de ebi.ac.uk.
- Chloric acid. Recuperado de ebi.ac.uk.
- Belousov Zhabotinsky reaction 8 x normal speed. Recuperado de youtubecom.