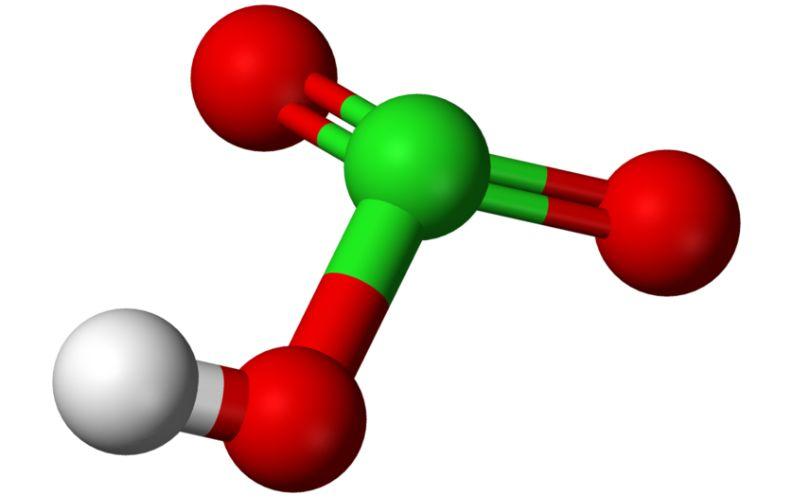
¿Qué es el ácido clórico?
El ácido clórico es un compuesto inorgánico de fórmula HClO3, un oxácido de cloro y precursor formal de las sales de clorato. Es un ácido fuerte capaz de donar un hidrógeno a un aceptor o base Bronsted.
El compuesto se obtiene con clorato de bario (clorato de barita) con ácido sulfúrico para producir sulfato de bario, insoluble en agua según la siguiente reacción:
Ba(ClO3)2 + H2SO4 → 2HClO3 + BaSO4
Otro método de obtención es calentando ácido hipocloroso para obtener ácido clórico y cloruro de hidrógeno según la reacción:
3HClO → HClO3 + 2HCl
El ácido clórico (HClO3) es un potente oxidante dado de que es capaz de reducirse a estados de oxidación +3, +1 y -1. Se utiliza para la fabricación de sales de clorato.
Se descompone en concentraciones superiores al 30%. También se descompone al calentarse, por ello debe mantenerse frío todo el tiempo, y todos los frascos de vidrio usados para manejar deben ser previamente refrigerados.
Propiedades físicas y químicas
– El ácido clórico existe únicamente en solución. Es un líquido incoloro sin aroma característico.
– El compuesto tiene un peso molecular de 84,459 g/mol y una densidad de 1 g/ml a 25 °C aproximadamente.
– Posee un punto de ebullición mayor a los 100 °C y una solubilidad en agua de 40 g por cada 100 ml de este solvente a 25 °C.
– El ácido clórico acelerará la quema de materiales combustibles y puede encender la mayoría en contacto. El compuesto es corrosivo para metales y tejidos.
Auto-reactivo
– Las concentraciones de ácido clórico por encima del 40% se descomponen.
– El sulfuro de antimonio y las soluciones concentradas de ácido clórico reaccionan con incandescencia.
– El sulfuro de arsénico y las soluciones concentradas de ácido clórico reaccionan con incandescencia.
– Reacciona con vigor, incluso explota con otros sulfuros metálicos, es decir, sulfuro de cobre.
– En contacto con materiales oxidables, incluyendo amoniaco, las reacciones pueden ser extremadamente violentas.
– El papel de filtro se enciende después de sumergirlo en ácido clorhídrico.
– Las explosiones han sido registradas por mezclas de solución de ácido clórico con metales como antimonio, bismuto y hierro. Esto es debido a la formación de compuestos explosivos, incluyendo el hidrógeno.
Reactividad y peligros
El ácido clórico es un compuesto inestable. Al ser un ácido fuerte, es extremadamente peligroso en caso de contacto con la piel (es corrosivo e irritante), de contacto con los ojos (irritante) y en caso de ingestión. También ese muy peligroso en caso de inhalación.
Una sobreexposición severa puede producir daño pulmonar, asfixia, pérdida del conocimiento o muerte. La exposición prolongada puede causar quemaduras en la piel y ulceraciones.
La sobreexposición por inhalación puede causar irritación respiratoria. La inflamación del ojo se caracteriza por enrojecimiento, riego y picazón. La inflamación de la piel se caracteriza por picazón, descamación, enrojecimiento y ocasionalmente, formación de ampollas.
La sustancia es tóxica para los riñones, los pulmones y las membranas mucosas. La exposición repetida o prolongada a la sustancia puede producir daños en estos órganos.
En caso de contacto con los ojos se debe verificar si se está usando lentes de contacto y removerlos inmediatamente. Se debe enjuagar los ojos con agua corriente durante al menos 15 minutos, manteniendo los párpados abiertos. Se puede usar agua fría. No se debe emplear ungüento para los ojos.
Si el producto químico entra en contacto con la ropa, retírela lo más rápido posible, protegiendo sus propias manos y cuerpo. Coloque a la víctima bajo una ducha de seguridad.
Si el producto químico se acumula en la piel expuesta de la víctima, como las manos, se lava suave y cuidadosamente la piel contaminada con agua corriente y jabón no abrasivo.
También se puede neutralizar el ácido con hidróxido de sodio diluido o con una base débil como bicarbonato de sodio. Si la irritación persiste, busque atención médica. Lave la ropa contaminada antes de volver a usarla.
Si el contacto con la piel es grave, se debe lavar con un jabón desinfectante y cubrir la piel contaminada con una crema antibacteriana.
En caso de inhalación, se debe dejar reposar a la víctima en un área bien ventilada. Si la inhalación es grave, se debe evacuar a la víctima a una zona segura tan pronto como sea posible.
Afloje la ropa apretada, tales como cuello de camisa, cinturones o corbata. Si a la víctima le resulta difícil respirar, se debe administrar oxígeno. Si la víctima no está respirando, se realiza una resucitación boca a boca.
Se debe tener en cuenta que puede ser peligroso para la persona que proporciona ayuda dar reanimación boca a boca, cuando el material inhalado es tóxico, infeccioso o corrosivo.
En caso de ingestión, no induzca el vómito. Afloje la ropa apretada, como cuellos de camisa, cinturones o corbatas. Si la víctima no está respirando, hacer resucitación boca a boca. En todos los casos se debe buscar atención médica inmediata.
Usos
El ácido clórico es usado principalmente para la formación de sales de clorato, como clorato de sodio, de calcio, de magnesio, estroncio, plomo, cobre y plata, así como el protoclorato y el perclorato de mercurio se preparan usando el ácido clórico como reactivo.
Precursor estable del dióxido de cloro, se utiliza en la producción electroquímica de perclorato de amonio de alta pureza.
La principal producción de ácido clórico se inició durante la Revolución industrial en Europa y se utilizó para fabricar cloruro de vinilo para tuberías de PVC.
Otro uso para el ácido en numerosas aplicaciones de menor escala, incluyendo limpieza doméstica, producción de gelatina y otros aditivos alimentarios, descalcificación y procesamiento del cuero.
Referencias
- chloric acid (S.F.). Recuperado de weebly.com.
- CHLORIC ACID (S.F.). Recuperado de chemicalbook.com.