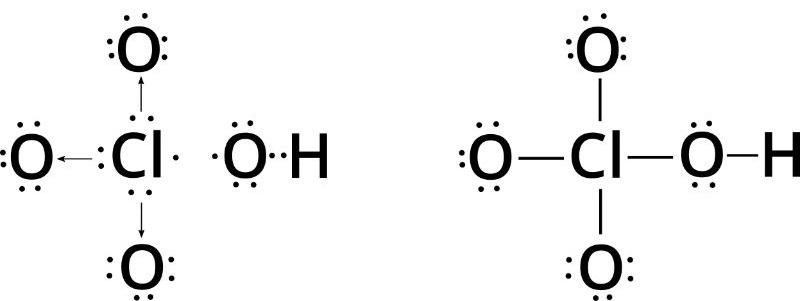
¿Qué es el ácido perclórico?
El ácido perclórico es un ácido que resulta de unir el óxido perclórico con H₂O. Es un ácido muy fuerte, usualmente encontrado como una solución acuosa incolora y sin olor, corrosiva para metales y tejidos. Su fórmula química es HClO4.
Es un potente oxidante cuando está caliente, pero sus soluciones acuosas (hasta aproximadamente el 70% en peso) a temperatura ambiente son generalmente seguras, mostrando solamente características ácidas fuertes y sin propiedades oxidantes.
El ácido perclórico y sus sales (particularmente perclorato de amonio [NH4ClO4], perclorato de sodio [NaClO4], y perclorato de potasio [KClO4]), encuentran muchas aplicaciones debido a su fuerte poder oxidante.
Su producción ha aumentado debido a su uso como material de partida para la producción de perclorato de amonio puro, un ingrediente básico de explosivos y propulsores sólidos para cohetes y misiles.
El ácido perclórico también se utiliza, a escala limitada, como reactivo con fines analíticos. Sus envases contenedores cerrados pueden romperse violentamente bajo exposición prolongada al calor.
Características del ácido perclórico
- Apariencia: líquido incoloro.
- Olor: inodoro.
- Peso molecular: 100.454 g/mol.
- Punto de ebullición: 19 °C.
- Punto de fusión: -112 °C.
- Densidad: 1.768 g/cm³.
- Solubilidad en agua: miscible.
- Acidez (pKa): -15.2 (±2.0).
- El ácido perclórico pertenece al grupo de los ácidos oxidantes fuertes.
Inflamabilidad
- Los ácidos oxidantes fuertes generalmente no son inflamables, pero pueden acelerar la combustión de otros materiales proporcionando oxígeno (actuando como agentes oxidantes).
- Las soluciones de ácido perclórico pueden explotar por efecto del calor o la contaminación.
- Cuando se calientan por encima de 160 °C, o se involucran en un incendio, pueden descomponerse explosivamente.
- Pueden reaccionar explosivamente con hidrocarburos (combustibles). Pueden encender combustibles (madera, papel, aceite, ropa, etc.).
- Los contenedores pueden explotar cuando se calientan.
- La escorrentía puede crear peligro de incendio o explosión.
Reactividad
- Los ácidos oxidantes fuertes generalmente son solubles en agua con la liberación de iones hidrógeno. Las soluciones resultantes tienen pH de 1 o cerca de 1.
- Los materiales de este grupo reaccionan con bases químicas (por ejemplo: aminas e hidróxidos inorgánicos) para formar sales. Estas reacciones de neutralización se producen cuando la base acepta iones de hidrógeno que el ácido dona.
- Las neutralizaciones pueden generar cantidades peligrosamente grandes de calor en espacios pequeños.
- La adición de agua a los ácidos a menudo genera suficiente calor en la pequeña región de la mezcla, como para hacer hervir dicha parte del agua explosivamente, pudiendo producirse salpicaduras de ácido muy peligrosas.
- Estos materiales tienen una capacidad significativa como agentes oxidantes, pero esa capacidad varía entre uno y otro.
- Pueden reaccionar con metales activos (como el hierro y aluminio) y también con muchos metales menos activos, para disolver el metal y liberar hidrógeno y/o gases tóxicos.
- Sus reacciones con sales de cianuro y sus compuestos liberan cianuro de hidrógeno gaseoso.
- También se generan gases inflamables y/o tóxicos por sus reacciones con ditiocarbamatos, isocianatos, mercaptanos, nitruros, nitrilos, sulfuros y agentes reductores débiles o fuertes.
- Se producen reacciones adicionales generadoras de gas con sulfitos, nitritos, tiosulfatos (para dar H2S y SO3), ditionitos (SO2) e incluso carbonatos: el dióxido de carbono, gas de la última, no es tóxico, pero el calor y las salpicaduras de la reacción pueden ser molesto.
- Pueden reaccionar vigorosamente o detonar, cuando se mezcla con materiales oxidables (alcoholes, aminas, boranos, dicianógeno, hidrazinas, hidrocarburos, hidrógeno, nitroalcanos, metales en polvo, silanos y tioles, entre otros).
- El ácido perclórico se enciende al contacto con cloruro de sulfinilo.
Toxicidad
- Los ácidos oxidantes fuertes son corrosivos para los tejidos. Los vapores de ácido irritan los tejidos sensibles (como los ojos y el sistema respiratorio) severamente.
- La inhalación, ingestión o contacto (de la piel, los ojos, etc.) con las soluciones de ácido perclórico o con sus vapores puede causar lesiones graves, quemaduras o la muerte.
- Al entrar en contacto con el fuego pueden producir gases irritantes, corrosivos y/o tóxicos.
- La escorrentía del control de incendios o del agua de dilución puede causar contaminación.
Usos
- El ácido perclórico se utiliza en las áreas de investigación científica y desarrollo, y en la fabricación de productos químicos y equipos eléctricos, electrónicos y ópticos.
- Es usado como precursor en la producción de perclorato de amonio puro, un ingrediente básico de explosivos y propulsores sólidos para cohetes y misiles.
- Los usos del ácido perclórico en el hogar incluyen limpiadores de inodoros, de metal y de desagües, removedores de óxido, en baterías y como imprimación para uñas postizas.
- Los usos industriales incluyen: refinación de metales, plomería, blanqueo, grabado, galvanoplastia, fotografía, desinfección, municiones, fabricación de fertilizantes, limpieza de metales y remoción de óxido.
- El ácido perclórico también se utiliza, a escala limitada, como reactivo con fines analíticos.
Efectos clínicos
- Los ácidos causan necrosis por coagulación. Los iones de hidrógeno desecan las células epiteliales, causando edema, eritema, desprendimiento de tejido y necrosis, con formación de úlceras y escaras.
- En la exposición a estos ácidos por la vía gastrointestinal, los pacientes pueden desarrollar quemaduras de grado II (ampollas superficiales, erosiones y ulceraciones) que corren el riesgo de sufrir una posterior formación de estenosis, en particular la vía gástrica y el esófago.
- También se pueden desarrollar quemaduras profundas y necrosis de la mucosa gastrointestinal. Las complicaciones a menudo incluyen perforación (esofágica, gástrica, rara vez duodenal), formación de fístulas (traqueoesofágico, aortoesofágico) y hemorragia gastrointestinal.
- La exposición por inhalación puede causar disnea, dolor torácico pleurítico, tos y broncoespasmo, edema de las vías respiratorias superiores y quemaduras. El edema de las vías respiratorias superiores es común y a menudo amenaza la vida.
- La exposición ocular puede producir severa irritación conjuntival y quemosis, defectos epiteliales de la córnea, isquemia límbica, pérdida permanente de la visión y, en casos graves, de perforación.
- La exposición de la dérmica leve puede causar irritación y quemaduras de grosor parcial. Una exposición más prolongada o de alta concentración puede causar quemaduras de grosor completo.
- Las complicaciones pueden incluir celulitis, sepsis, contracturas, osteomielitis y toxicidad sistémica.
Seguridad y riesgos
Declaraciones de peligro del Sistema Globalmente Armonizado de clasificación y etiquetado de productos químicos (SGA)
El Sistema Globalmente Armonizado de clasificación y etiquetado de productos químicos (SGA) es un sistema acordado internacionalmente, creado por las Naciones Unidas y diseñado para reemplazar las diversas normas de clasificación y etiquetado utilizadas en diferentes países mediante el uso de criterios coherentes a nivel mundial.
Las clases de peligro (y su correspondiente capítulo del SGA), las normas de clasificación y etiquetado, y las recomendaciones para el ácido perclórico son las siguientes:
Declaraciones de peligro del GHS
H271: Puede causar fuego o explosión; Oxidante fuerte [Peligro Líquidos oxidantes; Sólidos comburentes – Categoría 1].
H290: Puede ser corrosivo para metales [Advertencia Corrosivo para Metales – Categoría 1].
H302: Nocivo por ingestión [Advertencia Toxicidad aguda, oral – Categoría 4].
H314: Provoca quemaduras graves en la piel y lesiones oculares [Peligro Corrosión / irritación cutáneas – Categoría 1A, B, C].
H318: Provoca lesiones oculares graves [Peligro Lesiones oculares graves / irritación ocular – Categoría 1].
H371: Puede causar daño a los órganos [Advertencia Toxicidad específica en órganos diana, exposición única – Categoría 2].
Referencias
- Perchloric acid. Brief Profile. Recuperado de echa.europa.eu.
- Ácido perclórico. Recuperado de es.wikipedia.org.
- Perchloric acid. Recuperado de es.wikipedia.org.