
¿Qué son las ciclooxigenasas?
Las ciclooxigenasas (COX) son enzimas esenciales, catalizadoras de la producción de prostaglandinas, tromboxanos y otras sustancias a partir del ácido araquidónico.
Las ciclooxigenasas son enzimas bifuncionales, pues tienen dos actividades catalíticas distintas: una actividad ciclooxigenasa y otra peroxidasa, que les permiten catalizar la bis-oxigenación y la reducción del ácido araquidónico para formar prostaglandina.
No se han encontrado en plantas, insectos o en organismos unicelulares, pero en las células de los vertebrados estas enzimas se localizan principalmente en la membrana del retículo endoplásmico, habiendo reportes de su presencia en la envuelta nuclear, cuerpos lipídicos, mitocondrias, estructuras filamentosas, vesículas, etc.
Las primeras detecciones de los productos sintetizados por las ciclooxigenasas fueron hechas en fluidos seminales, por lo que inicialmente se pensó que se trataba de sustancias producidas en la próstata, de allí la denominación de “prostaglandinas”.
Hoy en día se sabe que las prostaglandinas son sintetizadas en todos los tejidos de los animales vertebrados e incluso en organismos que no poseen glándulas prostáticas, y que los diferentes isómeros de estas moléculas tienen diversas funciones en distintos procesos fisiológicos y patológicos, como fiebre, sensibilidad al dolor o algesia, inflamación, trombosis, mitogénesis, vasodilatación y vasoconstricción, ovulación, función renal, etc.
Tipos de ciclooxigenasas
Las ciclooxigenasas (COX), como ya se mencionó, son enzimas clave en el metabolismo del ácido araquidónico, responsables de la síntesis de prostaglandinas, prostaciclinas y tromboxanos, moléculas implicadas en la inflamación, la fiebre, el dolor y la hemostasia. Existen principalmente tres tipos:
- COX-1. Es una enzima constitutiva, siempre presente en muchos tejidos. Tiene funciones fisiológicas “de mantenimiento”, como protección de la mucosa gástrica, regulación del flujo sanguíneo renal, o producción de tromboxano A₂ (importante en la agregación plaquetaria).
- COX-2. Es una enzima inducible, expresada sobre todo en procesos inflamatorios. Se activa en respuesta a citoquinas, factores de crecimiento y estímulos inflamatorios. Su función principal es mediar la síntesis de prostaglandinas proinflamatorias. Por eso, los antiinflamatorios selectivos de COX-2 (como celecoxib) se diseñaron para disminuir inflamación y dolor con menor daño gástrico.
- COX-3 (variante de COX-1). Es una isoforma descrita en el sistema nervioso central, aunque su papel exacto en humanos todavía es controvertido. Se ha relacionado con la acción de fármacos como el paracetamol, que no inhibe de forma potente COX-1 ni COX-2, pero sí podría actuar sobre esta variante.
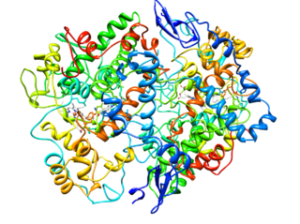
A partir del análisis de sus estructuras se ha determinado que las enzimas COX-1 y COX-2 poseen en su extremo N-terminal y en el sitio adyacente al péptido señal, un “módulo” único de factor de crecimiento epidérmico (EGF, del inglés Epidermal Growth Factor).
En este módulo se encuentran unos enlaces o puentes disulfuro sumamente conservados, que funcionan como “dominio de dimerización” entre los dos polipéptidos de cada enzima homodimérica.
Las proteínas también poseen unas hélices anfipáticas que les facilitan el anclaje a una de las capas de la membrana. Además, el dominio catalítico de ambas tiene dos sitios activos, uno con actividad ciclooxigenasa y otro con actividad peroxidasa.
Ambas enzimas son proteínas sumamente conservadas, encontrándose entre diferentes especies diferencias poco significativas respecto a los mecanismos de dimerización y unión a la membrana, así como también de algunas características de sus dominios catalíticos.
Las proteínas COX tienen, adicionalmente, sitios de glicosilación, esenciales para su funcionamiento y que están absolutamente conservados.
Reacción de las ciclooxigenasas
Las enzimas ciclooxigenasas 1 y 2 se encargan de catalizar los dos primeros pasos de la biosíntesis de prostaglandinas, los cuales comienzan con la conversión del ácido araquidónico en precursores de las prostaglandinas, conocidos como hidroperoxi-endoperóxido PGG2.
Para que estas enzimas puedan ejercer sus funciones, deben ser primero activadas a través de un proceso dependiente de su actividad peroxidasa. En otras palabras, su actividad principal depende de la reducción de un sustrato peróxido (mediada por el sitio activo peroxidasa) para que ocurra la oxidación del hierro asociado al grupo hemo que le sirve como cofactor.
La oxidación del grupo hemo provoca la formación de un radical tirosil en el sitio activo ciclooxigenasa, lo que activa la enzima y promueve la iniciación de la reacción ciclooxigenasa. Esta reacción de activación puede ocurrir una sola vez, pues el radical tirosil es regenerado durante la última reacción de la ruta.
Inhibidores de las ciclooxigenasas
Las ciclooxigenasas están implicadas en la síntesis de las prostaglandinas, que son hormonas con funciones en la protección de la mucosa intestinal, en la agregación de las plaquetas y en la regulación de la función renal, además de participar en los procesos de inflamación, dolor y fiebre.
En vista de que estas enzimas son claves para la producción de dichas hormonas, especialmente de aquellas que tienen que ver con los procesos inflamatorios, numerosos estudios farmacológicos se han enfocado en la inhibición de las ciclooxigenasas.
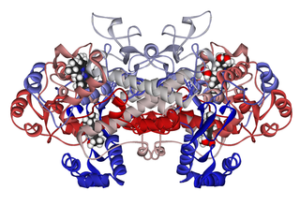
Así, se ha demostrado que el mecanismo de acción de muchas drogas antiinflamatorias no esteroideas tiene que ver con la acetilación irreversible o reversible (inhibitoria) del sitio activo ciclooxigenasa en estas enzimas.
Entre estas drogas se encuentran piroxicam, ibuprofeno, aspirina, flurbiprofeno, diclofenac, naproxeno y otras.
Referencias
- Botting, R. M. Inhibitors of cyclooxygenases: mechanisms, selectivity and uses. Journal of physiology and pharmacology.
- Fitzpatrick, F. A. Cyclooxygenase enzymes: regulation and function. Current pharmaceutical design.
- Kundu, N., Smyth, M. J., Samsel, L., Fulton, A. M. Cyclooxygenase inhibitors block cell growth, increase ceramide and inhibit cell cycle. Breast cancer research and treatment.
- Rouzer, C. A., Marnett, L. J. Cyclooxygenases: structural and functional insights. Journal of lipid research.
- Vane, J. R., Bakhle, Y. S., Botting, R. M. CYCLOOXYGENASES 1 AND 2. Annual review of pharmacology and toxicology.