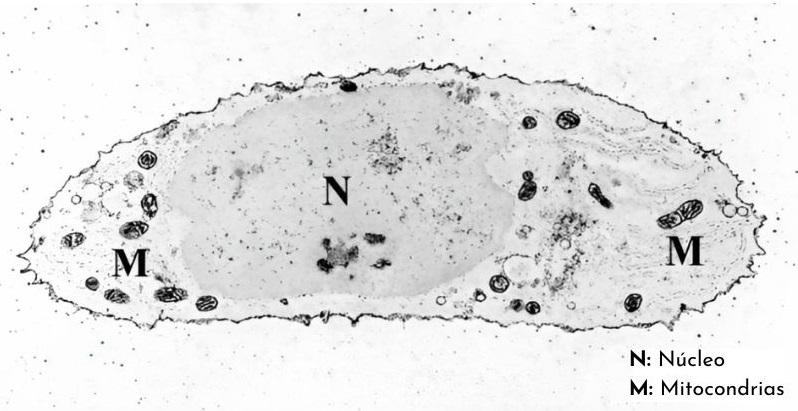
¿Qué es la citoquímica?
La citoquímica es la rama de la citología que estudia la identificación y disposición de ciertas sustancias específicas en el interior de la célula. Esta rama de la biología celular combina la morfología de la célula con la estructura química.
La finalidad de la citoquímica es descubrir la organización química de las células para comprender los misterios de la vida, y estudiar los cambios dinámicos que ocurren durante los distintos estadios funcionales. De esta manera es posible determinar el papel metabólico que cumplen estas sustancias dentro de la célula.
La citoquímica utiliza dos métodos principales. El primero se basa en procedimientos químicos y físicos. Estas técnicas recurren al microscopio como instrumento indispensable para visualizar las reacciones químicas ocurridas sobre sustancias específicas dentro de la célula. Ejemplo: el uso de colorantes citoquímicos, como la reacción de Feulgen o reacción de PAS, entre otras.
El segundo método se fundamenta en la bioquímica y en la microquímica. Con esta metodología es posible determinar cuantitativamente la presencia de sustancias químicas intracelulares.
Entre las sustancias que se pueden evidenciar en un tejido o estructura celular están los siguientes: proteínas, ácidos nucleicos, polisacáridos y lípidos.
Historia de la citoquímica
Las técnicas citoquímicas han ayudado a comprender la composición de las células, y a través del tiempo han surgido una variedad de técnicas que utilizan diversos tipos de colorantes con afinidades y fundamentos disímiles.
Posteriormente, la citoquímica abrió nuevos horizontes con el uso de determinados sustratos para evidenciar colorimétricamente la presencia de enzimas u otras moléculas dentro de la célula.
Asimismo, han surgido otras técnicas, como la inmunocitoquímica, que ha sido de gran ayuda para el diagnóstico de muchas enfermedades. La inmunocitoquímica se basa en reacciones antígeno-anticuerpo.
Por otra parte, la citoquímica también ha utilizado sustancias fluorescentes denominadas fluorocromos, excelentes marcadores para la detección de ciertas estructuras celulares. Debido a las características del fluorocromo, destaca las estructuras a las que se ha fijado.
¿Qué estudia la citoquímica?
Las diversas técnicas citoquímicas utilizadas sobre una muestra biológica tienen en común poner en evidencia la presencia de un tipo específico de sustancia y conocer su localización dentro de la estructura biológica en evaluación, bien sea un tipo celular o un tejido.
Estas sustancias pueden ser enzimas, metales pesados, lípidos, glucógeno y grupos químicos definidos (aldehídos, tirosina, etc.).
La información aportada por estas técnicas puede orientar no solo para identificar células, sino también para diagnosticar diversas patologías. Por ejemplo, las tinciones citoquímicas son muy útiles para diferenciar entre los diversos tipos de leucemias, ya que algunas células expresan ciertas enzimas o sustancias claves y otras no.
Por otra parte, cabe destacar que para que sea posible el uso de la citoquímica se deben tomar las siguientes consideraciones:
- La sustancia debe ser inmovilizada en el lugar donde se encuentra naturalmente.
- La sustancia debe identificarse usando sustratos que reaccionan de forma específica con ella y no con otros compuestos.
Utilidad de la citoquímica
Las muestras que pueden ser estudiadas a través de las técnicas citoquímicas son:
- Extendidos de sangre periférica.
- Extendidos de médula ósea.
- Tejidos fijados para técnicas de histoquímica.
- Células fijadas por citocentrifugación.
Las técnicas citoquímicas son de gran apoyo en el área de hematología, pues se utilizan frecuentemente para ayudar en el diagnóstico y diferenciación de ciertos tipos de leucemias. Por ejemplo: las reacciones de esterasas sirven para diferenciar entre una leucemia mielomonocítica de una leucemia monocítica aguda.
Los frotis de médula ósea y sangre periférica de estos pacientes se parecen, pues algunas células son difíciles de identificar solo desde el punto de vista morfológico. Para ello se realiza la prueba de esterasa.
En la primera dan positivas las esterasas específicas, mientras que en la segunda dan positivas las esterasas inespecíficas.
También son de gran utilidad en histología, ya que, por ejemplo, la técnica de coloración con metales pesados (impregnación argéntica), tiñe las fibras reticulares de color marrón intenso en el tejido miocárdico.
Técnicas en citoquímica
Estas son las técnicas más usadas:
- Uso de colorantes. Los colorantes utilizados son muy diversos en las técnicas citoquímicas, y estos pueden clasificarse según varios puntos de vista:
- De acuerdo al radical por el que tienen afinidad. Se dividen en ácidos, básicos o neutros. Son los más sencillos y los más utilizados, permitiendo distinguir los componentes basófilos de los acidófilos. Ejemplo: la coloración hematoxilina-eosina. En este caso, los núcleos de las células se tiñen de azul (toman la hematoxilina, que es el colorante básico) y los citoplasmas de rojo (toman la eosina, que es el colorante ácido).
- Según el color que proporcionan. Pueden ser ortocromáticos o metacromáticos. Los ortocromáticos tiñen las estructuras del mismo color que posee el colorante. Por ejemplo, el caso de la eosina, cuyo color es rojo y tiñe de rojo. Los metacromáticos, en cambio, tiñen las estructuras de un color diferente al suyo, como la toluidina, cuyo color es azul y tiñe de violeta.
- Colorantes vitales o supravitales. Son colorantes inocuos, es decir, colorean las células y estas se mantienen vivas. A estos colorantes se les llama vitales (ej: el azul de tripán para teñir macrófagos) o supravitales (ej: el verde de Janus para teñir mitocondrias o el rojo neutro que tiñe los lisosomas).
- Detección de lípidos por medio de colorantes liposolubles
- Tetróxido de osmio. Tiñe los lípidos (ácidos grasos no saturados) de negro. Esta reacción puede observarse con el microscopio óptico, pero debido a que este colorante es de alta densidad también puede visualizarse con microscopio electrónico.
- Sudán III. Es uno de los más utilizados. Este colorante se difunde y solubiliza en los tejidos, acumulándose en el interior de las gotas de lípido. El color es rojo escarlata.
- Tinción de Sudán negro B. Produce mejor contraste que los anteriores debido a que es capaz de disolverse también en los fosfolípidos y en el colesterol. Es útil para detectar gránulos azurófilos y específicos de los granulocitos maduros y de sus precursores. Por tanto, identifica las leucemias mieloides.
- Tinción de grupos aldehídos (tinción del ácido peryódico de Schiff). La tinción de ácido peryódico de Schiff puede detectar tres tipos de grupos aldehídos. Ellos son:
- Reacción del PAS. Esta tinción detecta ciertos tipos de carbohidratos, como por ejemplo, el glucógeno. El ácido peryódico de Schiff rompe los enlaces C-C de los carbohidratos debido a la oxidación de los grupos glicólicos 1-2, logrando liberar grupos aldehídos. Los grupos de aldehídos libres reaccionan con el reactivo de Schiff y forman un compuesto rojo púrpura. La aparición del rojo púrpura evidencia una reacción positiva. Esta prueba da positiva en células vegetales, detectando almidón, celulosa, hemicelulosa y peptinas. Mientras que en células animales detecta mucinas, mucoproteínas, ácido hialurónico y quitina. Además, es útil en el diagnóstico de leucemias linfoblásticas o eritroleucemia, entre otras patologías del tipo mielodisplásicas. En el caso de hidratos de carbono ácidos se puede utilizar la tinción de azul alcián. La prueba es positiva si se observa un color celeste/turquesa.
- Reacción plasmal. La reacción plasmal pone en evidencia la presencia de ciertos aldehídos alifáticos de cadena larga, como el palmital y el estearal. Esta técnica se aplica sobre cortes histológicos congelados. Se trata de forma directa con el reactivo de Schiff.
- Reacción de Feulgen. Esta técnica detecta la presencia de ADN. La técnica consiste en someter el tejido fijado a una hidrólisis ácida débil para posteriormente hacerlo reaccionar con el reactivo de Schiff. La hidrólisis deja expuestos los grupos aldehídos de la desoxirribosa a nivel de la unión desoxirribosa-purina. Luego, el reactivo de Schiff reacciona con los grupos aldehídos que quedaron libres. Esta reacción da positiva en los núcleos y negativa en los citoplasmas de las células. La positividad se evidencia por la presencia de color rojo. Si esta técnica se combina con el verde de metilo-pironina es posible detectar de forma simultánea el ADN y el ARN.
- Tinciones citoquímicas para estructuras proteicas. Para ello se puede utilizar la reacción de Millon, donde se utiliza como reactivo el nitrato de mercurio. Las estructuras que contengan aminoácidos aromáticos se teñirán de rojo.
- Tinciones citoquímicas que utilizan sustratos para evidenciar la presencia de enzimas. Estas tinciones se basan en la incubación de la muestra biológica con un sustrato determinado y el producto de la reacción reacciona posteriormente con sales diazoicas para formar un complejo coloreado.
- Esterasas. Estas enzimas están presentes en los lisosomas de algunas células hemáticas y son capaces de hidrolizar los ésteres orgánicos liberando naftol. Este último forma un azocolorante insoluble cuando se une a una sal diazoica, tiñendo el lugar donde ocurre la reacción. Existen varios sustratos, y dependiendo cuál se use se pueden identificar esterasas específicas y esterasas inespecíficas. Las primeras están presentes en las células inmaduras de la serie mieloide, y las segundas en las células de origen monocíticas. El sustrato utilizado para la determinación de esterasas específicas es el naftol-AS-D cloroacetato. Para la determinación de esterasas inespecíficas se pueden usar varios sustratos, como el naftol AS-D acetato, el alfa naftil acetato y el alfa naftil butirato. En ambos casos, las células se teñirán de rojo intenso cuando la reacción sea positiva.
- Mieloperoxidasa. Esta enzima se encuentra en los gránulos azurófilos de las células granulocíticas y de los monocitos. Su detección se utiliza para diferenciar las leucemias de origen mieloide de las linfoides. Las células que contienen mieloperoxidasas se colorean de amarillo ocre.
- Fosfatasas. Estas enzimas liberan ácidos fosfóricos de distintos sustratos. Se diferencian entre sí de acuerdo a la especificidad del sustrato, el pH y la acción de inhibidores e inactivadores. Entre las más conocidas están las fosfomonoesterasas que hidrolizan ésteres simples (P-O). Ejemplo: la fosfatasa alcalina y la fosfatasa ácida, así como las fosfamidasas que hidrolizan las uniones (P-N). Se usan para diferenciar síndromes linfoproliferativos y para diagnosticar tricoleucemia.
- Coloraciones tricrómicas
- Tricrómico de Mallary-Azan. Son útiles para diferenciar el citoplasma de las células de las fibras del tejido conectivo. Las células se tiñen de rojo y las fibras colágenas de azul.
- Tricrómico de Masson. Esta tiene la misma utilidad que la anterior pero, en este caso, las células se tiñen de rojo y las fibras colágenas de verde.
- Colorantes que tiñen organelos específicos
- Verde de Janus. Tiñe selectivamente las mitocondrias.
- Sales de plata y ácido ósmico. Tiñe el aparato de Golgi.
- Azul de toluidina. Tiñe los cuerpos de Nissi.
- Sales de plata y PAS. Tiñen las fibras reticulares y la lámina basal.
- Orceína y fucsina resorcina. Tiñen las fibras elásticas. Con la primera se tiñen de color café y con la segunda, de azul o morado intenso.
- Otras técnicas utilizadas en citoquímica
- Uso de sustancias fluorescentes o fluorocromos. Existen técnicas que utilizan sustancias fluorescentes para estudiar la localización de una estructura en una célula. Estas reacciones se visualizan con microscopios especiales, llamados de fluorescencia. Ejemplo: técnica de IFI (Inmunofluorescencia indirecta).
- Detección de componentes celulares mediante inmunocitoquímica. Estas técnicas son de gran utilidad en medicina, ya que ayudan a detectar cierta estructura celular y también la cuantifica. Se basa en una reacción antígeno-anticuerpo. Por ejemplo: las técnicas de ELISA (Enzima Inmuno Ensayo).
Recomendaciones en citoquímica
- Es necesario usar frotis controles para evaluar el buen funcionamiento de los colorantes.
- Se debe usar frotis frescos para someterlos a coloraciones citoquímicas. De no ser posible, se deben mantener protegidos de la luz y conservados a 4 °C.
- Se debe cuidar que el fijador utilizado no influya negativamente sobre la sustancia a investigar. Es decir, evitar que este sea capaz de extraerla o inhibirla.
- Se debe respetar el tiempo de uso de los fijadores, pues por lo general solo debe durar segundos, ya que exponer el frotis más tiempo al fijador puede dañar algunas enzimas.
Referencias
- Citoquímica. Recuperado de es.wikipedia.org.
- Villarroel, P., de Suárez, C. Métodos de Impregnación Metálica para el Estudio de las Fibras Reticulares Miocárdicas: Estudio comparativo. Recuperdo de scielo.org.
- Santana, A., Lemes, A., Bolaños, B., Parra, A., Martín, M., Molero, T. Citoquímica de la fosfatasa ácida: Consideraciones metodológicas. Rev. Diagn. Biol.
- De Robertis, E., De Robertis, M. Biología celular y molecular. 11 va edición. Editorial Ateneo.
- Herramientas clásicas para el estudio en biología celular. Recuperado de dbbe.fcen.uba.ar.