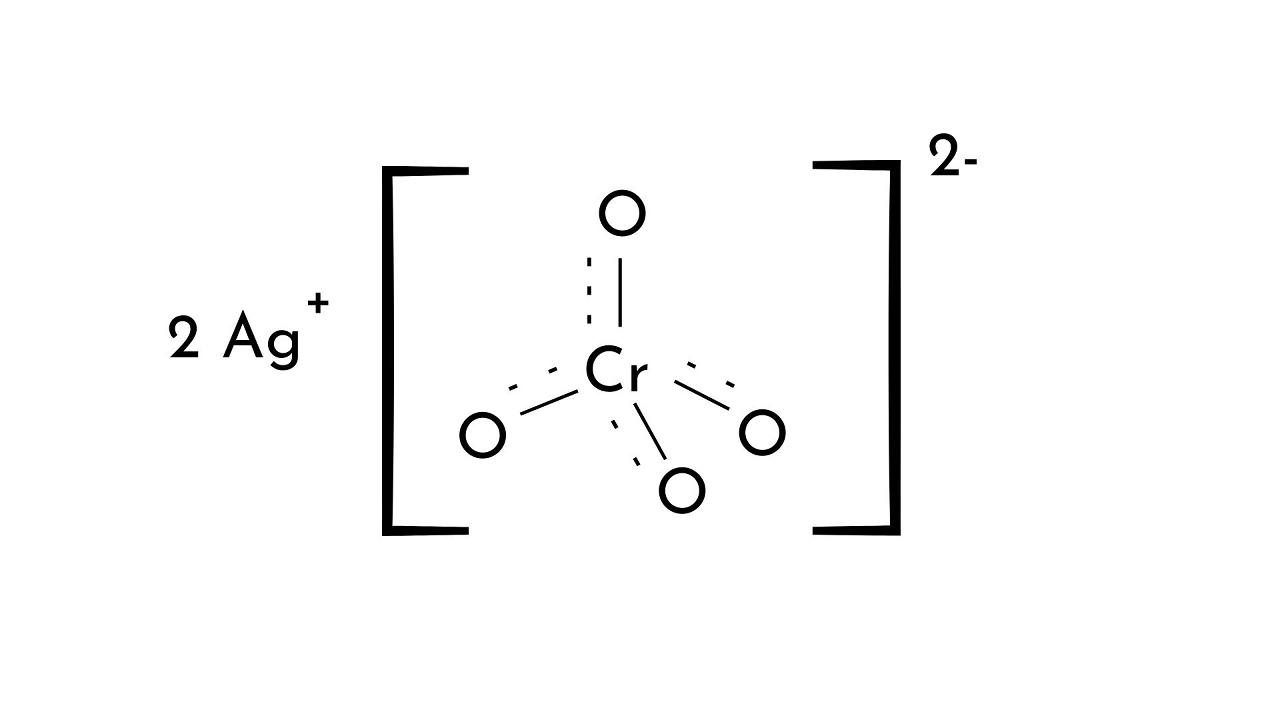
¿Qué es el cromato de plata?
El cromato de plata es un compuesto químico de fórmula Ag2CrO4. Es uno de los compuestos de cromo en estado de oxidación (VI) y se dice que es el precursor de la fotografía moderna.
La preparación del compuesto es sencilla. Se produce mediante una reacción de intercambio con una sal de plata soluble, como la que existe entre el cromato de potasio y el nitrato de plata.
2AgNO3(aq) + Na2CrO4(aq) →Ag2CrO4(s) + 2NaNO3(aq)
Casi todos los compuestos de metales alcalinos y nitratos son solubles, pero la mayoría de los compuestos de plata son insolubles (excepto los acetatos, percloratos, cloratos y nitratos).
Por lo tanto, cuando se mezclan las sales solubles nitrato de plata y cromato de sodio, forma cromato de plata insoluble y precipita.
Propiedades físicas y químicas del cromato de plata
El cromato de plata son cristales monoclínicos de color rojo o marrón sin olor o sabor característicos.
El compuesto tiene un peso molecular de 331,73 g/mol y una densidad de 5,625 g/ml. Posee un punto de 1.550 °C y es muy poco soluble en agua y soluble en ácido nítrico y amoniaco.
Como todos los compuestos de cromo (VI), el cromato de plata es un fuerte agente oxidante. Pueden reaccionar con los agentes reductores para generar calor y productos que pueden ser gaseosos (causando la presurización de los recipientes cerrados).
Los productos pueden ser capaces de otras reacciones, como la combustión en el aire. La reducción química de los materiales en este grupo puede ser rápida o incluso explosiva, pero a menudo requiere de iniciación.
Reactividad y peligros
El cromato de plata es un oxidante fuerte, higroscópico (que absorbe la humedad del aire) y es sensible a la luz. Las mezclas explosivas de agentes oxidantes inorgánicos con agentes reductores a menudo permanecen inalteradas durante largos períodos si se evita la iniciación.
Tales sistemas son típicamente mezclas de sólidos, pero pueden implicar cualquier combinación de estados físicos. Algunos agentes oxidantes inorgánicos son sales de metales solubles en agua.
Como todos los compuestos de cromo (VI), el cromato de plata es cancerígeno para humanos, además de ser irritante en caso de contacto con la piel o de ingestión.
Aunque menos peligroso, hay que prevenir en caso de contacto con la piel (corrosivo), de contacto con los ojos (irritante), e inhalación. La exposición prolongada puede causar quemaduras en la piel y ulceraciones. La sobreexposición por inhalación puede causar irritación respiratoria.
Si el compuesto entra en contacto con los ojos, se debe revisar y quitar los lentes de contacto, si se tienen. Se deben lavar inmediatamente los ojos con abundante agua fría durante al menos 15 minutos.
En caso de contacto con la piel, se debe enjuagar inmediatamente el área afectada con abundante agua durante al menos 15 minutos mientras se quita la ropa contaminada y los zapatos.
Hay que cubrir la piel irritada con una loción emoliente. Lavar la ropa y zapatos antes de volver a usarlos. Si el contacto es grave, lavar con un jabón desinfectante y cubrir la piel contaminada con una crema antibacteriana.
En caso de inhalación, se debe trasladar a la víctima a un lugar fresco. Si no respira, se administra respiración artificial. Si la respiración es difícil, proporcionar oxígeno.
Si el compuesto se ingiere, no se debe inducir el vómito a menos que lo indique el personal médico. Aflojar la ropa apretada, como cuello de camisa, cinturón o corbata.
En todos los casos se debe obtener atención médica de inmediato.
Usos del cromato de plata
Reactivo en el método de Mohr
El cromato de plata es empleado como reactivo para indicar el punto final en el método de Mohr de argentometría. La reactividad del anión cromato con plata es menor que los haluros (cloruro y otros). Así, en una mezcla de ambos iones se formará cloruro de plata.
Solo cuando no se deje ningún cloruro (o cualquier halógeno) se formará cromato de plata (rojo-marrón) y precipitará.
Antes del punto final, la solución tiene un aspecto amarillo limón lechoso, debido al color del ion cromato y al precipitado de cloruro de plata ya formado. Al acercarse al punto final, las adiciones de nitrato de plata llevan a una progresiva disminución de coloraciones rojas.
Cuando permanezca el color pardo rojizo (con manchas grisáceas de cloruro de plata en el mismo) se alcanza el punto final de la titulación. Esto es para pH neutro.
En pH muy ácido, el cromato de plata es soluble, y en pH alcalino la plata precipita como hidróxido.
Teñido celular
La reacción de formación de cromato de plata ha sido importante en la neurociencia, ya que se utiliza en el método de Golgi de tinción de las neuronas para la microscopía: el cromato de plata producido precipita dentro de las neuronas y hace que su morfología sea visible.
El método de Golgi es una técnica de tinción de plata que se utiliza para visualizar el tejido nervioso bajo microscopía óptica y electrónica. El método fue descubierto por Camillo Golgi, un médico y científico italiano, que publicó la primera fotografía realizada con la técnica en 1873.
La tinción de Golgi fue utilizada por el neuroanatomista español Santiago Ramón y Cajal (1852-1934) para descubrir una serie de hechos novedosos sobre la organización del sistema nervioso, inspirando el nacimiento de la doctrina neuronal.
Además, Ramón y Cajal mejoró la técnica utilizando un método que él denominó “doble impregnación”. La técnica de tinción de Ramón y Cajal, todavía en uso, se llama Mancha de Cajal.
Estudio de nanopartículas
Se han sintetizado microcristales de Ag2CrO4 usando el método de coprecipitación.
Estos microcristales se caracterizaron por difracción de rayos X (XRD) con análisis de Rietveld, microscopía electrónica de barrido por emisión de campo (FE-SEM), microscopía electrónica de transmisión (TEM) con espectroscopia de dispersión de energía (EDS), micro-Raman.
Las micrografías FE-SEM y TEM revelaron la morfología y el crecimiento de nanopartículas de Ag sobre microcristales de Ag2CrO4 durante la irradiación con haz de electrones.
Los análisis teóricos basados en el nivel de teoría funcional de la densidad indican que la incorporación de electrones es responsable de las modificaciones estructurales y la formación de defectos en los cúmulos [AgO6] y [AgO4], generando condiciones ideales para el crecimiento de nanopartículas de Ag.
Otros usos
El cromato de plata es usado como agente de revelado para fotografía. También es usado como catalizador para la formación de aldol a partir de alcohol (Silver chromate (VI), S.F.) y como agente oxidante en distintas reacciones de laboratorio.
Referencias
- NILE CHEMICALS (S.F.). SILVER CHROMATE. Recuperado de nilechemicals.com.
- Across Organic. Material Safety Data Sheet Silver chromate, 99%. Recuperado de t3db.ca.