
¿Qué es el fluoruro de calcio?
El fluoruro de calcio es un sólido inorgánico formado por un átomo de calcio (Ca) y dos átomos de flúor (F). Su fórmula química es CaF2 y es un sólido blanco grisáceo cristalino.
En la naturaleza se encuentra en la fluorita o espato flúor. Existe de manera natural en los huesos y en los dientes. La fluorita es la principal fuente para obtener otros compuestos de flúor.
Además, el CaF2 se utiliza para prevenir caries en los dientes, por lo que se añade a materiales que usan los odontólogos para curarlas. De hecho, el fluoruro de calcio también se agrega al agua potable para que la población se beneficie al ingerirla y al cepillarse los dientes.
El CaF2 se utiliza en forma de cristales grandes en equipos ópticos y cámaras fotográficas. También se emplea en pequeños aparatos que sirven para detectar cuánto ha estado expuesta una persona a la radioactividad.
Estructura del fluoruro de calcio
El fluoruro de calcio CaF2 es un compuesto iónico formado por un catión calcio Ca2+ y dos aniones fluoruro F–. Sin embargo, algunas fuentes de información indican que sus enlaces poseen cierto carácter covalente.
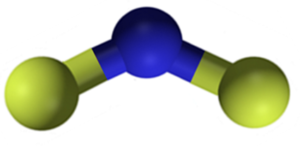
Propiedades del fluoruro de calcio
- Estado físico. Sólido incoloro a blanco grisáceo con estructura cristalina cúbica.
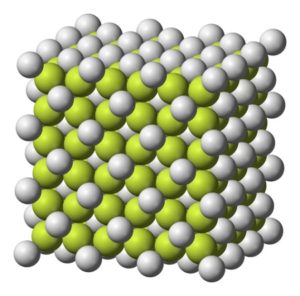
- Peso molecular. 78,07 g/mol.
- Punto de fusión. 1418 °C.
- Punto de ebullición. 2533 °C.
- Densidad. 3,18 g/cm3 a 20 °C.
- Índice de refracción. 1,4328.
- Solubilidad. Es insoluble en agua a 20 °C. Casi insoluble a 25 °C: 0,002 g/100 mL de agua. Ligeramente soluble en ácidos.
- Propiedades químicas. Sus propiedades oxidantes o reductoras son muy débiles, sin embargo, estas reacciones pueden ocurrir. Aunque, por lo general, en muy pocos casos. Es inerte a compuestos químicos orgánicos y a muchos ácidos, incluyendo el ácido fluorhídrico HF. Se disuelve lentamente en ácido nítrico HNO3. No es inflamable. No reacciona rápidamente con aire ni agua. Debido a su poca afinidad por el agua, aunque se exponga a un alto porcentaje de humedad, esta no lo afecta incluso hasta por un mes a temperatura ambiente normal. En presencia de humedad, las paredes de sus cristales se disuelven lentamente a temperaturas superiores a 600 °C. En ambientes secos se puede utilizar hasta unos 1000 °C sin verse afectado de forma apreciable.
Presencia del fluoruro de calcio en la naturaleza
El fluoruro de calcio CaF2 se encuentra de forma natural en el mineral fluorita o espato flúor.
Aunque el CaF2 puro es incoloro, la fluorita a menudo es coloreada por la presencia de electrones atrapados en los “huecos” de la estructura cristalina.
Este mineral es muy apreciado por su brillo vidrioso y variedad de colores (púrpura, azul, verde, amarillo, transparente, marrón, rosado, negro y naranja-rojizo). Se dice que es “el mineral más coloreado del mundo”.




El fluoruro de calcio se encuentra además en los huesos en cantidades entre 0,2 y 0,65%, y también en el esmalte de los dientes en un 0,33-0,59%.
Usos del fluoruro de calcio
- En la obtención de compuestos de flúor. La fluorita es la fuente básica o mayoritaria del flúor a nivel mundial. Es la materia prima para preparar casi todos los compuestos de flúor. El más importante de estos es el ácido fluorhídrico HF, a partir del cual se preparan los demás compuestos fluorados. El ion fluoruro F– se libera del mineral mediante la reacción de este con ácido sulfúrico concentrado H2SO4: CaF2 (sólido) + H2SO4 (líquido) → CaSO4 (sólido) + 2 HF (gas).
- En el cuidado de los dientes. El fluoruro de calcio CaF2 es un agente para la prevención de las caries. Se utiliza para fluorar aguas potables (aguas que se pueden beber) con dicho objetivo. Además, las bajas concentraciones de fluoruro F– (del orden de 0,1 partes por millón) que se emplean en pastas dentífricas y enjuagues bucales han demostrado tener un efecto positivo profundo en el cuidado dental preventivo de las caries.
- Nanopartículas de CaF2 más efectivas. A pesar de que se utilizan fluoruros en pastas dentales y enjuagues, la baja concentración de calcio (Ca) en la saliva hace que no se formen los depósitos de CaF2 en los dientes de la manera más efectiva posible. Por ello se ha ideado una forma de obtener polvo de CaF2 como nanopartículas. Para eso se utiliza un secador por rocío (del inglés spray-dryer) en donde dos soluciones (una de hidróxido de calcio Ca(OH)2 y una de fluoruro de amonio NH4F) se mezclan mientras son rociadas en una cámara con flujo de aire caliente. Entonces ocurre la siguiente reacción: Ca(OH)2 + NH4F → CaF2 (sólido) + NH4OH. El NH4OH se volatiliza como NH3 y H₂O y quedan las nanopartículas de CaF2. Estas presentan una alta reactividad y mayor solubilidad, lo que las hace más efectivas para la remineralización de los dientes y como anticaries.
- En lentes para equipos ópticos. El fluoruro de calcio se emplea para construir elementos ópticos como los prismas y ventanas de espectrofotómetros de luz infrarroja y ultravioleta (UV). Estos aparatos permiten medir la cantidad de luz absorbida por un material cuando esta pasa a través de él. El CaF2 es transparente en dichas regiones del espectro de luz, tiene un índice de refracción extremadamente bajo y permite obtener una resolución más eficiente que la del NaCl en el intervalo 1500-4000 cm–1. Gracias a su estabilidad química puede soportar condiciones adversas, por lo que los elementos ópticos de CaF2 no son atacados. Además, tiene una alta dureza.
- En cámaras fotográficas. Algunos fabricantes de cámaras fotográficas utilizan lentes de CaF2 cristalizado de forma artificial para reducir la dispersión de luz y lograr una excelente corrección de la distorsión de los colores.

- En la industria metalúrgica. El CaF2 se emplea como agente fundente en la industria metalúrgica, debido a que es una fuente de calcio insoluble en agua y, por lo tanto, efectiva en aplicaciones sensibles al oxígeno. Se usa para fundir y procesar de forma líquida el hierro y el acero. Esto se basa en que posee un punto de fusión similar al del hierro y además a que puede disolver óxidos y metales.
- En detectores de radioactividad o radiaciones peligrosas. El CaF2 es un material termoluminiscente. Esto significa que puede absorber radiaciones en los electrones de su estructura cristalina y posteriormente al ser calentado liberarla en forma de luz. Esta luz emitida se puede medir mediante una señal eléctrica, proporcional a la cantidad de radiación que recibió el material. Significa que, a mayor cantidad de radiación recibida, mayor será la cantidad de luz que emitirá después al ser calentado. Por ello, el CaF2 se usa en los llamados dosímetros personales, que son utilizados por personas que están expuestas a radiaciones peligrosas y se desea saber cuánta radiación han recibido en un período de tiempo.
- Otros usos
- Se usa como catalizador en reacciones químicas de deshidratación y deshidrogenación para la síntesis de compuestos orgánicos.
- Se emplea en electrodos alcalinos de soldadura. Se obtiene una soldadura más fuerte que con electrodos ácidos. Estos electrodos son útiles en la fabricación de barcos y de recipientes de acero para alta presión.
- Como suplemento alimenticio en cantidades extremadamente bajas (ppm o partes por millón).
Referencias
- Pirmoradian, M., Hooshmand, T. Remineralization and antibacterial capabilities of resin-based dental nanocomposites. Synthesis and characterization of calcium fluoride (CaF2). In Applications of Nanocomposite Materials in Dentistry. Recuperado de sciencedirect.com.
- Calcium fluoride. Recuperado de pubchem.ncbi.nlm.nih.gov.
- Weman, K. Manual metal arc (MMA) welding with coated electrodes. In Welding Processes Handbook (Second Edition). Recuperado de sciencedirect.com.
- Ropp, R.C. Group 17 (H, F, Cl, Br, I) Alkaline Earth Compounds. Calcium Fluoride. In Encyclopedia of the Alkaline Earth Compounds. Recuperado de sciencedirect.com.
- Cotton, F.A., Wilkinson, G. Advanced Inorganic Chemistry. Fourth Edition. John Wiley & Sons.