¿Qué es el óxido plumboso?
El óxido plumboso, óxido de plomo (II) o monóxido de plomo, es un compuesto químico de fórmula PbO. Se encuentra en dos polimorfos: el litargirio y la masicotita. En su composición, el litargirio es el producto oxidado de plomo fundido que se ha agitado o atomizado para incorporar aire, luego se enfrió y se molió para formar el polvo amarillo.
El nombre masicotita se usa tanto para el mineral nativo como para el producto de monóxido de plomo producido calentando carbonato de plomo a 300 °C.
La masicotita posee una estructura ortorrómbica, mientras que el litargirio tiene una estructura cristalina tetragonal. El óxido de plomo (II) tiene la capacidad de cambiar de estructura al calentarse o enfriarse.
El PbO se produce oxidando el plomo metálico. Se funde el metal para hacer tabletas del plomo, y después se muelen entre 170 ~ 210 °C y se pasa por la llama para la oxidación en temperaturas sobre 600 ℃. Los productos de óxido se trituran para obtener el óxido de plomo terminado.
2Pb + O2 → 2PbO
El PbO se produce a gran escala como producto intermedio en el refinado de los minerales de plomo en plomo metálico. El mineral de plomo que se emplea es la galena (sulfuro de plomo (II)). A alta temperatura (1000 °C) el sulfuro se convierte en el óxido de la siguiente forma:
2PbS + 3O2 → 2PbO + 2SO2
Propiedades físicas y químicas del óxido plumboso
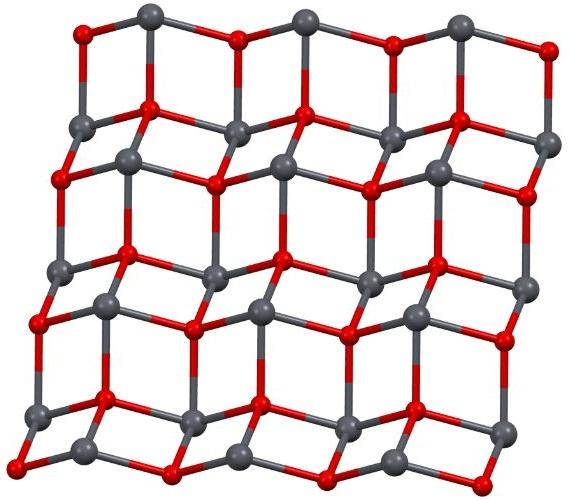
- El monóxido de plomo puede presentar dos distintas apariencias: como polvo seco de color amarillo con estructura ortorrómbica (masicotita) o como cristales tetragonales de color rojizo (litargirio). Ambas formas se ilustran en la figura inferior.

- El compuesto tiene un peso molecular de 223,20 g/mol.
- Tiene una densidad de 9,53 g/ml.
- Posee un punto de fusión de 888 °C y un punto de ebullición de 1470 °C.
- El compuesto es muy poco soluble en agua, pudiendo disolverse apenas 0,0504 gramos por cada litro a 25 °C en forma de masicotita y 0,1065 gramos por cada litro a 25 °C en forma de litargirio. El compuesto también es insoluble en alcohol. Es soluble en ácido acético, HNO3 diluido y álcalis.
- Es un agente oxidante o reductor débil, sin embargo, aún pueden producirse reacciones de redox. Estos compuestos no son reactivos al agua.
- El óxido de plomo oxida al carburo de aluminio con incandescencia al calentarse. Las mezclas de óxido de plomo con polvo de aluminio (como con otros metales: sodio, zirconio) dan una explosión violenta.
Reactividad y peligros del óxido plumboso
- El monóxido de plomo es un compuesto clasificado como venenoso. La sustancia es tóxica para el sistema nervioso central y puede ser cancerígeno en humanos.
- El síntoma de envenenamiento temprano son líneas de plomo que aparecen en el borde de las encías y la piel se torna grisácea. El síndrome neurasténico también surgirá en el período inicial de envenenamiento.
- El envenenamiento cerebeloso puede resultar en la depresión por envenenamiento por plomo, manía de envenenamiento por plomo, así como toxicidad por plomo y sensibilidad a la parálisis neuritis múltiple.
- El envenenamiento por plomo también puede causar anemia hipocrómica y trastornos metabólicos y endocrinos. Además, el envenenamiento por plomo puede inhibir la actividad de ciertas enzimas en el sistema digestivo y causar indigestión, dolor abdominal intenso y daño hepático. También puede causar hipertensión arterial y aumento del colesterol.
- Si hay dolor abdominal severo, pueden tomarse algunas medidas, como la inyección subcutánea de atropina y otras drogas, abdominal caliente, enema, baño de agua caliente y así sucesivamente. La concentración máxima permitida en el aire es de 0,01 mg / m³.
- En caso de contacto con los ojos o con la piel se debe lavar con abundante agua. En caso de inhalación o ingestión se debe llevar a la víctima a un lugar ventilado. No se debe inducir el vómito. Si la víctima no respira, se debe administrar resucitación de boca a boca.
- En todos los casos se debe buscar atención médica inmediata. El monóxido de plomo es un compuesto dañino para el medio ambiente, la bioacumulación de este producto químico puede ocurrir en plantas y mamíferos.
- Se recomienda encarecidamente que esta sustancia no entre en el medio ambiente, por lo que debe de ser manejada y almacenada según las estipulaciones establecidas.
Usos del óxido plumboso
- El óxido plumboso se ha utilizado como secador de pinturas y como flujo de fuego bajo en la fabricación de cerámica y vidrio. El vidrio de cristal de plomo es empleado en la fabricación de vajilla de alta calidad.
- Usando monóxido de plomo como fundente, es posible obtener un vidrio con un alto índice de refracción y por consiguiente, el brillo deseado.
- Los conductores cerámicos semimetálicos tienen las conductividades más altas de todas las cerámicas, excepto las superconductoras. El óxido de plomo es un ejemplo de este tipo de cerámicas semimetálicas. Estos materiales tienen bandas de energía de electrones superpuestas y, por lo tanto, son excelentes conductores electrónicos.
- El óxido de plomo se emplea principalmente en tubos de electrones, tubos de imagen, vidrio óptico, vidrio de plomo anti-rayos X y cauchos resistentes a radiación.
- Es utilizado como reactivo analítico, el flujo de silicato, pero también para la precipitación de aminoácidos.
- El óxido de plomo se usa en la fabricación del estabilizador plástico del PVC y también es la materia prima de otras sales de plomo. También se aplica en la refinación del petróleo y para la determinación de oro y plata.
- Asimismo, se emplea como un pigmento amarillo en pinturas y esmaltes. La masicotita fue utilizada como un pigmento de artistas de los siglos XV a XVIII.
- Las capas delgadas de monóxido de plomo se usan para producir colores iridiscentes en latón y bronce. El litargirio se mezcla con el glicerol para hacer el cemento del fontanero.
Referencias
- Glass. Recuperado de britannica.com.
- Lead monoxide. Recuperado de cameo.mfa.org.
- Conductive ceramics. Recuperado de britannica.com.