¿Qué son las oxidorreductasas?
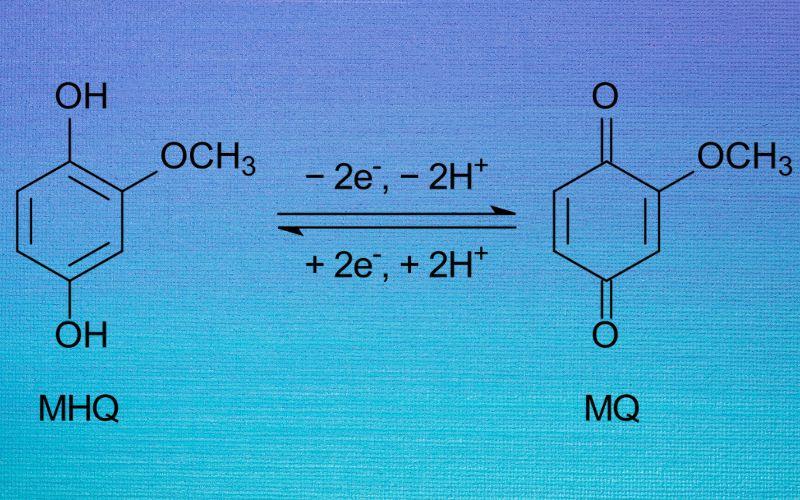
Las oxidorreductasas son proteínas con actividad enzimática, encargadas de catalizar reacciones de óxido-reducción, es decir, reacciones que implican la remoción de átomos de hidrógeno o de electrones en los sustratos sobre los que actúan.
Las reacciones catalizadas por estas enzimas, como su nombre lo indica, son reacciones de óxido-reducción, donde una molécula dona electrones o átomos de hidrógeno y otra los recibe, cambiando sus estados de oxidación respectivos.
Ejemplo de enzimas oxidorreductasas muy comunes en la naturaleza es el de las deshidrogenasas y oxidasas. Podría mencionarse la enzima de alcohol deshidrogenasa, que cataliza la deshidrogenación del etanol para producir acetaldehído de forma NAD+ dependiente o la reacción inversa, para producir etanol durante la fermentación alcohólica llevada a cabo por algunas levaduras comercialmente importantes.
Las enzimas de la cadena transportadora de electrones en las células aeróbicas son oxidorreductasas encargadas del bombeo de protones, por lo que generan el gradiente electroquímico a través de la membrana mitocondrial interna que permite impulsar la síntesis de ATP.
Características de las oxidorreductasas
– Función principal. Catalizan reacciones de oxidación y reducción, donde una molécula se oxida (pierde electrones o hidrógeno) y otra se reduce (los gana).
– Uso de coenzimas. Muchas oxidorreductasas requieren cofactores o coenzimas para transferir electrones. Los más comunes son NAD⁺/NADH, NADP⁺/NADPH, FAD/FADH₂ y FMN.
– Subclases importantes. Deshidrogenasas: eliminan átomos de hidrógeno (ejemplo: alcohol deshidrogenasa). Oxidasas: transfieren electrones al oxígeno molecular (ejemplo: citocromo c oxidasa). Oxigenasas: incorporan oxígeno en sustratos (ejemplo: monooxigenasas). Reductasas: catalizan la reducción de compuestos (ejemplo: ribonucleótido reductasa).
– Localización biológica. Están presentes en mitocondrias, cloroplastos, citoplasma y otros compartimentos celulares. Son claves en rutas como la respiración celular y la fotosíntesis.
– Importancia metabólica. Participan en procesos de obtención y almacenamiento de energía (glucólisis, ciclo de Krebs, cadena de transporte de electrones). Regulan la síntesis de biomoléculas y el equilibrio redox celular.
Clasificación de las oxidorreductasas
Muchas veces, la nomenclatura y clasificación de estas enzimas se basa tanto en el sustrato principal que emplean como en el tipo de coenzima que requieren para funcionar.
Según las recomendaciones del Comité de Nomenclatura de la Unión Internacional para Bioquímica y Biología Molecular (NC-IUBMB), estas enzimas pertenecen a la clase E.C. 1 e incluyen más o menos 23 tipos diferentes (E.C.1.1-E.C.1.23), que son:
- E.C. 1.1: actúan en los grupos CH-OH de los donadores.
- E.C. 1.2: actúan en el grupo aldehído o el grupo oxo de los donadores.
- E.C. 1.3: actúan en los grupos CH-CH de los donadores.
- E.C. 1.4: actúan en los grupos CH-NH2 de los donadores.
- E.C. 1.5: actúan en los grupos CH-NH de los donadores.
- E.C. 1.6: actúan en el NADH o en el NADPH.
- E.C. 1.7: actúan sobre otros compuestos nitrogenados como donadores.
- E.C. 1.8: actúan sobre los grupos sulfurados de los donadores.
- E.C. 1.9: actúan en los grupos hemo de los donadores.
- E.C. 1.10: actúan en donadores como difenoles y otras sustancias relacionadas.
- E.C. 1.11: actúan sobre peróxido como aceptor.
- E.C. 1.12: actúan sobre el hidrógeno como donador.
- E.C. 1.13: actúan sobre donadores sencillos con la incorporación de oxígeno molecular (oxigenasas).
- E.C. 1.14: actúan sobre donadores “apareados”, con la incorporación o la reducción de oxígeno molecular.
- E.C. 1.15: actúan sobre superóxidos como aceptores.
- E.C. 1.16: oxidan iones metálicos.
- E.C. 1.17: actúan sobre grupos CH o CH2.
- E.C. 1.18: actúan sobre proteínas que contienen hierro y azufre como donadoras.
- E.C. 1.19: actúan sobre flavodoxina reducida como donador.
- E.C. 1.20: actúan sobre donadores como el fósforo y el arsénico.
- E.C. 1.21: actúan en la reacción X-H + Y-H = X-Y.
- E.C. 1.22: actúan sobre el halógeno de los donadores.
- E.C. 1.23: reducen los grupos C-O-C como aceptores.
- E.C. 1.97: otras oxidorreductasas.
Cada una de estas categorías incluye, además, subgrupos en los cuales se separan las enzimas de acuerdo con la preferencia de sustratos.
Por ejemplo, dentro del grupo de las oxidorreductasas que actúan sobre los grupos CH-OH de sus donadores existen unas que prefieren NAD+ o NADP+ como aceptores, mientras que otras utilizan citocromos, oxígeno, azufre, etc.
Estructura de las oxidorreductasas
Como el grupo de las oxidorreductasas es sumamente diverso, establecer una característica estructural definida resulta bastante complicado. Su estructura no solo varía de enzima a enzima, sino también entre especies o grupo de seres vivos, e incluso de célula a célula en tejidos diferentes.
La enzima piruvato deshidrogenasa, por ejemplo, es un complejo compuesto por tres subunidades catalíticas unidas secuencialmente, y conocidas como la subunidad E1 (piruvato deshidrogenasa), la subunidad E2 (dihidrolipoamida acetiltransferasa) y la subunidad E3 (dihidrolipoamida deshidrogenasa).
Cada una de estas subunidades, a su vez, puede estar compuesta por más de un monómero proteico del mismo tipo o de tipos diferentes, es decir, pueden ser homodiméricas (las que tienen solo dos monómeros iguales), heterotriméricas (las que tienen tres monómeros distintos) y así sucesivamente.
No obstante, usualmente se trata de enzimas compuestas por hélices alfa y láminas β-plegadas dispuestas de diferentes formas, con interacciones intra e intermoleculares específicas de diferentes tipos.
Funciones de las oxidorreductasas
- Catalizar reacciones de óxido-reducción. Facilitan la transferencia de electrones o átomos de hidrógeno entre moléculas. Permiten que un compuesto se oxide y otro se reduzca, procesos esenciales en el metabolismo.
- Participar en la obtención de energía. Son claves en la respiración celular: oxidan nutrientes (como glucosa o ácidos grasos) y transfieren electrones a la cadena de transporte, produciendo ATP. Ejemplo: deshidrogenasas del ciclo de Krebs.
- Intervenir en la fotosíntesis. En organismos fotosintéticos, ayudan a transferir electrones durante la fase lumínica, capturando energía solar y almacenándola en moléculas como NADPH.
- Mantener el equilibrio redox celular. Regulan la proporción de cofactores como NAD⁺/NADH y NADP⁺/NADPH, fundamentales para el metabolismo y la defensa antioxidante.
- Participar en la biosíntesis de compuestos. Algunas oxidorreductasas (como las reductasas) permiten la síntesis de lípidos, nucleótidos y aminoácidos al proveer electrones.
- Detoxificación y defensa celular. Enzimas como las oxidasas y peroxidasas ayudan a neutralizar compuestos tóxicos (radicales libres, peróxido de hidrógeno). Ejemplo: catalasa, que descompone el H₂O₂ en agua y oxígeno.
- Participación en reacciones especiales, Oxigenasas incorporan átomos de oxígeno en moléculas, fundamentales en el metabolismo de fármacos y hormonas. Ejemplo: citocromo P450.
Ejemplos de oxidorreductasas
Existen cientos de ejemplos de enzimas oxidorreductasas en la naturaleza y en la industria. Estas enzimas, como se comentó, tienen funciones de suma importancia para el funcionamiento celular y, por lo tanto, para la vida per se.
Las oxidorreductasas no solo incluyen las enzimas peroxidasas, lacasas, glucosa oxidasas o alcohol deshidrogenasas; también aúnan importantes complejos como la enzima gliceraldehído 3-fosfato deshidrogenasa o el complejo piruvato deshidrogenasa, etc., esenciales desde el punto de vista del catabolismo de la glucosa.
Incluye también todas las enzimas del complejo de transporte electrónico en la membrana mitocondrial interna o en la membrana interna de las bacterias, similares a algunas de las enzimas que se encuentran en los cloroplastos de los organismos vegetales.
- Peroxidasas. Las peroxidasas son enzimas muy diversas y emplean el peróxido de hidrógeno como aceptor de electrones para catalizar la oxidación de gran variedad de sustratos, entre los que se incluyen fenoles, aminas o tioles, entre otros. En sus reacciones reducen el peróxido de hidrógeno hasta producir agua. Son muy importantes desde el punto de vista industrial, siendo la peroxidasa del rábano picante la más importante y estudiada de todas. Biológicamente hablando, las peroxidasas son importantes para la eliminación de compuestos de oxígeno reactivos que pueden causar importantes daños en las células.
Referencias
- Oxidoreductases. Recuperado de britannica.com.
- Ercili-Cura, D., Huppertz, T., Kelly, A.L. Enzymatic modification of dairy product texture. In Modifying Food Texture. Woodhead Publishing.
- Mathews, C.K., Van Holde, K.E., Ahern, K.G. Biochemistry. Add. Wesley Longman.
- Nelson, D.L., Lehninger, A.L., Cox, M.M. Lehninger principles of biochemistry. MacMillan.
- Patel, M.S., Nemeria, N.S., Furey, W., Jordan, F. The pyruvate dehydrogenase complexes: structure-based function and regulation. Journal of Biological Chemistry.