¿Qué es la piruvato quinasa?
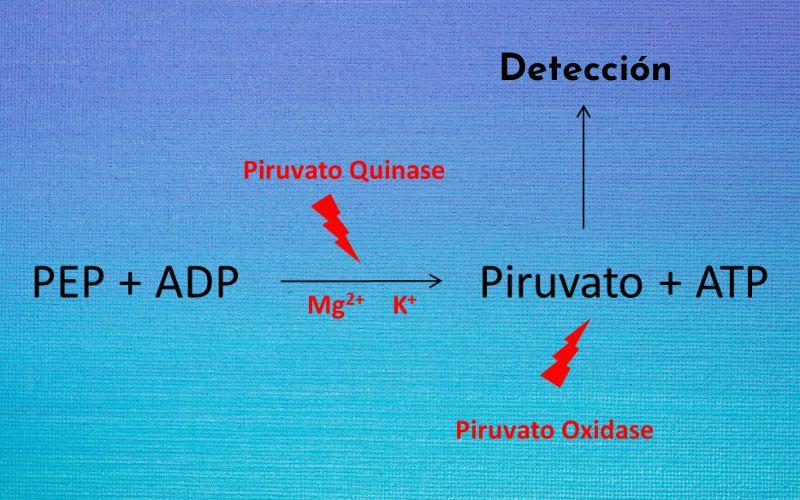
La piruvato quinasa (PYK) es la enzima que cataliza el último paso de la ruta glucolítica, que implica la transferencia irreversible del grupo fosfato de una molécula de fosfoenolpiruvato (PEP) hacia una molécula de ADP, lo que resulta en la síntesis de una molécula de ATP y otra de ácido pirúvico o piruvato.
El piruvato así producido posteriormente participa en diversas rutas catabólicas y anabólicas (biosintéticas): puede ser descarboxilado para producir acetil-CoA, carboxilado para producir oxalacetato, transaminado para producir alanina, oxidado para producir ácido láctico, o puede ser dirigido hacia la gluconeogénesis para la síntesis de glucosa.
Puesto que participa en la glucólisis, esta enzima es de suma importancia para el metabolismo de carbohidratos de muchos organismos, unicelulares y multicelulares, que la emplean como la principal ruta catabólica para obtener energía.
Un ejemplo de células estrictamente dependientes de la glucólisis para la obtención de energía es el de los eritrocitos de los mamíferos, para los cuales una deficiencia en cualquiera de las enzimas que participan en esta ruta puede tener efectos considerablemente negativos.
Estructura de la piruvato quinasa
En los mamíferos se han descrito cuatro isoformas de la enzima piruvato quinasa:
- PKM1, típica en los músculos.
- PKM2, únicamente en los fetos (ambas productos del procesamiento alternativo del mismo ARN mensajero).
- PKL, presente en el hígado.
- PKR, presente en los eritrocitos (ambas codificadas por el mismo gen, PKLR, pero transcritas por promotores diferentes).
Empero, los análisis realizados a la estructura de las diferentes enzimas piruvato quinasa en la naturaleza (incluyendo estas 4 de los mamíferos) demuestran una gran similitud en la estructura general, así como respecto a la arquitectura del sitio activo y los mecanismos de regulación.
- Peso molecular. En líneas generales, se trata de una enzima de 200 kDa.
- Estructura. Tetramérica compuesta por 4 unidades proteicas idénticas, de más o menos 50 o 60 kDa, y cada una con 4 dominios, a saber: un dominio helicoidal pequeño en el extremo N-terminal (ausente en las enzimas bacterianas); un dominio “A”, identificado por una topología de 8 láminas β plegadas y 8 hélices α; un dominio “B”, insertado entre la lámina beta plegada número 3 y la hélice alfa número 3 del dominio “A”; un dominio “C”, que posee una topología α+β.
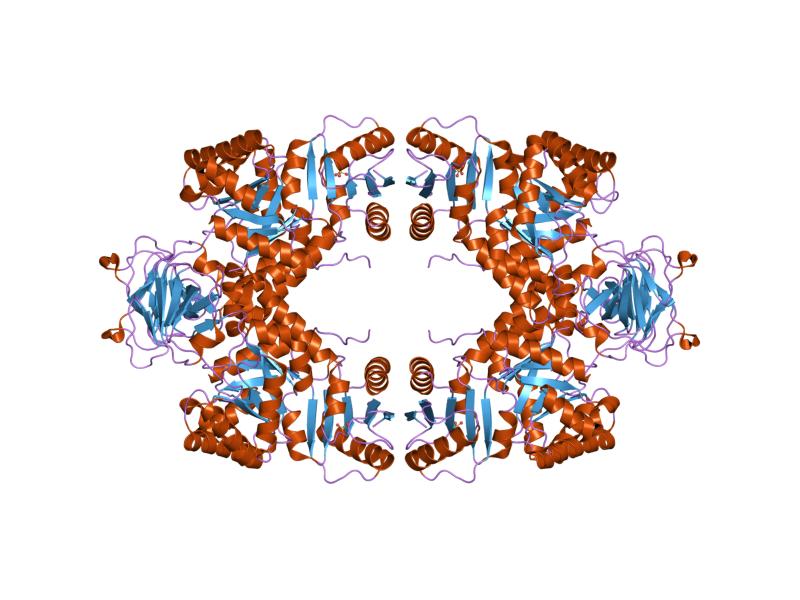
- Sitios. Se han detectado tres en los tetrámeros de la piruvato quinasa de diferentes organismos: el sitio activo, el sitio efector y el sitio de unión a aminoácidos. El sitio activo de estas enzimas se encuentra entre los dominios A y B, en las cercanías del “sitio efector”, que pertenece al dominio C. En el tetrámero, los dominios C forman una interfase “pequeña”, mientras que los dominios A forman una interfase de mayor tamaño.
Funciones de la piruvato quinasa
- Función catalítica principal. Cataliza la reacción final de la glucólisis: Fosfoenolpiruvato (PEP) + ADP → Piruvato + ATP. Es decir, transforma el fosfoenolpiruvato en piruvato, generando ATP. Esta es una reacción irreversible y fundamental en la obtención de energía.
- Producción de energía. Es una de las etapas donde se produce ATP por fosforilación a nivel de sustrato. Aporta energía rápida, especialmente importante en células con gran demanda energética (como las musculares durante el ejercicio).
- Regulación metabólica. Es un punto de control clave de la glucólisis. Se regula de manera alostérica por activadores: fructosa-1,6-bisfosfato (efecto de retroalimentación positiva) e inhibidores: ATP y alanina (indicadores de que ya hay suficiente energía o sustratos). En el hígado, también está regulada por fosforilación/desfosforilación en respuesta a hormonas como la insulina y el glucagón.
- Conexión con otras rutas metabólicas. El piruvato formado puede tener distintos destinos: convertirse en acetil-CoA (entrada al ciclo de Krebs), transformarse en lactato en condiciones anaerobias, o servir como precursor en la gluconeogénesis o en la síntesis de aminoácidos. Así, la PK conecta la glucólisis con otros procesos metabólicos esenciales.
- Relevancia fisiológica y clínica. Existen isoformas de la piruvato quinasa (PKM1, PKM2, PKL, PKR) con funciones específicas en diferentes tejidos. Alteraciones en la PK pueden provocar enfermedades, como la deficiencia de piruvato quinasa (causa de anemias hemolíticas hereditarias). En el cáncer, la isoforma PKM2 favorece la reprogramación metabólica de las células tumorales (efecto Warburg).
Regulación de la piruvato quinasa
La piruvato quinasa es una enzima sumamente importante desde el punto de vista del metabolismo celular, pues es la que forma el último compuesto resultante de la ruta del catabolismo de la glucosa: el piruvato.
Además de ser una de las tres enzimas más reguladas de toda la ruta glucolítica (siendo las otras dos la hexoquinasa (HK) y la fosfofructoquinasa (PFK)), la piruvato quinasa es una enzima indispensable para el control del flujo metabólico y la producción de ATP por glucólisis.
Es activada por el fosfoenolpiruvato, uno de sus sustratos (regulación homotrópica), así como por otros azúcares mono y difosforilados, aunque su regulación depende del tipo de isoenzima que se considere.
Algunos textos científicos sugieren que la regulación de esta enzima depende también de su arquitectura “multidominio”, pues su activación parece depender de algunas rotaciones en los dominios de las subunidades y de alteraciones en la geometría del sitio activo.
Para muchos organismos, la activación alostérica de la piruvato quinasa depende de la fructosa 1,6-bifosfato (F16BP), pero esto no es cierto para las enzimas vegetales. Otras enzimas son activadas también por el AMP cíclico y la glucosa 6-fosfato.
Además, se ha demostrado que la actividad de la mayor parte de las piruvato quinasas estudiadas depende enormemente de la presencia de iones monovalentes como el potasio (K+) y de iones divalentes como el magnesio (Mg+2) y el manganeso (Mn+2).
Inhibición de la piruvato quinasa
La piruvato quinasa es inhibida principalmente por efectores alostéricos fisiológicos, por lo que estos procesos varían considerablemente entre especies diferentes e incluso entre tipos de células y tejidos del mismo organismo.
En muchos mamíferos, el glucagón, la epinefrina y el AMPc tienen efectos inhibitorios sobre la actividad de la piruvato quinasa, efectos que pueden ser contrarrestados por la insulina.
Además, se ha comprobado que algunos aminoácidos, como, por ejemplo, la fenilalanina, pueden tener acciones como inhibidores competitivos para esta enzima en el cerebro.