Explicamos qué es el potasio, su historia, estructura química, propiedades físicas y químicas, reacciones, usos y más.
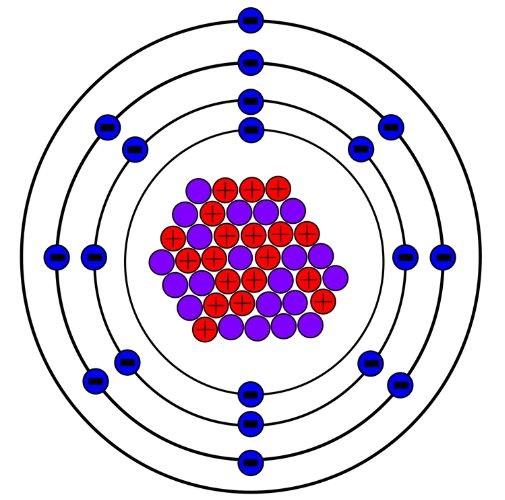
¿Qué es el potasio?
El potasio es un metal alcalino cuyo símbolo químico es K. Su número atómico es el 19 y se ubica debajo del sodio en la tabla periódica. Es un metal blando que puede cortarse con cuchillo. Es bastante liviano, y puede flotar sobre el agua líquida mientras reacciona vigorosamente.
Recién cortado, presenta un color blanco plateado muy brillante, pero al exponerse al aire se oxida rápidamente y pierde su lustre, tornándose grisáceo.
El potasio reacciona explosivamente con el agua para formar el hidróxido de potasio e hidrógeno gaseoso. Precisamente este gas es el causante de la explosividad de la reacción. Cuando arde en el mechero, sus átomos excitados tiñen la llama de un color lila intenso. Esta es una de sus pruebas cualitativas.
Es el séptimo metal más abundante en la corteza terrestre y representa el 2,6% de su peso. Se encuentra principalmente en rocas ígneas, lutitas y sedimentos, además de minerales como la silvita (KCl). Al contrario del sodio, su concentración en el agua de mar es baja (0,39 g/L).
Historia del potasio
Potasa
Desde la Antigüedad, se ha usado la potasa como fertilizante, aunque se desconocía la existencia del potasio y su relación con la potasa. Se preparaba con las cenizas de los troncos y hojas de árboles, a los que se les agregaba agua, que posteriormente se evaporaba.
Los vegetales contienen mayormente potasio, sodio y calcio. Pero los compuestos de calcio son poco solubles en agua. Por esta razón, la potasa era un concentrado de compuestos de potasio. La palabra se deriva de la contracción de las palabras inglesas ‘pot’ y ‘ash’.
En 1702, G. Ernst Stahl sugirió una diferencia entre las sales de sodio y potasio, sugerencia que fue comprobada por Henry Duhamel du Monceau, en 1736. Como no se conocía la composición exacta de las sales, Antoine Lavoiser (1789) decidió no incluir los álcalis en la lista de elementos químicos.
Descubrimiento
En 1797, el químico alemán Martin Klaproth descubrió potasa en los minerales leucita y lepidolita, por lo que concluyó que no era solamente un producto de las plantas.
En 1806, el químico inglés Humphrey Davy descubrió que el enlace entre los elementos de un compuesto era de naturaleza eléctrica. Luego, Davy aisló potasio mediante la electrólisis de hidróxido de potasio, logrando observar unos glóbulos de brillo metálico que se acumulaban en el ánodo. Llamó al metal con la palabra de etimología inglesa potassium.
En 1809, Ludwig Wilhelm Gilbert propuso el nombre de kalium (kalio) para el potasio de Davy. Berzelius evocó el nombre de kalium para asignarle al potasio el símbolo químico “K”. Finalmente, Justus Liebig en 1840 descubrió que el potasio es un elemento necesario para las plantas.
Estructura y configuración electrónica del potasio
El potasio metálico cristaliza en condiciones normales en la estructura cúbica centrada en el cuerpo (bcc, por sus siglas en inglés: body centered cubic). Esta es poco densa, lo cual concuerda con las propiedades del potasio. Un átomo K está rodeado de ocho vecinos, justo en el centro de un cubo y con los otros átomos K situados en los vértices.
A esta fase bcc también se le designa como fase K-I (la primera). Cuando aumenta la presión, la estructura cristalina se compacta a la fase cúbica centrada en las caras (fcc, por face centered cubic). Sin embargo, se necesita una presión de 11 GPa para que dicha transición ocurra espontáneamente.
Esta fase fcc, más densa, se le conoce como K-II. A presiones más altas (80 GPa), y temperaturas más bajas (menores a -120 ºC), el potasio adquiere una tercera fase: K-III. El K-III se caracteriza por su capacidad de alojar otros átomos o moléculas dentro de sus cavidades cristalinas.
Existen además otras dos fases cristalinas a presiones todavía más grandes: el K-IV (54 GPa) y K-V (90 GPa). A temperaturas muy frías, el potasio exhibe una fase amorfa (con los átomos K desordenados).
Número de oxidación
La configuración electrónica del potasio es:
[Ar] 4s1
El orbital 4s es el más externo y, por lo tanto, posee el único electrón de valencia. Este, en teoría, es el responsable del enlace metálico que mantiene unidos los átomos de K para definir un cristal.
A partir de la misma configuración electrónica es fácil entender por qué el potasio suele tener siempre (o casi siempre) un número de oxidación de +1. Cuando pierde un electrón para formar el catión K+, se vuelve isoelectrónico al gas noble argón, con su octeto de valencia completo.
En la mayoría de sus compuestos derivados se asume que el potasio se halla como K+ (aun si sus enlaces no sean puramente iónicos).
Por otro lado, aunque menos probable, el potasio puede ganar un electrón, teniendo dos electrones en su orbital 4s. Así, se vuelve isoelectrónico al metal calcio:
[Ar] 4s2
Se dice entonces que ganó un electrón y tiene un número de oxidación negativo, -1. Cuando en un compuesto se calcula este número de oxidación, se asume la existencia del anión potasuro, K–.
Propiedades del potasio
- Apariencia. Metal plateado blanco brillante.
- Carga nuclear efectiva. La carga nuclear efectiva del potasio es +1. Posee una baja energía de ionización, por lo que tiene una gran facilidad para perder el único electrón presente en su capa externa.
- Masa molar. 39,0983 g/mol.
- Punto de fusión. 83,5 ºC.
- Punto de ebullición. 759 ºC.
- Densidad. 0,862 g/cm3, a temperatura ambiente. 0,828 g/cm3, en el punto de fusión (líquido).
- Solubilidad. Reacciona violentamente con el agua. Soluble en amoniaco líquido, etilendiamina y anilina. Soluble en otros metales alcalinos para formar aleaciones, y en mercurio.
- Densidad del vapor. 1,4 en relación al aire tomado como 1.
- Presión de vapor. 8 mmHg a 432 ºC.
- Estabilidad. Estable si está protegido del aire y la humedad.
- Corrosividad. Puede ser corrosivo en contacto con los metales. Por contacto, puede causar quemaduras en piel y ojos.
- Tensión superficial. 86 dinas/cm a 100 ºC.
- Calor de fusión. 2,33 kJ/mol.
- Calor de vaporización. 76,9 kJ/mol.
- Capacidad térmica molar. 29,6 J/(mol·K).
- Electronegatividad. 0,82 en la escala de Pauling.
- Energías de ionización. Primer nivel de ionización: 418,8 kJ/mol. Segundo nivel de ionización: 3.052 kJ/mol. Tercer nivel de ionización: 4.420 kJ/mol.
- Radio atómico. 227 pm.
- Radio covalente. 203 ± 12 pm.
- Expansión térmica. 83,3 µm/(m·K) a 25 ºC.
- Conductividad térmica. 102,5 W/(m·K).
- Resistividad eléctrica. 72 nΩ·m (a 25 ºC).
- Dureza. 0,4 en la escala Mohs.
- Isótopos naturales. El potasio se presenta como tres isótopos principalmente: 39K (93,258 %),41K (6,73 %) y 40K (0,012 %, radiactivo de emisión β)
Nomenclatura del potasio
Los compuestos de potasio tienen por defecto el número de oxidación +1 (salvo excepciones muy especiales). Por lo tanto, en la nomenclatura stock se omite el (I) al final de los nombres, y en la nomenclatura tradicional, los nombres terminan con el sufijo -ico.
Por ejemplo, el KCl es el cloruro de potasio, y no cloruro de potasio (I). Su nombre tradicional es cloruro potásico o monocloruro de potasio, de acuerdo a la nomenclatura sistemática.
De resto, a menos que sean nombres muy comunes o de minerales (como la silvina), la nomenclatura en torno al potasio es bastante simple.
Formas del potasio
El potasio no está en la naturaleza en forma metálica, pero puede ser obtenido industrialmente bajo esta forma para ciertos usos. Se encuentra sobre todo en los seres vivos, bajo la forma iónica (K+). En general, es el principal catión intracelular.
El potasio está presente en numerosos compuestos, como el hidróxido, acetato o cloruro de potasio, etc. También forma parte de cerca de 600 minerales, como la silvita, la alunita, la carnalita, etc.
El potasio forma aleaciones con otros elementos alcalinos, como el sodio, el cesio y el rubidio. También forma aleaciones ternarias con sodio y cesio, a través de las llamadas fusiones eutécticas.
Papel biológico del potasio
- Plantas. El potasio constituye, junto al nitrógeno y el fósforo, los tres nutrientes principales de las plantas. Es absorbido por las raíces en forma iónica, proceso favorecido por la existencia de condiciones adecuadas de humedad, temperatura y oxigenación.
- Animales. En los animales, en general, el potasio es el principal catión intracelular con una concentración de 140 mmol/L, mientras que la concentración extracelular varía entre 3,8 y 5,0 mmol/L. El 98% del potasio corporal se encuentra confinado en el compartimiento intracelular.
- Repolarización de las células. La formación de los potenciales de acción e inicio de la contracción muscular es una responsabilidad compartida del sodio y potasio.
- Otras funciones. El potasio cumple otras funciones en los seres humanos, como el tono vascular, el control de la presión sanguínea sistémica y la motilidad gastrointestinal.
Dónde se encuentra el potasio y producción

El potasio se encuentra principalmente en rocas ígneas, lutitas y en sedimentos. Además, en minerales como la moscovita y la ortoclasa, que son insolubles en el agua. La ortoclasa es un mineral que se suele presentar en las rocas ígneas y en el granito.
El potasio también está presente en compuestos minerales solubles en el agua, como la carnalita (KMgCl3·6H2O), la silvita (KCl), y la landbeinita [K2Mg2(SO4)3], que se encuentran en lechos secos de lagos y en el fondo marino.
Además, el potasio se encuentra en salmueras y como producto de la incineración de troncos y hojas de plantas en un proceso usado para producir potasa. Aunque su concentración en agua de mar es baja (0,39 g/L), también se usa para la obtención de potasio.
El potasio está presente en grandes yacimientos, como el existente en Saskatchewan, en Canadá, rico en el mineral silvita (KCl) y capaz de producir el 25% del consumo mundial de potasio. Los líquidos de desechos de las salinas pueden contener una cantidad importante de potasio, bajo la forma de KCl.
Electrólisis
El potasio se produce por dos métodos: electrólisis y térmico. En la electrólisis se ha seguido, sin grandes modificaciones, el método usado por Davy para aislar el potasio.
Sin embargo, este método, desde el punto industrial, no es eficiente, ya que debe disminuirse el alto punto de fusión de los compuestos de potasio fundidos.
El método de electrólisis del hidróxido de potasio fue usado industrialmente en la década de 1920. El método térmico lo suplantó, y se convirtió en el método dominante a partir de 1950 para producir este metal.
Método térmico
En el método térmico el potasio se produce por la reducción de cloruro potásico fundido a 870 ºC. Este alimenta continuamente a una columna de destilación empacada con la sal. Mientras, el vapor de sodio pasa a través de la columna para producir la reducción del cloruro de potasio.
El potasio es el componente más volátil de la reacción y se acumula en la parte superior de la columna de destilación, donde es recogido en forma continua. La producción de potasio metálico por el método térmico puede esquematizarse en la siguiente ecuación química:
Na(g) + KCl(l) => K(l) + NaCl(l)
También se usa el proceso de Griesheimer, que emplea la reacción del fluoruro de potasio con el carburo de calcio:
2 KF + CaC2 => 2 K + CaF2 + 2 C
Reacciones del potasio
- Inorgánicas. El potasio es un elemento muy reactivo que reacciona rápidamente con el oxígeno para formar tres óxidos: óxido (K2O), peróxido (K2O2) y superóxido (KO2) de potasio. El potasio es un elemento fuertemente reductor, por esto se oxida más rápidamente que la mayoría de los metales. Es utilizado para reducir las sales de metales, reemplazando el potasio al metal de la sal. Este método permite la obtención de metales puros:
MgCl2 + 2 K => Mg + 2 KCl
-
- Reacciona fuertemente con el agua para formar hidróxido de potasio y liberar el gas hidrógeno de carácter explosivo (imagen inferior). El hidróxido de potasio puede reaccionar con el dióxido de carbono para producir el carbonato de potasio. El potasio reacciona con el monóxido de carbono a temperatura de 60 ºC para producir un carbonilo explosivo (K6C6O6). También reacciona con hidrógeno a 350 ºC, formando un hidruro. Asimismo, es altamente reactivo con los halógenos, y explota en contacto con el bromo líquido. También se producen explosiones cuando el potasio reacciona con los ácidos halogenados, como el ácido clorhídrico, y la mezcla es golpeada o sacudida fuertemente. El potasio fundido reacciona además con azufre y sulfuro de hidrógeno.

- Orgánicas. Reacciona con compuestos orgánicos que contienen grupos activos, pero es inerte a los hidrocarburos alifáticos y aromáticos. El potasio reacciona lentamente con el amonio para formar potasomina (KNH2). Al contrario del sodio, el potasio reacciona con el carbono bajo la forma de grafito para formar una serie de compuestos interlaminares. Estos compuestos tienen relaciones atómicas carbono-potasio: 8, 16, 24, 36, 48, 60 o 1; es decir, KC60, por ejemplo.
Usos del potasio
- Potasio metálico. No hay mucha demanda industrial por el potasio metálico. La mayor parte se convierte en superóxido de potasio, usado en los equipos de respiración, ya que libera oxígeno y elimina el dióxido de carbono y el vapor de agua. La aleación de NaK tiene gran capacidad de absorción de calor, por lo que se usa como refrigerante en algunos reactores nucleares. Asimismo, se ha usado el metal vaporizado en turbinas.
- Compuestos
- Cloruro. Se usa el KCl en la agricultura como fertilizante. También como materia prima para la producción de otros compuestos de potasio, como el hidróxido de potasio.
- Hidróxido. También conocida como potasa cáustica, KOH, se usa en la fabricación de jabones y detergentes. Su reacción con el yodo produce yoduro de potasio. Esta sal se añade a la sal de mesa (NaCl) y al pienso para protegerlo contra una deficiencia de yodo. El hidróxido de potasio es usado en la fabricación de las pilas alcalinas.
- Nitrato. También conocido como salitre, KNO3, se usa como fertilizante. Además, se emplea para fabricar fuegos artificiales, como conservante de alimentos, y en el endurecimiento del vidrio.
- Cromato. Se utiliza en la producción de fertilizante y producción de alumbre de potasio.
- Carbonato. Se usa en la fabricación de vidrios, especialmente los utilizados en la fabricación de los televisores.
Referencias
- Química Inorgánica (Cuarta edición). McGraw Hill.
- Potassium. Recuperado de en.wikipedia.org.
- Potassium. Recuperado de britannica.com.