La prueba del bromo es un ensayo que se aplica a muestras de compuestos orgánicos de composición desconocida y que permite detectar la presencia de enlaces dobles, enlaces triples, grupos fenólicos y anilinas.
La muestra desconocida se añade a una solución acuosa de bromo, la cual es marrón o naranja. Si al agregar el ejemplar la coloración marrón desaparece, significa que hay una insaturación presente y si ocurre la formación de un sólido blanco es señal de que hay un fenol o una anilina.

Es un test cualitativo, pues no se determinan cantidades sino solo la presencia de los grupos funcionales mencionados.
Las insaturaciones presentes en los alquenos (dobles enlaces C=C) reaccionan fácilmente con el bromo. Igualmente ocurre con los fenoles y anilinas en los cuales el anillo aromático se vuelve muy reactivo por la influencia de los grupos –OH y –NH2 respectivamente.
Existen dos ensayos afines a esta prueba que utilizan la misma reacción química. Permiten obtener parámetros importantes para caracterizar de forma cualitativa corrientes de refinación del petróleo y algunos de sus derivados.
[toc]
Fundamento de la prueba del bromo
El bromo reacciona con los enlaces dobles y triples y también con moléculas que contienen nitrógeno básico como las aminas aromáticas y con los alcoholes aromáticos (fenoles). Sin embargo, las olefinas son los lugares más reactivos.
Bromo
Este elemento (Br) pertenece al grupo de los halógenos junto con el flúor, cloro y yodo. El bromo molecular (Br2) es un líquido marrón rojizo. Una solución acuosa saturada de bromo molecular a 20 °C contiene 3,6 % (masa/volumen) de este elemento.

Olefinas o alquenos
Son compuestos insaturados de fórmula CnH2n. Se llaman insaturados porque poseen uno o más enlaces dobles C=C. El nombre de estos compuestos finaliza en –eno, como por ejemplo eteno (también llamado etileno), propeno (propileno), buteno, penteno, etc.
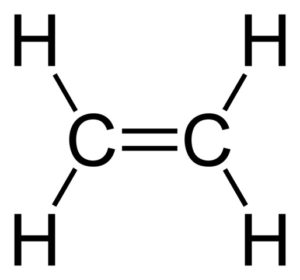
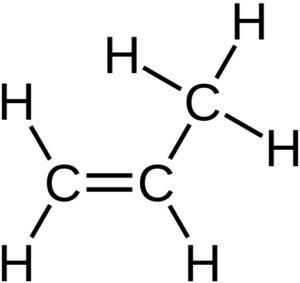
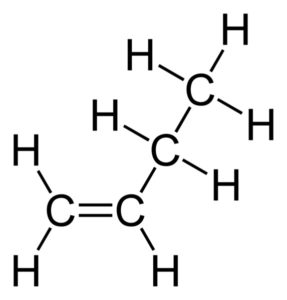
Son sustancias inestables si se comparan con los alcanos, por lo que reaccionan fácilmente con el bromo y otros compuestos.
Reacción del bromo con las olefinas y algunos alquinos
El bromo molecular reacciona con el doble enlace de los alquenos formando compuestos dibromados. Esta reacción es denominada adición. A continuación un ejemplo de adición de bromo a un doble enlace:
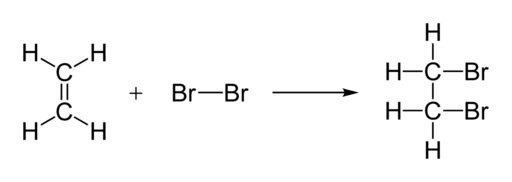
Al añadir el alqueno a la solución marrón o naranja de bromo este reacciona con la olefina formando un compuesto incoloro. El alqueno decolora el agua de bromo, los alcanos no lo hacen.
Los alquinos poseen enlaces triples (C≡C). La bromación del etino (HC≡CH) produce cis– y trans-1,2-dibromoeteno y 1,1,2,2-tetrabromoetano. En la figura que se encuentra a continuación está representado el trans-1,2-dibromoeteno.
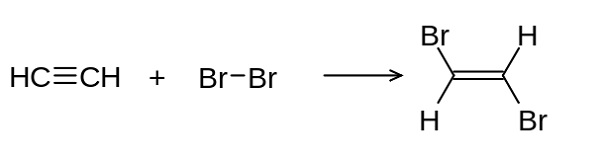
Fenoles y reacción con el bromo
Estos son compuestos cuya fórmula general es ArOH, donde Ar es un grupo aromático como fenilo, fenilo sustituido o cualquier otro grupo aromático. Se diferencian de los alcoholes en que el grupo –OH se encuentra unido directamente al anillo aromático.
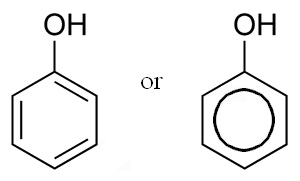
Una de sus propiedades químicas más importantes, además de la acidez, es la alta reactividad de su anillo aromático hacia la sustitución electrofílica. Es decir, la sustitución de un hidrógeno del anillo por un átomo ávido de electrones.
Es por ello que reaccionan fácilmente con el bromo.
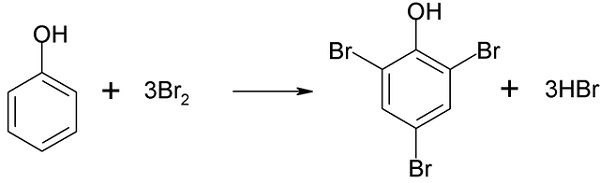
Anilinas y reacción con el bromo
Son aminas aromáticas, es decir, compuestos que poseen un grupo amino (–NH2) cuyo átomo de nitrógeno está unido directamente a un anillo aromático. El miembro más sencillo es la anilina:
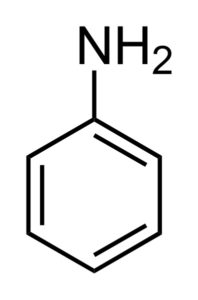
Presentan una basicidad apreciable. El nitrógeno del grupo amino tiene un par de electrones libres que le confieren un alto grado de nucleofilicidad o afinidad hacia compuestos que le faltan electrones y le proporcionan una alta reactividad al anillo aromático.
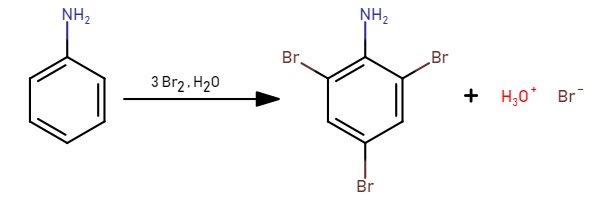
Por esta razón reaccionan fácilmente con el bromo, el cual ataca el anillo aromático. Por ejemplo la anilina con el bromo forma la 2,4,6-tribromoanilina.
Pruebas relacionadas con este ensayo
Existen otras pruebas que también aprovechan la reacción del bromo con los enlaces dobles. Son métodos cualitativos para medir los sitios reactivos de una muestra. Las pruebas son el número de bromo y el índice de bromo.
Número de bromo
Es el número de gramos (g) de bromo que reaccionan con 100 g de la muestra. Se emplea en destilados de petróleo como gasolina, kerosén y algunos gasóleos. Se aplica también en mezclas comerciales de monoolefinas alifáticas.
Índice de bromo
Es el número de miligramos (mg) de bromo que reaccionan con 100 g de la muestra. Se emplea en la industria química en materiales o líquidos que tienen un contenido de olefinas muy bajo.
Generación de bromo in situ
En estos ensayos el bromo se genera en el sitio utilizando una solución de bromuro y bromato.
BrO3– + 5 Br– + 6 H+ → 3 Br2 + 3 H2O
Una vez formado, el bromo reacciona con los enlaces C=C. La reacción se monitorea por titulación electrométrica. El procedimiento preciso ha sido publicado por la Sociedad Americana para Pruebas y Materiales o ASTM (siglas del inglés American Society for Testing and Materials).
El número de bromo corresponde al método ASTM D1159 y el índice de bromo se encuentra descrito en los métodos ASTM D 2710, ASTM D 1492 y ASTM D 5776.
Aplicaciones de estos ensayos
El número de bromo es una medida de las insaturaciones alifáticas en muestras de petróleo y sus destilados. En monoolefinas alifáticas comerciales sirve para proporcionar evidencia de su pureza e identidad.
El índice de bromo se aplica solamente a hidrocarburos esencialmente libres de olefinas, permitiendo medir trazas de estas.
Corrientes de alimentación a FCC
También se miden ambos parámetros en materiales pesados como la alimentación al sistema de craqueo catalítico en lecho fluidizado o FCC (siglas del inglés Fluid Catalytic Cracking), utilizado en la refinación del petróleo.
Ambas pruebas forman parte de una serie de ensayos que se aplican de forma rutinaria a las corrientes de alimentación a FCC, los cuales son importantes para su caracterización en cuanto a estructura molecular, pues permiten desarrollar modelos cinéticos para predecir el rendimiento de los productos deseados.

Razones para que el contenido de alquenos sea bajo
Dentro de los procesos de FCC las olefinas pueden polimerizar y generar productos indeseables como lodos y coque. Es por ello que se desea que las corrientes de alimentación al FCC posean menos de 5% (en peso) de olefinas.
Las corrientes de alimentación hidrotratadas poseen un número de bromo menor a 5, en el gasoil pesado de vacío es 10 y en el gasóleo de coquización es de 50. Como regla general se dice que la fracción de olefinas de una muestra es aproximadamente la mitad de su número de bromo.
Combustibles
En los motores de combustión los alquenos presentes en la gasolina pueden polimerizar formando gomas y barnices que se depositan en las paredes del sistema, filtros y tuberías finas tapándolos.
Esto puede resultar en disminución del flujo de combustible, reducción de la potencia del motor e incluso impedir que este arranque.


Por estas razones es importante la determinación de olefinas en algunos derivados del petróleo, al menos de forma cualitativa con estos ensayos.
Referencias
- Sadeghbeigi, R. (2012). FCC Feed Characterization. Bromine Number and Bromine Index. In Fluid Catalytic Cracking Handbook. Chapter 3. (Third Edition). Recuperado de sciencedirect.com.
- Marczenko, Z. and Balcerzak, M. (2000). Separation, Preconcentration and Spectrophotometry in Inorganic Analysis. In Analytical Spectroscopy Library. Recuperado de sciencedirect.com.
- Wikimedia Foundation. (2020). Bromine test. Recuperado de en.wikipedia.org.
- Saikia, I. et al. (2016). Use of Bromine and Bromo-Organic Compounds in Organic Synthesis. Chemical Reviews 2016, 116, 12, 6837-7042. Recuperado de pubs.acs.org.
- Morrison, R.T. and Boyd, R.N. (2002). Organic Chemistry. 6th Edition. Prentice-Hall.
- Mettler Toledo. ASTM D1159 Bromine Number of Petroleum Products – Mettler Toledo. Recuperado de mt.com.
- ASTM D2710-09 (2018). Standard Test Method for Bromine Index of Petroleum Hydrocarbons by Electrometric Titration. Recuperado de astm.org.
- ASTM D1159-07 (2017). Standard Test Method for Bromine Numbers of Petroleum Distillates and Commercial Aliphatic Olefins by Electrometric Titration. Recuperado de astm.org.
- Metrohm AG. (2018). Application Bulletin 177/5 e. Automatic determination of the bromine number and the bromine index in petroleum products. Recuperado de metrohm.com.