¿Qué es la troponina?
La troponina es una proteína presente en el músculo esquelético y cardíaco de los vertebrados, asociada con los filamentos, en las fibras musculares y con funciones en la regulación de la actividad contráctil (contracción y relajación muscular).
Las fibras musculares son las células que componen el tejido muscular, cuya capacidad de contracción se basa en la interacción entre unos filamentos que se encuentran ordenados y estrechamente asociados en su interior, ocupando la mayor parte del volumen citoplásmico.
Estos filamentos se conocen como miofilamentos, y hay dos clases: los gruesos y los delgados. Los filamentos gruesos están compuestos por moléculas de miosina II, mientras que los filamentos delgados son polímeros de actina globular o actina G en asociación con otras dos proteínas.
Tanto la actina como la miosina se encuentran también en otras células del cuerpo humano y otros organismos, aunque en menor proporción y participando en procesos diferentes, como la migración celular, la exocitosis, la citocinesis (durante la división celular) e incluso en el tráfico vesicular intracelular.
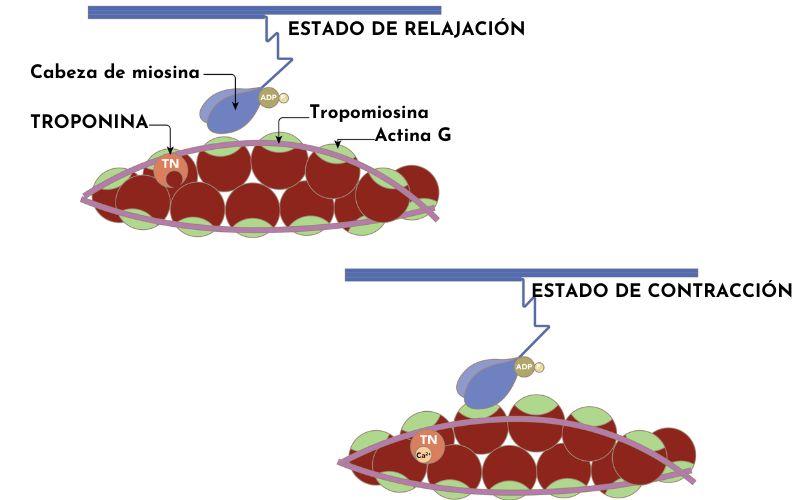
La troponina y la tropomiosina son las dos proteínas asociadas con los filamentos delgados de actina que participan en la regulación de los procesos de contracción y relajación de las miofibrillas de las células o fibras musculares.
Los mecanismos de acción a través de los cuales estas dos proteínas ejercen su función están relacionados con la concentración intracelular de calcio. El sistema de regulación de la troponina es uno de los sistemas mejor conocidos en la fisiología y bioquímica de la contracción del músculo esquelético.
Estas proteínas son de gran importancia para el organismo. En la actualidad se sabe a ciencia cierta que algunas cardiomiopatías familiares o congénitas son producto de mutaciones en la secuencia de los genes que codifican para alguna de las dos (troponina o tropomiosina).
Características de la troponina
- Ubicación. Se encuentra en el músculo cardíaco (miocardio) y en el músculo esquelético. Sin embargo, su papel principal y su importancia clínica radican en su presencia en el corazón.
- Función contráctil. En el músculo cardíaco, la troponina desempeña un papel esencial en la regulación de la contracción muscular. Junto con la tropomiosina, controla la interacción entre la actina y la miosina, lo que permite que las fibras musculares del corazón se contraigan de manera coordinada para bombear sangre.
- Marcador de daño cardíaco. La troponina se libera en la sangre cuando el tejido cardíaco se daña. Es un marcador altamente específico y sensible para detectar eventos cardíacos adversos, como un infarto de miocardio (ataque al corazón).
- Diagnóstico y pronóstico. La medición de la troponina ayuda a los médicos a confirmar o descartar un infarto de miocardio y a evaluar su gravedad. Los niveles elevados de troponina también pueden indicar otros problemas cardíacos, como angina inestable o insuficiencia cardíaca. Además, los niveles de troponina en sangre pueden usarse para predecir el pronóstico de un paciente después de un evento cardíaco.
- Clasificación. Esta proteína se compone de tres subunidades: troponina C, troponina I y troponina T. Las subunidades I y T son las más utilizadas como biomarcadores cardíacos. La troponina I (TnI) se considera la más específica para el daño cardíaco y se emplea con mayor frecuencia en los análisis de laboratorio.
Estructura de la troponina
La troponina es un complejo proteico compuesto por tres subunidades globulares diferentes, conocidas como troponina I, troponina C y troponina T, que juntas suman, más o menos, 78 kDa.
En el cuerpo humano existen variantes tejido-específicas para cada una de estas subunidades, diferenciadas entre sí tanto a nivel genético y molecular (con respecto a los genes que las codifican), como a nivel estructural (respecto a sus secuencias aminoacídicas).
La troponina C, o TnC, es la más pequeña de las tres y quizá una de las más importantes. Tiene 18 kDa de peso molecular y posee sitios para unirse al calcio (Ca2+).
La troponina T, o TnT, es la que posee los sitios de unión para anclar el complejo de las tres subunidades a la tropomiosina y tiene 30 kDa de peso molecular.
La troponina I, o TnI, de poco más de 180 residuos aminoacídicos, tiene el mismo peso molecular que la troponina T, pero en su estructura posee los sitios especiales para unirse a la actina, bloqueando la interacción entre esta última y la miosina, que es el fenómeno responsable de la contracción de las fibras musculares.
Muchos libros de texto se refieren a esta subunidad como la subunidad inhibitoria y como la “pega” molecular entre las tres subunidades de la troponina. Su capacidad de unión a la actina y su actividad inhibitoria son potenciadas por su asociación con la tropomiosina, mediada por la subunidad TnT.
Se ha demostrado que, en la subunidad I, la región de la secuencia encargada de la inhibición está definida por un péptido central de 12 residuos aminoacídicos entre las posiciones 104 y 115, y que la región C-terminal de la subunidad también tiene una función durante la inhibición.
Funciones de la troponina
- Regulación de la contracción muscular. Actúa como un interruptor molecular que regula la contracción muscular en el músculo cardíaco. Trabaja con la tropomiosina y la actina, para permitir o bloquear la interacción entre la miosina y la actina. Esta interacción es esencial para que las fibras musculares del corazón se contraigan de manera coordinada y eficiente.
- Control de la fuerza de contracción. Ayuda a controlar la fuerza con la que el músculo cardíaco se contrae. Cuando el corazón necesita bombear más sangre, se activa la troponina, lo que permite una contracción muscular más fuerte. Cuando se necesita una menor fuerza de contracción, la troponina desactiva la contracción muscular.
- Sensibilidad al calcio. Es especialmente sensible a la concentración de calcio en el citoplasma de las células musculares cardíacas. Cuando los niveles de calcio aumentan en respuesta a la estimulación eléctrica del corazón, la troponina cambia de forma y desencadena la contracción muscular al permitir que la miosina se una a la actina.
- Relajación muscular. Después de que la troponina permite la contracción muscular, también es esencial para el proceso de relajación del músculo cardíaco. Cuando los niveles de calcio disminuyen, la troponina vuelve a su estado original, lo que permite que la miosina se separe de la actina y el músculo se relaje.
- Mantenimiento del ritmo cardíaco. También está involucrada en la regulación del ritmo cardíaco al responder a señales eléctricas y químicas del sistema de conducción del corazón. Esto asegura que las contracciones cardíacas ocurran de manera coordinada y sincronizada.
Prueba de la troponina
La troponina es un excelente biomarcador para detectar lesiones cardíacas. Por ello, la prueba de la troponina es muy utilizada en el diagnóstico bioquímico, temprano y/o preventivo, de algunas condiciones patológicas cardíacas, como el infarto agudo de miocardio.
Muchos médicos consideran que esta prueba facilita la toma de decisiones con respecto a qué hacer y qué tratamiento administrar a los pacientes que presentan dolor en el pecho.
Por lo general, se relaciona con la detección de las subunidades T e I de la troponina, puesto que la isoforma de troponina C también se encuentra en los músculos esqueléticos de contracción lenta. Es decir, no es específica del corazón.
¿En qué se basa la prueba de la troponina?
Esta prueba suele ser un ensayo inmunológico que detecta las isoformas cardíacas de las subunidades T e I de la troponina. Se basa en las diferencias que existen entre ambas isoformas.
Isoforma de la subunidad troponina I (cTnI)
En el tejido muscular del miocardio existe solo una isoforma de la subunidad I de la troponina, caracterizada por la presencia de una “cola” postraduccional de 32 aminoácidos en su extremo N-terminal.
Esta isoforma se detecta por el desarrollo de anticuerpos monoclonales específicos que no reconocen otras isoformas no-cardíacas, puesto que la cola de aminoácidos es más o menos 50% diferente a los extremos de otras isoformas.
La cTnI no se expresa en tejidos dañados, sino que es exclusiva para el tejido cardíaco adulto.
Isoforma de la subunidad troponina T (cTnT)
La isoforma cardíaca de la subunidad T de la troponina está codificada en tres genes diferentes, cuyos ARNm pueden sufrir cortes y empalmes alternativos que dan como resultado la producción de isoformas con secuencias variables en los extremos N- y C-terminales.
A pesar de que el músculo cardíaco de los seres humanos contiene 4 isoformas de la TnT, solo una es característica del tejido cardíaco de un adulto. Esta es detectada con anticuerpos específicos diseñados contra el extremo N-terminal de su secuencia aminoacídica.
Las pruebas de “nueva generación” para la subunidad T de la isoforma cardíaca prestan mucha atención al hecho de que algunos tejidos musculares esqueléticos lesionados pueden re-expresar esta isoforma, por lo que se pueden obtener reacciones cruzadas con los anticuerpos.
Referencias
- Babuin, L., & Jaffe, A. S. Troponin: the biomarker of choice for the detection of cardiac injury. CMAJ.
- Farah, C., & Reinach, F. The troponin complex and regulation of muscle contraction. FASEB.
- Ross, M., & Pawlina, W. Histology. A Text and Atlas with correlated cell and molecular biology (5th ed.). Lippincott Williams & Wilkins.
- Wakabayashi, T. Mechanism of the calcium-regulation of muscle contraction. In pursuit of its structural basis. Proc. Jpn. Acad. Ser. B.