
¿Qué es la resistina?
La resistina, también conocida como factor secretor específico del tejido adiposo (ADSF por sus siglas en inglés), es una hormona peptídica rica en cisteína. Su nombre se debe a la resistencia que presenta ante la acción de la insulina. Es una citoquina que presenta de 10 a 11 residuos de cisteína.
Fue descubierta en 2001 en células del tejido adiposo de ratones y en células inmunes y epiteliales de seres humanos, perros, cerdos, ratas y otras varias especies de primates.
El papel que desempeña esta hormona ha sido muy controversial desde su descubrimiento, debido a su participación en la fisiología de la diabetes y la obesidad. También se conoce que tiene otras implicaciones médicas, como un aumento del colesterol malo y de lipoproteínas de baja densidad en las arterias.
Características de la resistina
– La resistina forma parte de una familia de moléculas del tipo resistina (Resistin like molecules, RELMs). Todos los miembros de la familia RELMs presentan una secuencia N-terminal, que presenta la señal de secreción que se encuentra entre 28 y 44 residuos.
– Tienen una zona o región central variable, con un extremo carboxilo terminal, de un dominio que varía entre 57 y unos 60 residuos, altamente preservados o conservados y abundantes en cisteína.
– Esta proteína ha sido encontrada en varios mamíferos. La mayor atención ha sido dirigida a la resistina secretada por ratones y la presente en humanos. Estas dos proteínas presentan de un 53 a un 60% de semejanza (homologías) en sus secuencias de aminoácidos.
En ratones
– En estos mamíferos, la principal fuente de resistina son las células adipositarias o el tejido adiposo blanco.
– La resistina en ratones es rica en cisteína de 11 kDa. El gen de esta proteína está ubicado en el octavo (8) cromosoma. Es sintetizado como un precursor de 114 aminoácidos.
– También presentan una secuencia señal de 20 aminoácidos y un segmento maduro de 94 aminoácidos.
– Estructuralmente, la resistina en ratones tiene cinco enlaces disulfuros y múltiples giros β. Puede formar complejos de dos moléculas idénticas (homodímeros) o formar proteínas con estructuras cuaternarias (multímeros) de distintos tamaños gracias a los enlaces disulfuro y no disulfuro.
En humanos
– La resistina humana se caracteriza por ser, al igual que en ratones u otros animales, una proteína peptídica rica en cisteína, solo que en humanos es de 12 kDa, con una secuencia madura de 112 aminoácidos.
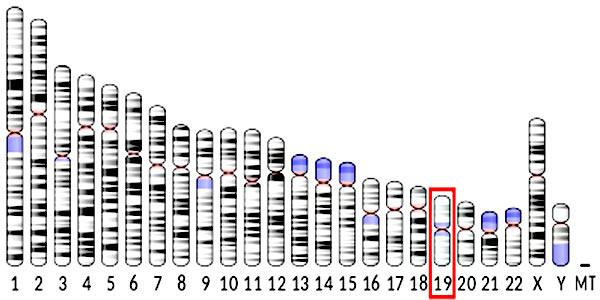
– El gen de esta proteína se encuentra en el cromosoma 19. La fuente de resistina en humanos son las células macrófagas (células del sistema inmunológico) y el tejido epitelial. Circula en la sangre como una proteína dimérica de 92 aminoácidos unidos por enlaces disulfuros.
Sinonimias
La resistina es conocida por múltiples nombres, entre los que destacan: proteína FIZZ3 secretada rica en cisteína (Cysteine-rich secreted protein FIZZ3, en inglés), factor de secreción especifico del tejido adiposo ADSF (Adipose tissue-specific secretory factor, ADSF), proteína rica en cisteína secretada mieloide específica C/EBP-epsilon-regulada (C/EBP-epsilon-regulated myeloid-specific secreted cysteine-rich protein), proteína rica en cisteína secretada A12-alpha-like 2 (Cysteine-rich secreted protein A12-alpha-like 2), RSTN, XCP1, RETN1, MGC126603 y MGC126609.
Descubrimiento
Esta proteína es relativamente nueva para la comunidad científica. Fue descubierta independientemente por tres grupos de científicos a principios de este siglo, quienes le pusieron distintos nombres: FIZZ3, ADSF y resistina.
FIZZ3
Fue descubierta en el 2000, en tejido de pulmón inflamado. Fueron identificados y descritos tres genes de ratones y dos genes homólogos de humanos asociados con la producción de esta proteína.
ADSF
Proteína descubierta en el 2001, gracias a la identificación de un factor de secreción rico en cistina (Ser/Cys) (ADSF) específico del tejido lipídico blanco (adipositos).
A esta proteína le asignaron un papel importante en el proceso de diferenciación de células múltipotenciales a adipositos maduros (adipogénesis).
Resistina
También en el 2001, un grupo de investigadores describió en el tejido lipídico maduro de ratones la misma proteína rica en cistina, a la que llamaron resistina por su resistencia a la insulina.
Estructuras
Estructuralmente, se conoce que esta proteína está constituida por una zona anterior o cabeza de forma laminar, y una zona posterior (cola) con forma helicoidal, formando oligómeros de distintos pesos moleculares, según sea humano o de otro origen.
Presenta una región central con 11 residuos de Ser/Cys (Serina/Cisteína) y un área también rica en Ser/Cys cuya secuencia es CX11CX8CXCX3CX10CXCXCX9CCX3-6, en donde C es Ser/Cys y X es cualquier aminoácido.
Tiene una composición estructural considerada como inusual, ya que está formada por varias subunidades unidas por interacciones no covalentes, es decir, no emplean electrones, sino variaciones dispersas electromagnéticas para conformar su estructura.
Funciones
Las funciones de la resistina, hasta la fecha, son objeto de un amplio debate científico. Entre los hallazgos más relevantes de los efectos biológicos en humanos y ratones están:
– Múltiples tejidos en humanos y ratones reaccionan a la resistina, incluyendo células hepáticas, musculares, cardiacas, inmunes y adiposas.
– Los ratones hiperresistinémicos (es decir, con niveles elevados de resistina) experimentan alteración en la autorregulación (homeostasis) de la glucosa.
– La resistina disminuye la captación de glucosa estimulada por la insulina en las células del músculo cardiaco (corazón).
– En células inmunes (macrófagos) en humanos, la resistina induce la producción de proteínas que coordinan la respuesta del sistema inmunológico (citoquinas inflamatorias).
Enfermedades
En seres humanos se piensa que esta proteína contribuye fisiológicamente en la resistencia de la diabetes mellitus a la insulina.
Aún se desconoce el papel que juega en la obesidad, aunque se ha encontrado que existe una correlación entre el aumento del tejido adiposo y los niveles de resistina, es decir, la obesidad aumenta la concentración de resistina en el organismo. También ha sido demostrado que es la responsable de elevados niveles de colesterol malo en la sangre.
La resistina modula las vías moleculares en patologías inflamatorias y autoinmunes. Causa directamente la alteración funcional del endotelio, que a su vez conduce al endurecimiento de las arterias, también conocida como ateroesclerosis.
La resistina funciona como un indicador de enfermedades, e incluso como una herramienta clínica predictiva para enfermedades cardiovasculares. Está involucrada en la producción de vasos sanguíneos (angiogénesis), trombosis, asma, enfermedad del hígado graso no alcohólico, enfermedad renal crónica, entre otras.
Referencias
- Resistin human. Recuperado de prospecbio.com.
- S. Abramson. Resistin. Recuperado de collab.its.virginia.edu
- Resistin. Recuperado de en.wikipedia.org.