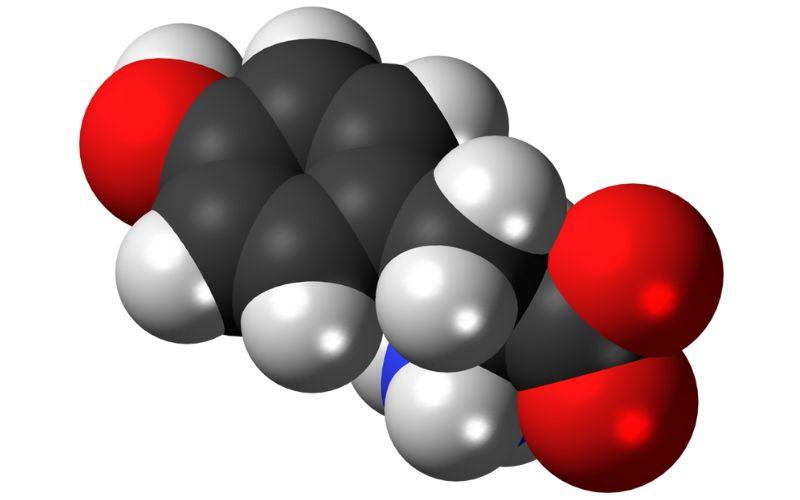
¿Qué es la tirosina?
La tirosina es uno de los 22 aminoácidos que conforman las proteínas de todas las células presentes en los seres vivos. A diferencia de otros aminoácidos, como la valina, la treonina, el triptófano, la leucina, la lisina y otros, la tirosina es un aminoácido “condicionalmente” esencial.
El nombre deriva del vocablo griego tiros, que significa queso, pues este aminoácido fue descubierto por primera vez en dicho alimento. El término fue acuñado en 1846 por Liebig, quien mezcló queso con hidróxido de potasio y obtuvo un compuesto desconocido, difícilmente soluble en agua.
Luego de la descripción inicial, otros investigadores, como Warren de la Rue y Hinterberger la obtuvieron a partir de insectos cocoideos y de proteínas de cuernos, respectivamente. Su separación a partir de la hidrólisis de otras proteínas con ácido hidroclórico fue descrita en 1901 por Mörner.
Generalmente, este aminoácido es obtenido en los mamíferos gracias a la hidroxilación de la fenilalanina, aunque también es absorbida en el intestino a partir de las proteínas consumidas con los alimentos.
La tirosina tiene múltiples funciones en el organismo, entre las más relevantes son, tal vez, la de ser sustrato para la producción de neurotransmisores y hormonas como la adrenalina y la hormona tiroidea.
Características de la tirosina
– Química. Es un aminoácido aromático, es decir, contiene un anillo bencénico en su estructura.
– Fórmula. Su fórmula molecular es C₉H₁₁NO₃.
– Polaridad. Aminoácido polar debido al grupo hidroxilo (-OH) en el anillo bencénico, lo que permite que participe en enlaces de hidrógeno y se disuelva en agua.
– Isomería. Existe en dos formas enantioméricas: L-tirosina (forma biológicamente activa) y D-tirosina. La L-tirosina es la que se encuentra en las proteínas de los seres vivos.
– Precursor metabólico. Precursora de varios compuestos importantes, como las catecolaminas (dopamina, norepinefrina y epinefrina), la hormona tiroidea y la melanina.
Estructura de la tirosina
Como el resto de los aminoácidos, la tirosina, o el ácido β-parahidroxifenil-α-amino propiónico, es un α-aminoácido que posee un átomo de carbono central, denominado carbono α, que es quiral, pues está unido a cuatro átomos o moléculas sustituyentes diferentes.
Este carbono quiral está unido a dos grupos característicos de los aminoácidos: un grupo amino (NH2) y un grupo carboxilo (COOH). También comparte uno de sus enlaces con un átomo de hidrógeno y el enlace restante está ocupado por el grupo R, o cadena lateral, propio de cada aminoácido.
En el caso de la tirosina, este grupo consiste en un anillo aromático asociado con un grupo hidroxilo (OH), que le da la capacidad de formar puentes de hidrógeno con otras moléculas y que le otorga características funcionales esenciales para ciertas enzimas.
Funciones de la tirosina
- Síntesis de neurotransmisores. Es un precursor esencial en la síntesis de las catecolaminas, que incluyen dopamina, norepinefrina (noradrenalina) y epinefrina (adrenalina). Estos neurotransmisores son fundamentales para la regulación del estado de ánimo, la respuesta al estrés y las funciones cognitivas.
- Producción de hormonas tiroideas. Es vital para la síntesis de las hormonas tiroideas T3 (triyodotironina) y T4 (tiroxina), que regulan el metabolismo, la temperatura corporal y el crecimiento y desarrollo.
- Metabolismo de proteínas. Como aminoácido, es un componente esencial de las proteínas, y participa en la síntesis y degradación de proteínas en el cuerpo.
- Formación de melanina. Es precursora de la melanina, pigmento responsable de la coloración de la piel, el cabello y los ojos. La tirosinasa, una enzima que cataliza la conversión de tirosina en melanina, es central en este proceso.
- Síntesis de coenzimas. Contribuye a la síntesis de coenzimas importantes, como la coenzima Q10, que juega un rol indispensable en la producción de energía celular a través de la cadena de transporte de electrones en las mitocondrias.
- Procesos cognitivos. Puede mejorar la función cognitiva en situaciones de estrés o fatiga al aumentar la disponibilidad de neurotransmisores como dopamina y norepinefrina en el cerebro.
- Funciones en las plantas. La tirosina y algunos de los intermediarios generados durante su biosíntesis, alimentan las rutas biosintéticas de metabolitos especializados en la defensa, en la atracción de los polinizadores, en el transporte electrónico y en el soporte estructural.
Biosíntesis de la tirosina
- En el ser humano. La tirosina se obtiene de la dieta o sintetizada en un solo paso por las células hepáticas a partir de la fenilalanina, un aminoácido esencial, a través de la reacción catalizada por el complejo enzimático fenilalanina hidroxilasa. Este complejo tiene actividad oxigenasa y solo está presente en el hígado humano o de otros mamíferos. La reacción de síntesis de tirosina implica la transferencia de un átomo de oxígeno a la posición para del anillo aromático de la fenilalanina. Dicha reacción ocurre al mismo tiempo que se forma una molécula de agua por la reducción de otro átomo de oxígeno molecular y el poder reductor es aportado directamente por un NADPH conjugado con una molécula de tetrahidropterina, semejante al ácido fólico.
- Biosíntesis en plantas. En las plantas, la tirosina es sintetizada de novo aguas abajo de la ruta del “shikimato”, que alimenta otras rutas biosintéticas de otros aminoácidos aromáticos, como la fenilalanina y el triptófano. En estos organismos, la síntesis parte de un compuesto conocido como “corismato”, producto final de la ruta del shikimato, y, además, el precursor común para todos los aminoácidos aromáticos, ciertas vitaminas y hormonas vegetales. El corismato es convertido en prefenato por la acción catalítica de la enzima corismato mutasa y es este el primer paso “comprometido” en la síntesis de la tirosina y la fenilalanina en las plantas. El prefenato es convertido en tirosina por una descarboxilación oxidativa y una transaminación, que pueden ocurrir en cualquier orden. En una de las rutas biosintéticas, estos pasos pueden ser catalizados por enzimas específicas, conocidas como tirosina deshidrogenasa prefenato-específica (PDH) (que convierte el prefenato en 4-hidroxifenilpiruvato (HPP)) y tirosina aminotransferasa (que produce la tirosina a partir del HPP), respectivamente. Otra vía de síntesis de tirosina a partir de prefenato implica la transaminación del prefenato a un aminoácido no proteinogénico llamado L-arogenato, catalizada por la enzima prefenato aminotransferasa. El L-arogenato es posteriormente sometido a una descarboxilación oxidativa para formar tiroxina, reacción dirigida por una enzima tirosina deshidrogenasa arogenato-específica, conocida también como ADH. Las plantas emplean preferencialmente la ruta del arogenato, mientras que la mayoría de los microbios sintetizan tirosina a partir del HPP derivado del prefenato.
Degradación de la tirosina
La degradación o el catabolismo de la tirosina resulta en la formación de fumarato y acetoacetato. El primer paso de esta ruta consiste en la conversión del aminoácido en 4-hidroxifenilpiruvato por una enzima citosólica conocida como tirosina aminotransferasa.
Este aminoácido también puede ser transaminado en las mitocondrias de los hepatocitos por una enzima aspartato aminotransferasa, aunque esta enzima no es muy importante en condiciones fisiológicas normales.
A través de la degradación de la tirosina puede producirse succinil-acetoacetato, que puede ser descarboxilado a succinil-acetato. El succinil-acetato es el más potente inhibidor de la enzima responsable de la síntesis del grupo hemo, la enzima ácido 5-aminolevulínico deshidratasa.
- Síntesis de adrenalina y noradrenalina. La tirosina es uno de los sustratos principales para la síntesis de dos neurotransmisores muy importantes para el cuerpo humano: la adrenalina y la noradrenalina. Esta es empleada inicialmente por una enzima conocida como tirosina hidroxilasa, capaz de añadir un grupo hidroxilo adicional al anillo aromático del grupo R de la tirosina, con lo que se forma el compuesto conocido como dopa. La dopa da lugar a la dopamina, una vez procesada enzimáticamente por una enzima dopa descarboxilasa, que remueve el grupo carboxilo del aminoácido de partida y que amerita de una molécula de fosfato piridoxal (FDP). La dopamina, posteriormente, es convertida en noradrenalina por acción de la enzima dopamina β-oxidasa, que cataliza la adición de un grupo hidroxilo al -CH que formaba parte del grupo R de la tirosina y que funcionaba de “puente” entre el anillo aromático y el carbono α. La adrenalina deriva de la noradrenalina por acción de la feniletanolamina N-metiltransferasa, que se encarga de la transferencia S-adenosil-metionina-dependiente de un grupo metilo (-CH3) al grupo amino libre de la noradrenalina.
Alimentos ricos en tirosina
La tirosina es un aminoácido “condicionalmente” esencial, pues es sintetizado en el cuerpo humano por hidroxilación de la fenilalanina, un aminoácido esencial.
Por lo tanto, si la ingesta de fenilalanina cubre las demandas corporales, la tirosina no es un factor limitante para el funcionamiento normal de las células. La tirosina, sin embargo, es adquirida también a partir de las proteínas que se consumen con los alimentos diarios.
Algunos estudios reportan que la ingesta diaria mínima tanto de tirosina como de fenilalanina debe estar entre los 25 y los 30 mg por kilogramo de peso, por lo que una persona promedio debería consumir más o menos 875 mg de tirosina por día.
Los alimentos con mayor contenido de tirosina son el queso y la soja. También están la carne de res, cordero, cerdo, pollo y pescado.
Algunas semillas y frutos secos como las nueces también confieren aportes significativos de este aminoácido, así como los huevos, los productos lácteos, los granos y los cereales.
Beneficios de la ingesta de tirosina
La tirosina se consume normalmente en forma de suplementos dietéticos o nutricionales, específicamente para el tratamiento de la patología conocida como fenilcetonuria, que sufren los pacientes incapaces de procesar adecuadamente la fenilalanina y, por lo tanto, no producen tirosina.
Se piensa que un aumento en la cantidad de tirosina consumida diariamente puede mejorar las funciones cognitivas relacionadas con el aprendizaje, la memoria y el estado de alerta en condiciones estresantes, pues su catabolismo está relacionado con la síntesis de los neurotransmisores adrenalina y noradrenalina.
Algunas personas toman comprimidos ricos en tirosina para mantenerse alertas durante el día si han perdido una cantidad importante de horas de sueño.
Como este aminoácido participa en la formación de la hormona tiroidea, su consumo puede tener efectos positivos en la regulación metabólica sistémica.
Trastornos por deficiencia de tirosina
El albinismo y la alcaptonuria son dos patologías relacionadas con el metabolismo de la tirosina. La primera condición tiene que ver con la síntesis defectuosa de melanina a partir de tirosina, y la segunda con defectos en la degradación de la tirosina.
El albinismo se caracteriza por la falta de pigmentación en la piel, es decir, los pacientes que lo padecen tienen el cabello blanco y piel rosácea, pues la melanina es el pigmento encargado de proporcionar el color a estas estructuras.
Esta patología tiene que ver con una deficiencia en la enzima tirosinasa específica de los melanocitos, la responsable de convertir la tirosina en DOPA-quinona, un intermediario en la síntesis de la melanina.
Los síntomas de la alcaptonuria son evidentes como una pigmentación exagerada de la orina (oscura) y artritis de desarrollo tardío.
Otras patologías metabólicas
Existen otros desórdenes relacionados con el metabolismo de la tirosina, entre los que están:
- Tirosinemia hereditaria de tipo I: caracterizada por una degeneración hepática progresiva y disfunción renal.
- Tirosinemia hereditaria de tipo II, o síndrome de Richner-Hanhart: que es evidente como una queratitis y lesiones ampulares en las palmas de las manos y las plantas de los pies.
- Tirosinemia tipo III: que puede ser asintomática o presentarse como retrasos mentales.
- Hawkinsinuria: caracterizada por acidosis metabólica en la infancia y por la incapacidad de prosperar en el crecimiento.
También existen otros defectos innatos en el metabolismo de la tirosina que tienen que ver con deficiencias en las enzimas encargadas de su degradación, como por ejemplo, la tirosina hidroxilasa, encargada del primer paso de la síntesis de la dopamina a partir de tirosina.
Referencias
- Aders Plimmer, R. The Chemical Constitution of The Proteins. Part I. Longmans, Green, and CO.
- Nelson, D.L., Cox, M.M. Lehninger Principios de Bioquímica. Ediciones Omega (5th ed.).
- Van de, G. Tyrosine. Recuperado de healthline.com.
- Tyrosine. Recuperado de webmd.com.
- Whitbread, D. Tyrosine. Recuperado de myfooddata.com.