¿Qué son los hidrocarburos alifáticos?
Los hidrocarburos alifáticos son compuestos orgánicos de carbono e hidrógeno cuyo carácter carece de aromaticidad. Clasificar los hidrocarburos de este modo resulta ambiguo e impreciso, pues no discrimina entre varios tipos de hidrocarburos que no son aromáticos.
Así, hay hidrocarburos alifáticos e hidrocarburos aromáticos. Estos últimos se reconocen por su unidad básica: el anillo bencénico. Los otros, en cambio, pueden adoptar cualquier estructura molecular: lineal, ramificada, cíclica, insaturada, policíclica; siempre y cuando no tengan sistemas conjugados como el del benceno.
El término ‘alifático’ deriva del griego aleiphar, que significa grasa, utilizada también para referirse a los aceites. Por lo tanto, en el siglo XIX se les asignó esta clasificación a los hidrocarburos obtenidos de los extractos aceitosos, mientras que los hidrocarburos aromáticos se extraían de resinas arbóreas y fragantes.
No obstante, a medida que se consolidaron las bases de la química orgánica, se descubrió que había una propiedad química que diferenciaba a los hidrocarburos, aún más importante que sus fuentes naturales: la aromaticidad (y no la fragancia).
De esta manera, los hidrocarburos alifáticos dejaron de ser únicamente los obtenidos de las grasas, para ser todos aquellos carentes de aromaticidad. En esta familia están los alcanos, alquenos y alquinos, sin importar que sean lineales o cíclicos. Por eso, ‘alifático’ se considera impreciso, aunque útil para abordar algunos aspectos generales.
Por ejemplo, cuando se dice ‘extremos’ o ‘cadenas’ alifáticos, se alude a regiones moleculares donde están ausentes los anillos aromáticos. De todos los hidrocarburos alifáticos, el más simple por definición es el metano, CH4; y el benceno es el más simple de los hidrocarburos aromáticos.
Propiedades de los de los hidrocarburos alifáticos
- Propiedades generales. Son compuestos formados solo por carbono e hidrógeno. Presentan cadenas abiertas, que pueden ser lineales o ramificadas. Pueden encontrarse en estado gaseoso, líquido o sólido, dependiendo del número de carbonos. Poseen baja densidad (menor que la del agua). Son poco solubles en agua, pero solubles en disolventes orgánicos como el éter o el benceno. Tienen olores característicos, que varían según su tamaño y tipo de enlace. Son inflamables y al arder liberan gran cantidad de energía.
- Propiedades físicas. El punto de ebullición y de fusión aumenta a medida que crece la cadena carbonada. Los de cadena corta suelen ser gases; los de cadena intermedia, líquidos; y los de cadena larga, sólidos. Son menos densos que el agua, por eso flotan sobre ella.
- Propiedades químicas. Pueden ser saturados (alcanos) o insaturados (alquenos y alquinos). Los alcanos son poco reactivos, pero pueden sufrir combustión y sustitución. Los alquenos y alquinos son más reactivos, participando en reacciones de adición. Todos los hidrocarburos alifáticos son combustibles y producen dióxido de carbono y agua al quemarse (si hay suficiente oxígeno).
Nomenclatura de los hidrocarburos alifáticos
La nomenclatura de los hidrocarburos difiere todavía más que sus propiedades. Si son alcanos, alquenos o alquinos, se sigue las mismas normas estipuladas por la IUPAC: seleccionar la cadena más larga, asignando los números indicadores más bajos al extremo más sustituido o a los heteroátomos o grupos más reactivos.
De esta manera se sabe en qué carbono se encuentra cada sustituyente, o inclusive las insaturaciones (dobles o triple enlaces). Para el caso de los hidrocarburos cíclicos, el nombre viene precedido por los sustituyentes enumerados en orden alfabético, seguidos de la palabra ‘ciclo’, contando los números de carbonos que lo integran.
Por ejemplo, considérese los dos ciclohexanos siguientes:
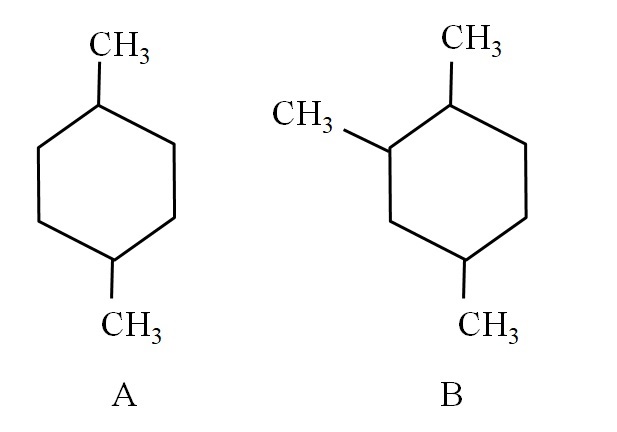
El ciclohexano A se llama 1,4-dimetilciclohexano. Si el anillo fuera de cinco carbonos, sería el 1,4-dimetilciclopentano. El ciclohexano B se llama 1,2,4-trimetilciclohexano, y no 1,4,6-ciclohexano, pues se busca utilizar los indicadores más bajos.
Ahora bien, la nomenclatura puede tornarse muy complicada para los hidrocarburos de estructuras estrambóticas. Para ellos existen reglas más específicas, que deben explicarse por separado y detenidamente, como sucede con los dienos, terpenos, polienos y los compuestos policíclicos.
Reacciones de los hidrocarburos alifáticos
- Combustión. Por suerte, las reacciones son menos variadas para estos hidrocarburos. Una de ellas ya se mencionó: combustionan fácilmente, produciendo dióxido de carbono y agua, además de otros óxidos o gases, dependiendo de la presencia de heteroátomos (Cl, N, P, O, etc.). Sin embargo, el CO₂ y H₂O son los productos principales de la combustión.
- Adición. Si presentan insaturaciones pueden sufrir reacciones de adición; es decir, incorporan moléculas pequeñas a su esqueleto como sustituyentes siguiendo un mecanismo específico. Entre estas moléculas están la del agua, el hidrógeno y los halógenos (F2, Cl2, Br2 y I2).
- Halogenación. Por otro lado, los hidrocarburos alifáticos bajo la incidencia de radiación ultravioleta (hv) y calor pueden romper enlaces C-H para cambiarlos por enlaces C-X (C-F, C-Cl, etc.). Esta es la reacción de halogenación, observada en alcanos de cadena muy corta, como el metano o pentano.
- Craqueo. Una reacción que pueden sufrir los hidrocarburos alifáticos, especialmente los alcanos de cadena larga. Consiste en el suministro de calor intenso para que la energía térmica rompa los enlaces C-C, y así se formen moléculas pequeñas, más cotizadas en el mercado de los combustibles, a partir de moléculas grandes.
Estas cuatro reacciones son las principales que puede sufrir un hidrocarburo alifático, siendo la combustión la más importante, pues no discrimina ningún compuesto: todos arderán en presencia de oxígeno, pero no todos adicionarán moléculas ni se romperán en moléculas pequeñas.
Tipos de hidrocarburos alifáticos
- Alcanos (saturados). Contienen solo enlaces simples (C-C). Su fórmula general es CₙH₂ₙ₊₂. Son los menos reactivos químicamente. Ejemplos: metano (CH₄), etano (C₂H₆), propano (C₃H₈), butano (C₄H₁₀).
- Alquenos (insaturados con doble enlace). Presentan uno o más enlaces dobles (C=C). Su fórmula general es CₙH₂ₙ. Son más reactivos que los alcanos. Ejemplos: eteno (C₂H₄), propeno (C₃H₆), buteno (C₄H₈).
- Alquinos (insaturados con triple enlace). Poseen uno o más enlaces triples (C≡C). Su fórmula general es CₙH₂ₙ₋₂. Son altamente reactivos debido a su enlace triple. Ejemplos: etino (acetileno, C₂H₂), propino (C₃H₄), butino (C₄H₆).
- Cicloalcanos (alifáticos cíclicos). Forman anillos cerrados de átomos de carbono, pero con enlaces simples, por lo que siguen siendo alifáticos (no aromáticos). Su fórmula general es CₙH₂ₙ. Ejemplos: ciclopropano (C₃H₆), ciclobutano (C₄H₈), ciclohexano (C₆H₁₂).
Usos de los hidrocarburos alifáticos
Nuevamente, los usos para estos hidrocarburos pueden variar dependiendo de cuál se considere. Sin embargo, en los apartados de propiedades y reacciones se dejó claro que todos combustionan, no solo para liberar moléculas gaseosas, sino también luz y calor. Así pues, son reservorios de energía, útiles para combustibles o fuentes de calor.
- Producción de fuego. Se utilizan como parte de la composición de la gasolina, para el gas natural, en los mecheros Bunsen, y en general para originar fuego. Uno de los ejemplos más destacables es el del acetileno, HC≡CH, cuya combustión permite excitar los iones metálicos de una muestra en la espectrometría de absorción atómica realizada en ensayos analíticos. Asimismo, el fuego resultante puede utilizarse para las soldaduras.
- Solventes. Los hidrocarburos alifáticos líquidos, como los parafínicos, se utilizan frecuentemente como solventes de grasas. Su acción disolvente puede utilizarse para remover manchas, esmaltes, pinturas, o sencillamente para preparar disoluciones de un compuesto orgánico determinado.
- Industria. Los de mayor masa molecular, ya viscosos o sólidos, se destinan para la elaboración de resinas, polímeros o medicinas.
Ejemplos de hidrocarburos alifáticos
Al principio se dijo que el metano es el más simple de los hidrocarburos alifáticos. Le siguen el propano, CH3CH2CH3, butano, CH3CH2CH2CH3, pentano, CH3CH2CH2CH2CH3, octano, nonano, decano, y así sucesivamente, teniendo alcanos cada vez más largos.
Lo mismo aplica para el etileno, CH2=CH2, propeno, CH3CH=CH2, buteno, CH3CH2CH=CH3, y para el resto de los alquinos. Si hay dos dobles enlaces, se trata de dienos, y si hay más de dos, polienos. Igualmente, puede haber dobles y triples enlaces en un mismo esqueleto, aumentando la complejidad estructural.
Entre los cicloalcanos podemos mencionar al ciclopropano, ciclobutano, ciclopentano, ciclohexano, cicloheptano, ciclooctano, así como el ciclohexeno y ciclohexino. De todos estos hidrocarburos se obtienen a su vez derivados ramificados, multiplicándose todavía más los ejemplos disponibles (como el 1,4-dimetilciclohexano).
De los terpenos más representativos tenemos al limoneno, el mentol, el pineno, la vitamina A, el escualeno, etc. El polietileno es un polímero saturado con unidades -CH2-CH2-, por lo que también es un ejemplo de estos hidrocarburos.
Referencias
- Morrison, R.T., Boyd, R.N. Química Orgánica. 5ta Edición. Editorial Addison-Wesley Interamericana.
- Carey, F. Química Orgánica (Sexta edición). McGraw Hill.
- Graham Solomons, T.W., Craig, B. Fryhle. Organic Chemistry. Amines (10th edition.). Wiley Plus.
- Helmenstine, A.M. Aliphatic Hydrocarbon Definition. Recuperado de thoughtco.com.
- Aliphatic compound. Recuperado de en.wikipedia.org.