¿Qué es el ácido gálico?
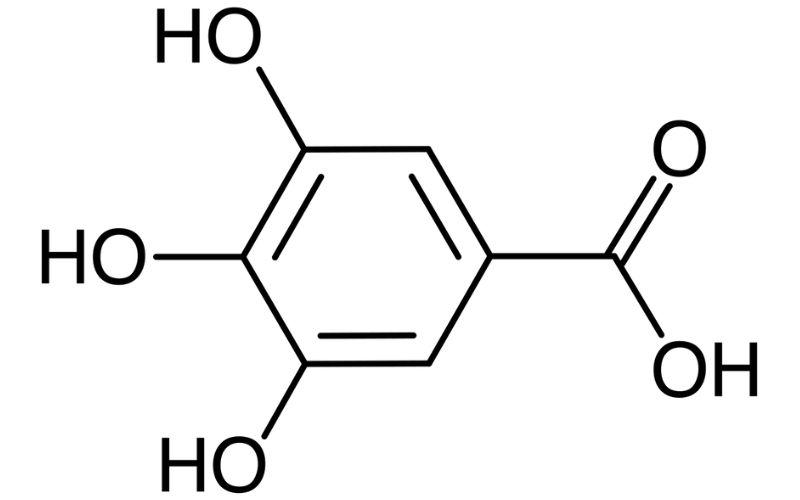
El ácido gálico es un compuesto orgánico de fórmula molecular C6H2(OH)3COOH, que pertenece a la categoría de los polifenoles. Tiene forma de polvo cristalino blanco cercano a amarillo pálido.
Es un ácido trihidroxibenzoico formado por un anillo bencénico al cual están unidos un grupo carboxílico ácido (-COOH) y 3 grupos hidroxilo (-OH) ubicados en las posiciones 3, 4 y 5 del anillo.
En la naturaleza se encuentra ampliamente diseminado, pues es un producto que se forma en cantidades importantes en plantas y hongos. Existe libre o unido a los taninos de la mayoría de especies vegetales, destacándose nueces, uvas, plantas de divi-divi, corteza de roble, granada o sus raíces, plantas de zumaque y té.
También se encuentra en la miel, el cacao, diversas bayas, el mango y otras frutas y vegetales, y en algunas bebidas como el vino y las infusiones de té.
En los tejidos vegetales está en forma de éster o galato. La cantidad que contiene depende de estímulos externos, como la cantidad de radiación UV que ha recibido la planta, estrés químico e infecciones microbianas.
En el caso de las uvas y el vino, depende de la variedad de uva, procesamiento y almacenaje. En el té verde es alto el contenido de galatos, pero el cacao contiene más que el té verde y el vino tinto.
Químicamente, se comporta como un agente reductor. Es astringente y antioxidante. Además, se ha empleado en tintas azules para escribir y se usa comúnmente en la industria farmacéutica.
Tiene amplio potencial en aplicaciones médicas, ya que las múltiples propiedades del ácido gálico y sus derivados lo convierten en un agente terapéutico prometedor en medicina preventiva.
Estructura del ácido gálico
El ácido gálico cristaliza en metanol absoluto o en cloroformo en forma de agujas blancas. Cristaliza en agua en forma de agujas sedosas de su monohidrato.
Nomenclatura del ácido gálico
- Ácido gálico.
- Ácido 3,4,5-trihidroxibenzoico.
Propiedades del ácido gálico
- Apariencia física. Sólido, agujas cristalinas.
- Peso molecular. 170,12 g/mol.
- Punto de fusión. Se descompone a 235-240 °C, generando pirogalol y CO₂
- Densidad. 1,694 g/cm3
- Solubilidad. En agua: moderadamente soluble (1 g en 87 ml de agua. 1 g en 3 ml de agua hirviendo). En etanol: 1 g en 6 ml de alcohol. En éter dietílico: 1 g en 100 ml de éter. En glicerol: 1 g en 10 ml. En acetona: 1 g en 5 ml. Prácticamente insoluble en benceno, cloroformo y éter de petróleo.
- Constante de disociación. K1 4,63 x 10-3 (a 30 °C). K2 1,41 x 10-9
- Propiedades químicas. Las soluciones de ácido gálico, particularmente de sales de metales alcalinos, absorben oxígeno y se vuelven marrones al exponerse al aire. Es un agente reductor fuerte que puede reducir sales de oro o plata al metal. Es incompatible con cloratos, permanganato, amoníaco, acetato de plomo, hidróxidos alcalinos, carbonatos alcalinos, sales de plata y agentes oxidantes en general. Con sales de hierro (II), el ácido gálico forma un complejo azul intenso. En el ácido gálico, el grupo hidroxilo (-OH) en la posición 4 es el más reactivo químicamente.
- Otras propiedades. Debe protegerse de la luz porque lo degrada fotoquímicamente.
- Toxicidad. Es un irritante local suave. La inhalación de polvo puede afectar a nariz y garganta y el contacto con ojos y piel causa irritación. Estudios en ratones indican que ingerido hasta un nivel de 5.000 mg/Kg, el ácido gálico no es tóxico para esos animales. Se considera de toxicidad baja y confirma la seguridad de su uso.
Obtención del ácido gálico
El ácido gálico se obtiene por hidrólisis alcalina o ácida de los taninos de nueces o materiales vegetales ricos en estos compuestos.
La hidrólisis también se puede efectuar de forma enzimática usando caldos de cultivo de mohos, como el Penicillium glaucum o el Aspergillus niger, que contienen tanasa, una enzima que rompe o escinde la molécula de tanino.
Otra forma de obtenerlo es a partir del ácido p-hidroxibenzoico, mediante sulfonación y fusión alcalina, con lo cual se logra la adición de los otros dos grupos -OH en la molécula.
Usos del ácido gálico
- Tintas y colorantes. Se emplea en la manufactura de antragalol y pirogalol, intermediarios en la producción de colorantes, como la galocianina y la galoflavina. A su vez, es materia prima en la síntesis de derivados de la oxazina, usados también como colorantes. Debido a que forma un complejo azul con hierro, el ácido gálico es muy importante en la producción de tintas para escribir. Estas tintas contienen principalmente una mezcla de ácido gálico, sulfato ferroso (FeSO4) y goma arábiga. Las tintas de hierro-acido gálico han sido materiales indispensables para la escritura de documentos, dibujo de planos y preparación de materiales escritos.
- Aplicaciones médicas. Se usa como astringente intestinal y agente para detener hemorragias (estíptico). El ácido gálico es materia prima para obtener rufigalol, un agente antimalárico. Por su capacidad química reductora, se emplea en la elaboración de productos farmacéuticos.
- Aplicaciones médicas potenciales contra el cáncer. El ácido gálico se ha identificado como principal responsable de las propiedades anticancerígenas de varios extractos de plantas. Al contrario de su particular acción antioxidante, se ha encontrado que puede presentar características pro-oxidantes en la inducción de apoptosis (muerte celular programada) de las células cancerígenas. Hay evidencias de que el ácido gálico y los galatos inducen la apoptosis selectiva en celdas de tumores de rápido crecimiento, dejando intactas las células sanas. Además, se ha reportado que frena la angiogénesis, y consecuentemente, la invasión del cáncer y la metástasis. Se ha encontrado actividad anticancerígena del ácido gálico en leucemia, cáncer de próstata, pulmón, estómago, páncreas y colon, cáncer de senos, cervical y esofágico.
- Contra diversas patologías. En varios estudios se ha demostrado que posee actividad antifungosa, antibacteriana, antiviral, antialérgica, antiinflamatoria, antimutagénica, anticolesterol, antiobesidad e inmunomodulatoria. Es un buen candidato para controlar la enfermedad periodontal (enfermedad de las encías). También exhibe potencial neuroprotector, cardioprotector, hepatoprotector y nefroprotector. Por ejemplo, en diversos estudios de tejidos del corazón en ratas se ha confirmado que el ácido gálico ejerce un efecto protector del miocardio contra el estrés oxidativo.
- Como agente antienvejecimiento celular. El ácido gálico proporciona protección eficiente contra el daño oxidativo causado por especies reactivas encontradas a menudo en sistemas biológicos, como los radicales hidroxilo (OH.), superóxido (O2.) y peroxilo (ROO.). Se ha determinado que en el tracto digestivo se absorbe más rápido que la mayoría de los polifenoles. Y es uno de los que presenta mayor capacidad antioxidante. Adicionalmente, algunos investigadores afirman que el ácido gálico puede ser transportado por niosomas para aumentar su actividad antienvejecimiento. El niosoma es un sistema molecular de liberación controlada de medicamentos en el lugar del organismo que lo requiera. Estas características le confieren un alto potencial contra el envejecimiento de las células.
- Usos veterinarios. Ha sido usado como astringente intestinal en animales.
- Diversas aplicaciones. El ácido gálico se usa en la manufactura de sus ésteres, como el galato de metilo, galato de propilo, galato de octilo y galato de laurilo. Estos derivados son ampliamente usados como antioxidantes y conservantes de alimentos procesados, en materiales para empaquetar alimentos, para prevenir ranciedad y deterioro oxidativo. Los derivados mencionados también se usan en cosméticos. El ácido gálico se emplea como revelador fotográfico y en la manufactura del papel. Además, se usa extensivamente en la estabilización del colágeno en el proceso de curtido de cuero. Como reactivo analítico, el ácido gálico es ideal como estándar para determinar el contenido fenólico de extractos de plantas, y los resultados se expresan como Equivalentes de Ácido Gálico. También se emplea en pruebas para determinación de ácidos minerales libres, dihidroxiacetona y alcaloides.
- Utilidad en ambientes acuáticos naturales. El ácido gálico, presente de forma natural en acuíferos en la materia vegetal, es uno de los responsables de la disponibilidad nutritiva del Fe (II), necesario para el crecimiento de especies acuáticas. Esto se debe a que es capaz de mantener altos niveles de concentración de hierro (II) disuelto bajo condiciones aeróbicas, pues forma un complejo con Fe (II) resistente a la oxidación.
Referencias
- Sajid, M. Nanoparticle-Based Delivery of Phytomedicines: Challenges and Opportunities. Recuperado de sciencedirect.com.
- Ullmann’s Encyclopedia of Industrial Chemistry. VCH Verlagsgesellschaft mbH.
- Badhani, B., Sharma, N., Kakkar, R. Gallic acid: A versatile antioxidant with promising therapeutic and industrial applications. Recuperado de rsc.org.
- Zanwar, A.A. Role of Gallic Acid in Cardiovascular Disorders. In Polyphenols in Human Health and Disease. Recuperado de sciencedirect.com.
- Nowak, R. Plant Polyphenols as Chemopreventive Agents. In Polyphenols in Human Health and Disease. Recuperado de sciencedirect.com.