¿Qué es el alosterismo?
El alosterismo, o regulación alostérica, es el proceso bioquímico donde la unión de una molécula a una proteína en un sitio distinto de su centro activo regula su actividad.
El término alostérico o alosterismo proviene de las raíces griegas allos, que quiere decir “otro”, y stereós, que significa “forma” o “lugar”, por lo que se traduce literalmente como “otro espacio”, “otro lugar” u “otra estructura”.
Algunos autores describen el alosterismo como un proceso por el cual sitios remotos en un sistema (la estructura de una enzima, por ejemplo) están acoplados energéticamente para producir una respuesta funcional, razón por la cual puede suponerse que un cambio en una región puede afectar a cualquier otra en el mismo.
Este tipo de regulación es típico de las enzimas que participan en múltiples procesos biológicos conocidos, como la transducción de señales, el metabolismo (anabolismo y catabolismo), la regulación de la expresión genética, entre otros.
Las primeras ideas sobre el alosterismo y su participación en el control del metabolismo celular fueron postuladas en la década de 1960 por F. Monod, F. Jacob y J. Changeux, mientras estudiaban las rutas biosintéticas de distintos aminoácidos, que eran inhibidas tras la acumulación de los productos finales.
Aunque la primera publicación al respecto tuvo que ver con la regulación genética, poco tiempo después Monod, Wyman y Changeux ampliaron la concepción de alosterismo a las proteínas con actividad enzimática y propusieron un modelo basado en proteínas multiméricas, sustentado principalmente en las interacciones entre las subunidades cuando cualquiera de estas se unía a un efector.
Muchos de los conceptos posteriores tuvieron sus basamentos en la teoría de “ajuste inducido”, introducida por Koshland unos años antes.
Aspectos generales del alosterismo
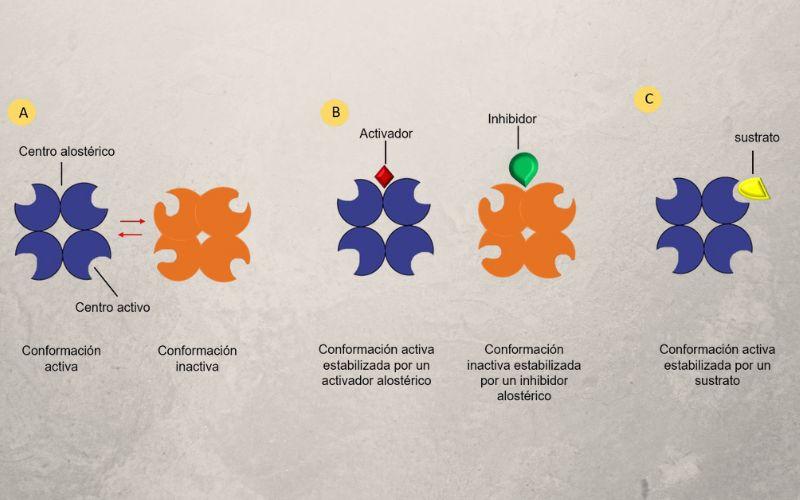
Por lo general, todas las enzimas poseen dos sitios diferentes para la unión de ligandos: uno se conoce como el sitio activo, al cual se unen las moléculas que funcionan como sustrato (responsable por la actividad biológica de la enzima), y el otro se conoce como sitio alostérico, que es específico para otros metabolitos.
Estos “otros metabolitos” se denominan efectores alostéricos y pueden tener efectos positivos o negativos en la velocidad de las reacciones catalizadas por las enzimas o en la afinidad con la que se unen a sus sustratos en el sitio activo.
Usualmente, la unión de un efector en el sitio alostérico de una enzima causa un efecto en otro sitio de la estructura, modificando su actividad o su desempeño funcional.
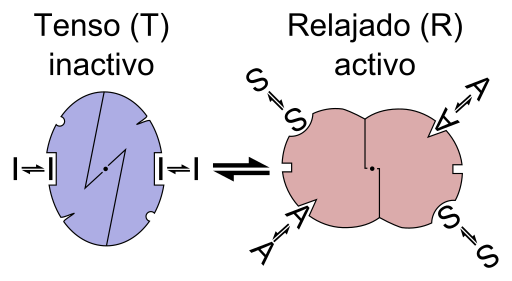
En otras palabras, la unión de un efector alostérico a su sitio específico en la estructura de una enzima provoca un cambio en la geometría molecular de la enzima, lo que se conoce como transición alostérica, es decir, es un evento que se transmite por toda la macromolécula, modificando su comportamiento.
El alosterismo puede ser homotrópico o heterotrópico. Un proceso de regulación alostérica homotrópica se define como aquel en el cual el mismo sustrato de una enzima actúa como su regulador alostérico, es decir, que el efector alostérico es el mismo sustrato; también se conoce como un tipo de cooperatividad.
Un proceso de regulación heterotrópica, por otra parte, se refiere a la regulación de la actividad de una enzima mediada por una molécula o efector alostérico que es diferente a su sustrato, y también puede tener efectos positivos o negativos sobre la actividad de la enzima.
Funciones del alosterismo
- Regular la actividad enzimática. Es su función principal. Permite aumentar o disminuir la velocidad de una reacción enzimática sin necesidad de alterar la concentración de la enzima. Según el tipo de efector, si activa la enzima es un activador alostérico. Si inhibe la enzima, es un inhibidor alostérico.
- Coordinar y equilibrar rutas metabólicas. Las enzimas alostéricas suelen encontrarse en puntos clave de las rutas metabólicas (como las etapas iniciales o de control). El alosterismo permite que el metabolismo sea eficiente, evitando gasto innecesario de energía o acumulación de productos. Facilita la retroalimentación negativa: el producto final de una ruta puede inhibir alostéricamente a la primera enzima de la vía, evitando la sobreproducción.
- Facilitar la cooperación entre subunidades (cooperatividad). En proteínas multisubunitarias, como la hemoglobina, el alosterismo permite una cooperatividad entre los sitios de unión. Cuando una molécula (por ejemplo, oxígeno) se une a una subunidad, cambia la conformación de las demás, facilitando su unión o liberación. Esto asegura una respuesta fisiológica ajustada a las condiciones del organismo (como el transporte de oxígeno).
- Permitir control rápido y reversible. A diferencia de los mecanismos que requieren síntesis o degradación de proteínas, el alosterismo actúa rápida y reversiblemente. Esto permite una adaptación inmediata a los cambios en las condiciones celulares (pH, concentración de metabolitos, temperatura, etc.).
- Integrar señales metabólicas. Las enzimas alostéricas pueden responder a múltiples efectores, integrando varias señales al mismo tiempo. Así, la célula puede coordinar diferentes vías metabólicas de manera simultánea (por ejemplo, activando una ruta y frenando otra).
Ejemplos de alosterismo
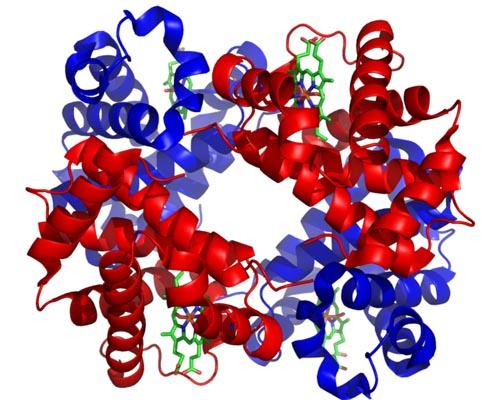
- Hemoglobina. Aunque existen miles de ejemplos de alosterismo o regulación alostérica en la naturaleza, algunos han sido más destacados que otros. Es el caso de la hemoglobina, una de las primeras proteínas descritas en profundidad en el aspecto estructural. La hemoglobina es una proteína muy importante para muchos animales, pues se encarga del transporte de oxígeno por la sangre desde los pulmones hacia los tejidos. Esta proteína presenta regulación alostérica homotrópica y heterotrópica al mismo tiempo. El alosterismo homotrópico de la hemoglobina tiene que ver con que la unión de una molécula de oxígeno a una de las subunidades que la componen afecta directamente la afinidad con la que se une la subunidad adyacente a otra molécula de oxígeno, incrementándola (regulación positiva o cooperativismo).
- Alosterismo heterotrópico. El alosterismo heterotrópico, por otra parte, se relaciona con los efectos que tienen tanto el pH como la presencia de 2,3-difosfoglicerato sobre la unión de oxígeno a las subunidades de esta enzima, inhibiéndola. La aspartato transcarbamilasa o ATCasa, que participa en la ruta de síntesis de las pirimidinas, también es uno de los ejemplos “clásicos” de regulación alostérica. Esta enzima, que tiene 12 subunidades, de las cuales 6 son catalíticamente activas y 6 son reguladoras, es inhibida heterotrópicamente por el producto final de la ruta que encabeza, la citidinatrifosfato (CTP).
- Operón lactosa de E. coli. El fruto de las primeras ideas de Monod, Jacob y Changeux fue un artículo publicado por Jacob y Monod relacionado con el operón lactosa de Escherichia coli, que es uno de los ejemplos típicos de regulación alostérica heterotrópica a nivel genético. La regulación alostérica de este sistema no se relaciona con la capacidad de conversión de un sustrato en un producto, sino con la afinidad de unión de una proteína a la región de ADN operadora.
Referencias
- Changeux, J.P., Edelstein, S.J. Allosteric mechanisms of signal transduction. Science.
- Goldbeter, A., Dupont, G. Allosteric regulation, cooperativity, and biochemical oscillations. Biophysical chemistry.
- Kern, D., Zuiderweg, E.R. The role of dynamics in allosteric regulation. Current opinion in structural biology.
- Laskowski, R.A., Gerick, F., Thornton, J.M. The structural basis of allosteric regulation in proteins. FEBS letters.
- Mathews, C.K., Van Holde, K.E., Ahern, K.G. Biochemistry, ed. San Francisco, Calif.