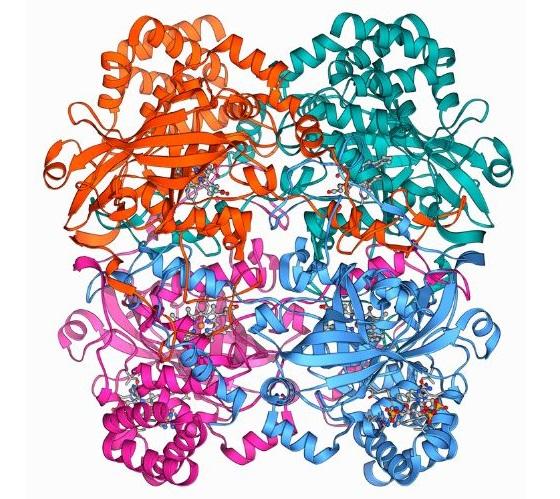
¿Qué es la catalasa?
La catalasa es una enzima oxidorreductasa (H2O2: H2O2 oxidorreductasa) ampliamente distribuida en la naturaleza. Cataliza, en diversos tejidos y tipos de células, la reacción de “descomposición” del peróxido de hidrógeno en oxígeno molecular y agua.
Las primeras observaciones de este tipo de enzima se remontan a comienzos de la década de 1810, pero fue en 1901 cuando Loew reconoció que la catalasa está presente virtualmente en todos los organismos vivos existentes y en múltiples tipos de células.
Esta enzima, crucial para el mantenimiento de la integridad celular y principal reguladora del metabolismo de peróxido de hidrógeno, fue un factor fundamental para afirmar que en la naturaleza existen enzimas que actúan sobre sustratos específicos.
Los mamíferos y otros organismos poseen enzimas catalasas que también pueden comportarse como peroxidasas, catalizando reacciones de oxidorreducción de diferentes sustratos utilizando el peróxido de hidrógeno.
En la mayor parte de los eucariotas, las enzimas catalasas se encuentran preponderantemente en orgánulos subcelulares conocidos como “peroxisomas”, y en los humanos existen numerosas condiciones patológicas relacionadas con la deficiencia de esta enzima.
Características de la catalasa
– Principal función. Esta enzima se encuentra en las células de la mayoría de los organismos aeróbicos, y su función principal es proteger las células del daño oxidativo causado por el peróxido de hidrógeno, un subproducto del metabolismo celular.
–Reacción. La reacción catalizada por la catalasa es la siguiente:
La enzima acelera esta descomposición del peróxido de hidrógeno en agua y oxígeno.
– Estructura y ubicación. Su estructura tridimensional es básica para su actividad catalítica. Se encuentra comúnmente en los peroxisomas, orgánulos celulares involucrados en el metabolismo de los lípidos y la desintoxicación celular.
– Protección celular. La descomposición del peróxido de hidrógeno es crucial porque este compuesto puede ser tóxico para las células y causar daño oxidativo. La catalasa ayuda a prevenir la acumulación de peróxido de hidrógeno y protege las células del estrés oxidativo.
– Ubicuidad. Se halla en una variedad de organismos, desde bacterias hasta plantas y animales. La presencia de esta enzima es indicativa de la adaptación evolutiva de los organismos para lidiar con el oxígeno y sus subproductos reactivos.
Estructura de la catalasa
- Codificación en humanos. La catalasa es codificada por un gen de 34 kb que posee 12 intrones y 13 exones y que codifica para una proteína de 526 aminoácidos.
- Forma. La mayoría de las catalasas estudiadas son enzimas tetraméricas.
- Peso molecular. Cercano a los 240 kDa (60 kDa por cada subunidad) y cada monómero está asociado con un grupo prostético hemina o ferroprotoporfirina.
- Estructura. Está conformada por cuatro dominios compuestos por estructuras secundarias constituidas por hélices alfa y láminas β-plegadas, y estudios realizados en la enzima del hígado de humanos y bovinos han demostrado que estas proteínas están unidas a cuatro moléculas de NADPH. Estas moléculas de NADPH no parecen esenciales para la actividad enzimática de la catalasa (para la producción de agua y oxígeno a partir de peróxido de hidrógeno), pero sí parece relacionarse con una disminución de la susceptibilidad de esta enzima frente a elevadas concentraciones de su tóxico sustrato.
- Dominios. Los dominios de cada subunidad en la catalasa de humanos son:
- Un brazo N-terminal extendido no-globular, que funciona para la estabilización de la estructura cuaternaria.
- Un β-barril de ocho láminas β-plegadas antiparalelas, que aportan algunos de los residuos de unión lateral al grupo hemo.
- Un dominio de “envoltura” que rodea el dominio exterior, incluyendo al grupo hemo.
- Un dominio con estructura de hélice alfa.
Las cuatro subunidades, con estos cuatro dominios, se encargan de la formación de un largo canal cuyo tamaño es crítico para el mecanismo de reconocimiento del peróxido de hidrógeno por la enzima (que emplea aminoácidos como histidina, asparragina, glutamina y ácido aspártico para ello).
Funciones de la catalasa
Según algunos autores, la catalasa cumple funciones enzimáticas:
- La descomposición del peróxido de hidrógeno en agua y oxígeno molecular (como una peroxidasa específica).
- La oxidación de donadores de protones, como el metanol, etanol, muchos fenoles y ácido fórmico, empleando un mol de peróxido de hidrógeno (como una peroxidasa inespecífica).
- Protección de la hemoglobina. En los eritrocitos, la gran cantidad de catalasa parece jugar un papel importante en la protección de la hemoglobina frente a agentes oxidantes, como el peróxido de hidrógeno, el ácido ascórbico, la metilhidracina y otros. La enzima presente en estas células se encarga de la defensa de otros tejidos con poca actividad catalasa frente a elevadas concentraciones de peróxido de hidrógeno.
- Defensa. Algunos insectos, como el escarabajo bombardero, usan la catalasa como mecanismo de defensa, pues descomponen el peróxido de hidrógeno y emplean el oxígeno gaseoso producto de dicha reacción para propulsar la salida de agua y otros compuestos químicos en forma de vapor.
- Respiración. En las plantas, la catalasa (también presente en los peroxisomas) es uno de los componentes del mecanismo de la fotorrespiración, durante el cual el fosfoglicolato producido por la enzima RuBisCO se emplea para la producción de 3-fosfoglicerato.
Patologías relacionadas con la catalasa en humanos
Las principales fuentes de producción del sustrato de la catalasa, el peróxido de hidrógeno, son las reacciones catalizadas por enzimas oxidasas, especies reactivas de oxígeno y algunas células tumorales.
Este compuesto está implicado en los procesos inflamatorios, en la expresión de moléculas adhesivas, en la apoptosis, en la regulación de la agregación de las plaquetas y en el control de la proliferación celular.
Cuando existen deficiencias de esta enzima se generan elevadas concentraciones de su sustrato, lo que produce lesiones en la membrana celular, defectos en el transporte electrónico, en las mitocondrias, en el metabolismo de la homocisteína y en el ADN.
Entre las enfermedades asociadas con mutaciones en el gen codificante para la catalasa de humanos se pueden mencionar:
- Diabetes mellitus.
- Hipertensión arterial.
- Alzheimer.
- Vitiligo y otras.
Referencias
- Agar, N., Sadrzadeh, S., Hallaway, P., & Eaton, J. Erythrocyte Catalase. A Somatic Oxidant Defense? J. Clin. Invest.
- Góth, L., Rass, P., & Páy, A. Catalase Enzyme Mutations and their Association with Diseases. Molecular Diagnosis.
- Kirkman, H. N., & Gaetani, G. F. Mammalian catalase: a venerable enzyme with new mysteries. Trends in Biochemical Sciences.
- Rawn, J. D. Biochemistry. Neil Patterson Publishers.
- Vainshtein, B., Melik-Adamyan, W., Barynin, V., Vagin, A., & Grebenko, A. Three-dimensional structure of the enzyme catalase. Nature.