Explicamos qué es el ciclo del nitrógeno, su función, características principales, etapas, e importancia.
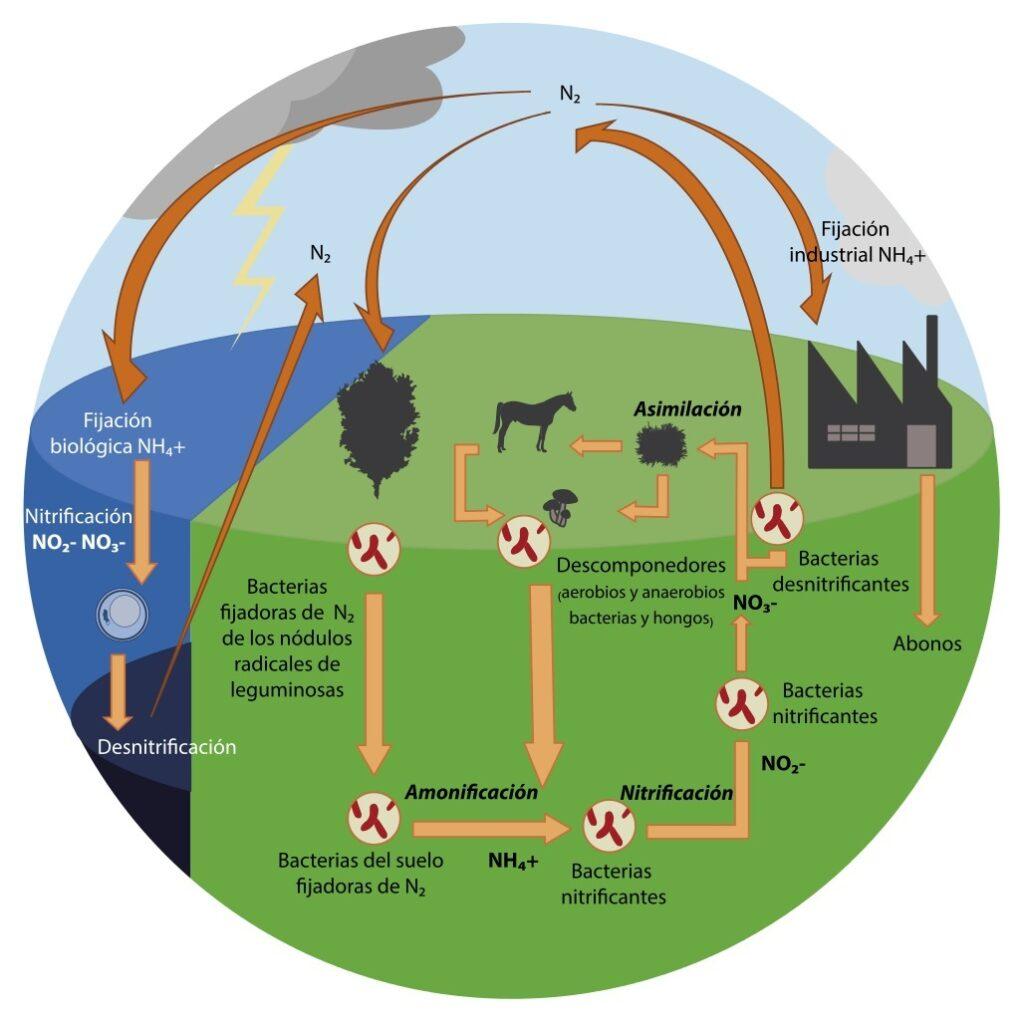
¿Qué es el ciclo del nitrógeno?
El ciclo del nitrógeno es el flujo de nitrógeno a través de la atmósfera, la tierra y los organismos vivos. El nitrógeno es un elemento importante para todos los seres vivos, ya que forma parte de las proteínas y otros compuestos fundamentales.
Sin embargo, este elemento no es utilizable por los seres vivos en su forma natural. En su lugar, deben realizar un proceso llamado fijación del nitrógeno para convertirlo en una forma que puedan utilizar. Esto ocurre cuando el nitrógeno es combinado con otros elementos para formar compuestos orgánicos, como los aminoácidos.
El nitrógeno va cambiando de estado a través de este ciclo. Cuando se encuentra en la atmósfera es un gas, mientras que en el suelo existe como óxido y dióxido de nitrógeno. Al ser utilizado como fertilizante es común que sea en forma de un gas incoloro llamado amoníaco.
En el ciclo del nitrógeno se pueden diferenciar cinco etapas: fijación, mineralización, nitrificación, inmovilización y desnitrificación. Otra división más sencilla se basa en cuatro fases principales: fijación, amonificación, nitrificación y desnitrificación.
Lo más importante del ciclo del nitrógeno es que circula a través de todos los elementos y organismos que hay en la naturaleza. Además, el nitrógeno es un componente esencial de las proteínas y de los ácidos nucleicos, por lo que su presencia es fundamental para la vida como la conocemos.
¿Cuál es la función del ciclo del nitrógeno?
El ciclo del nitrógeno es un ciclo natural que ayuda a los seres vivos a obtener nitrógeno. Los humanos y otros seres vivos necesitan nitrato para sobrevivir. Los animales comen plantas o carne de animales que han comido plantas para obtener nitratos. Las plantas utilizan el nitrato para crecer y producir frutos y verduras.
Características del ciclo del nitrógeno
– El nitrógeno es un recurso imprescindible para la vida, pero inaccesible para los organismos, si se conservara en la forma en la que se encuentra en la atmósfera.
– A través del ciclo del nitrógeno, este elemento se convierte en amoníaco, que queda disponible para los organismos vegetales.
– Al quedar disponible para los productores primarios, es decir, las plantas, se puede utilizar para generar proteínas, ADN y algunos otros compuestos que son muy importantes para las funciones biológicas.
– Durante la nitrificación, el amoníaco se convierte en nitrito, un paso fundamental para todo el ciclo del nitrógeno. Esta fase genera energía, al igual que otros procesos metabólicos.
– Cuando un organismo elimina desechos o muere, el nitrógeno de sus tejidos se encuentra en forma orgánica. Los hongos y los organismos procariotas se encargan de descomponer el tejido, liberando en el proceso nitrógeno inorgánico, a lo que se conoce como amonificación.
– Después de la amonificación, el amoníaco queda nuevamente disponible para las plantas y microorganismos que lo requieren para su crecimiento.
Etapas del ciclo del nitrógeno
1. Fijación
El nitrógeno gaseoso que se encuentra en la atmósfera reacciona con los rayos solares, formando óxidos de nitrógeno. Este compuesto se fija en bacterias y otros organismos procariotas que se encuentran en el suelo, agua y plantas, formando ion amonio (NH4+) y amoníaco (NH3). De esta manera, las plantas pueden utilizar el nitrógeno para sintetizar moléculas orgánicas que realizarán diversas funciones.
2. Amonificación
Los animales herbívoros ingieren plantas que han fijado el nitrógeno. Estos herbívoros son consumidos por animales carnívoros.
Los animales con exceso de nitrógeno se deshacen del mismo a través de la orina. Los animales terrestres producen urea ((NH2)2CO) y los animales acuáticos producen amoníaco (NH3).
3. Nitrificación
El amoníaco y urea que han expulsado los animales es utilizado por bacterias para obtener energía. A partir de la nitritación se obtiene nitrito (NO2–) a partir del amonio. A partir de la nitratación se obtiene nitrato (NO3–) a partir del nitrito.
4. Desnitrificación
Esta etapa consiste en la conversión del nitrato (NO3–) en nitrógeno gaseoso (N2).
El nitrito y el nitrato que han obtenido las bacterias es utilizado por otras bacterias heterótrofas, que realizan respiración anaerobia, liberando nitrógeno gaseoso a la atmósfera, y volviéndose de nuevo a la etapa 1 o fijación. De esta forma comienza de nuevo el ciclo.
Importancia del ciclo del nitrógeno en los seres vivos
Gracias al ciclo del nitrógeno las plantas pueden sintetizar la clorofila, proceso que se logra a partir del aprovechamiento de los compuestos nitrogenados.
El ciclo ayuda a convertir el gas inerte en un recurso accesible para los seres vivos que habitan en el planeta Tierra.
Durante la etapa o fase llamada amonificación, las bacterias pueden descomponer la materia animal y vegetal, apoyando así a limpiar de desechos el medio ambiente.
Cuando los nitratos y nitritos se liberan en el suelo, se enriquece la tierra, nutriéndose, y así se pueden cultivar diversos alimentos.
Los seres humanos dependen del ciclo del nitrógeno, al igual que el resto de los animales, pues requieren consumir proteínas que antes fueron procesadas por las plantas y por otros animales.
Los organismos vegetales pueden utilizar los desechos descompuestos por hongos y bacterias, lo que permite volver a aprovechar el nitrógeno que se liberó en la tierra.
El conjunto de todos estos procesos se repite de manera continua en el planeta, lo que mantiene estable el porcentaje de nitrógeno en la atmósfera terrestre. Este gas es uno de los principales elementos de nuestra atmósfera, con un 80 % aproximadamente.
Referencias
- Galloway JN. The global nitrogen cycle: past, present and future. Science in China Ser C Life Sciences 48: 669-677.
- Pajares S. La cascada del nitrógeno ocasionada por actividades humanas. Oikos 16: 14-17.
- Stein L y M Klotz. The nitrogen cycle. Current Biology 26: 83-101.