
¿Qué es la fibronectina?
La fibronectina es una proteína adhesiva (glucoproteína) que pertenece a la matriz extracelular y está en el plasma sanguíneo. Este tipo de proteínas, por lo general, se encargan de unir o enlazar la membrana celular a las fibras de colágeno que se encuentran en el exterior.
El nombre “fibronectina” proviene de un vocablo compuesto por dos palabras en latín, la primera es fibra, que significa fibra o filamento, y la segunda, necter, que significa conectar, enlazar, pegar o ligar.
La fibronectina fue visualizada por primera vez en 1948 como un contaminante del fibrinógeno preparado por el proceso de fraccionamiento con etanol frío de Cohn. Esta se identificó como una glucoproteína plasmática única que poseía las características de una globulina insoluble en frío.
Esta proteína posee un alto peso molecular y se ha relacionado con una gran variedad de funciones en el interior de los tejidos. Entre ellas, la adhesión entre célula y célula, la organización del citoesqueleto o la transformación oncogénica.
La fibronectina se distribuye por muchos lugares del cuerpo a través de su forma soluble en el plasma sanguíneo, el líquido cefalorraquídeo, el líquido sinovial, el líquido amniótico, el fluido seminal, la saliva y los exudados inflamatorios.
Investigadores han informado que las concentraciones plasmáticas de fibronectina se elevan cuando las mujeres embarazadas sufren de preeclampsia. Así pues, este incremento en la concentración de fibronectina ha sido incorporado por los especialistas para diagnosticar dicha condición.
Estructura de la fibronectina
Las fibronectinas son glucoproteínas grandes, las cuales poseen un peso molecular de aproximadamente 440 kDa. Están compuestas por cerca de 2.300 aminoácidos, que representan el 95% de la proteína, pues el otro 5% son carbohidratos.
Los distintos análisis que se han realizado sobre la secuencia genómica y transcriptómica (ARN mensajero) de la proteína han señalado que se compone de tres bloques de secuencias homólogas repetidas, con longitudes de 45, 60 y 90 aminoácidos cada una.
Los tres tipos de secuencias comprenden más del 90% de la estructura total de las fibronectinas. Las secuencias homólogas de tipo I y II son bucles unidos entre sí por puentes disulfuro. Estos bucles contienen 45 y 60 residuos de aminoácidos cada uno, respectivamente.
Las secuencias homólogas de tipo III corresponden a 90 aminoácidos ordenados de forma lineal y sin puentes disulfuro en su interior. Sin embargo, algunos de los aminoácidos internos de las secuencias homólogas de tipo III tienen grupos sulfhídricos libres (R-S-H).
Las tres secuencias homólogas se pliegan y se organizan en una matriz más o menos lineal para formar dos “brazos diméricos” de subunidades proteicas casi idénticas. Las diferencias entre las dos subunidades surgen de eventos de maduración postranscripcionales.
Las fibronectinas se pueden observar generalmente de dos formas. Una forma abierta, que se observa cuando se depositan sobre la superficie de la membrana y que se encuentran listas para enlazarse con algún otro componente del exterior celular. Esta forma solo se observa mediante microscopía electrónica.
La otra forma se puede apreciar en soluciones fisiológicas. Los extremos de cada brazo o prolongación se encuentran doblados hacia el centro de la proteína, uniéndose a través de los extremos carboxilo de los sitios de unión a colágeno. En esta forma, la proteína tiene un aspecto globular.
- Dominios y propiedades de multiadhesión. Las propiedades de multiadhesión de la fribonectina se originan debido a la presencia de diferentes dominios que poseen valores elevados de afinidad para sustratos y proteínas diferentes. Los “brazos diméricos” se pueden dividir en 7 dominios funcionales diferentes. Estos son clasificados según el sustrato o dominio al cual se une cada uno. Por ejemplo, el dominio 1 y el dominio 8, son dominios de unión a la proteína fibrina. El dominio 2 posee propiedades de unión al colágeno, el dominio 6 es una región de adhesión celular, es decir, que le permite anclarse en casi cualquier membrana o superficie externa de las células. Las funciones de los dominios 3 y 5 son desconocidas aún en la actualidad. En el dominio 9 se ubica el extremo carboxilo o extremo C-terminal de la proteína. Las regiones de adhesión celular del dominio 6 poseen el tripéptido constituido por la secuencia de aminoácidos Arginina-Glicina-Asparagina (Arg-Gly-Asp). Este tripéptido es compartido por varias proteínas como el colágeno y las integrinas. El mismo es la estructura mínima requerida para el reconocimiento de la membrana plasmática por las fibronectinas e integrinas. La fibronectina, cuando se encuentra en su forma globular, representa una forma soluble y libre en la sangre. Sin embargo, en las superficies celulares y en la matriz extracelular esta se encuentra en forma “abierta”, rígida e insoluble.
Funciones de la fibronectina
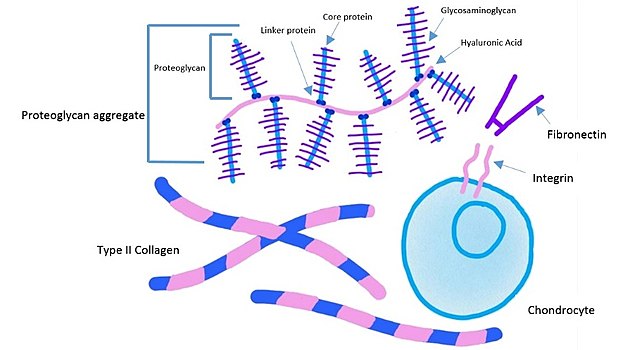
- Adhesión celular. Actúa como “puente” entre las células y los componentes de la MEC (colágeno, fibrina, proteoglicanos). Se une a integrinas en la membrana celular, favoreciendo la adhesión, el anclaje y la migración celular.
- Migración y diferenciación celular. Es fundamental en procesos de desarrollo embrionario, cicatrización y regeneración tisular. Guía el movimiento de células (ejemplo: fibroblastos, queratinocitos) hacia zonas donde deben proliferar o reparar.
- Cicatrización de heridas. Favorece la formación del coágulo inicial al unirse con fibrina y plaquetas. Estimula la llegada y organización de fibroblastos y células endoteliales para la formación de tejido de granulación y vasos nuevos (angiogénesis).
- Organización de la matriz extracelular. Participa en el ensamblaje de colágeno y otros componentes de la MEC, manteniendo la arquitectura tisular.
- Crecimiento y señalización celular. A través de su interacción con integrinas, activa vías de señalización que regulan proliferación, supervivencia y diferenciación celular.
- Defensa y reparación. Facilita la fagocitosis de restos celulares y microorganismos. Contribuye al cierre y remodelación de heridas después de la inflamación.
Referencias
- Conde-Agudelo, A., Romero, R., Roberts, J.M. Tests to predict preeclampsia. In Chesley’s hypertensive disorders in pregnancy. Academic Press.
- Farfán, J.Á.L., Tovar, H.B.S., de Anda, M.D.R.G., Guevara, C.G. Fibronectina fetal y longitud cervical como predictores tempranos de parto pretérmino. Ginecología y Obstetricia de México.
- Feist, E., Hiepe, F. Fibronectin autoantibodies. In Autoantibodies. Elsevier.
- Letourneau, P. Axonal pathfinding: Extracellular matrix role. Encyclopedia of neuroscience.
- Pankov, R., Yamada, K.M. Fibronectin at a glance. Journal of cell science.