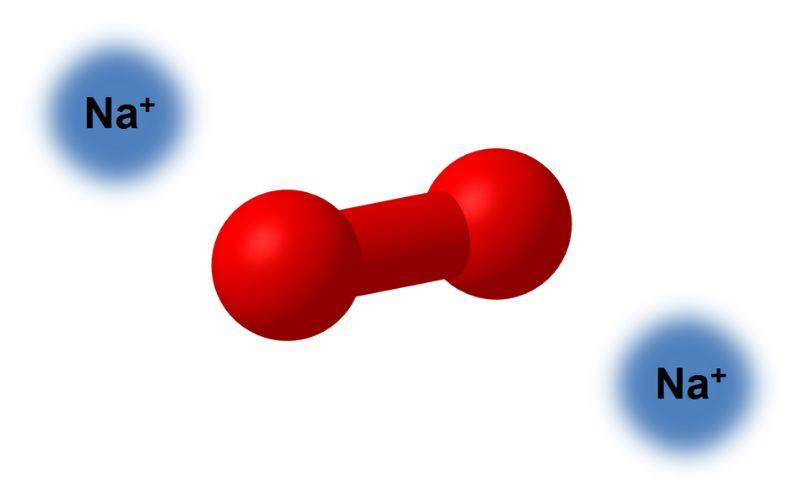
¿Qué es el peróxido de sodio?
El peróxido de sodio es un compuesto químico de fórmula Na2O2 que presenta dos enlaces iónicos entre los dos átomos de sodio y la molécula de O2. Existe en varios hidratos y peroxihidratos, incluyendo Na2O2 · 2H2O2 · 4H2O, Na2O2 · 2H2O, Na2O2 · 2H2O2 y Na2O2 · 8H2O.
Tiene una estructura cristalina hexagonal, pero al calentarse esta forma experimenta una transición a una fase de simetría desconocida a 512° C.
El peróxido de sodio puede prepararse a gran escala mediante la reacción de sodio metálico con oxígeno a 130-200° C, proceso que genera óxido de sodio, que en una etapa separada absorbe oxígeno:
4 Na + O2 → Na2O
2 Na2O + O2 → 2 Na2O2
El presente procedimiento discontinuo implica la oxidación de sodio en monóxido sódico con aire seco y posterior oxidación del monóxido en peróxido con un 90% de oxígeno.
En 1951, USI comenzó a operar el primer proceso continuo para la producción de peróxido de sodio. El proceso es único en un aspecto: utiliza aire en lugar de oxígeno puro.
Durante casi 70 años, se han utilizado variaciones de un proceso por lotes, por ejemplo, el producto comercial contiene entre 90 y 95% de peróxido de hidrógeno.
Propiedades físicas y químicas del peróxido de sodio
- El peróxido de sodio es un sólido granulado de color amarillento que se torna amarillo en contacto con la atmósfera.
- Su peso molecular es de 77,98 g/mol.
- Su densidad, de 2,805 g/ml.
- El punto de fusión es de 460,00° C donde comienza a descomponerse a óxido de sodio y oxígeno molecular según la reacción:
2 Na2O2 → 2 Na2O + O2
- Su punto de ebullición es 657° C.
- Reacciona violentamente con agentes reductores, materiales combustibles y metales ligeros. Reacciona exotérmica y rápidamente o incluso explosivamente con agua para formar una base fuerte (NaOH) y oxígeno (O2).
- Una mezcla con persulfato de amonio puede explotar si se somete a fricción (trituración en un mortero), si se calienta, o si una corriente de dióxido de carbono gaseoso pasa sobre él.
- Reacciona muy vigorosamente con sulfuro de hidrógeno gaseoso. Incluso en ausencia de aire, la reacción puede ir acompañada de llama. Se produce una explosión cuando se pasa dióxido de carbono gaseoso sobre una mezcla de peróxido de sodio con magnesio en polvo.
- Las mezclas con ácido acético o anhídrido acético pueden explotar si no se mantienen frías. Son espontáneamente inflamables en contacto con anilina, benceno, éter dietílico o materiales orgánicos, como papel y madera.
- Mezclas con carbón vegetal, glicerina, ciertos aceites y fósforo queman o explotan. Una mezcla con carburo de calcio (en polvo) puede estallar cuando se expone al aire húmedo y explota cuando se calienta.
- Se descompone, a menudo violentamente, en presencia de cantidades catalíticas de dióxido de manganeso. La mezcla con monocloruro de azufre conduce a una reacción violenta. Puede reaccionar y provocar la ignición de los combustibles.
Reactividad y peligros del peróxido de sodio
- Es un compuesto clasificado como base fuerte, explosivo y fuerte agente oxidante según su alerta de reactividad.
- Las mezclas con material combustible se inflaman fácilmente por fricción, calor o contacto con la humedad.
- Puede descomponerse vigorosamente bajo exposición prolongada al calor, causando el rompimiento de los recipientes que lo contienen.
- Muy peligroso en caso de contacto con la piel y con los ojos (irritante) y en los casos de ingestión y de inhalación. La exposición prolongada puede causar quemaduras en la piel y ulceraciones. La sobreexposición por inhalación puede causar irritación respiratoria.
- La inflamación del ojo se caracteriza por enrojecimiento, riego y picazón. La inflamación de la piel se caracteriza por picazón, descamación, enrojecimiento o, a veces, formación de ampollas.
- En caso de contacto con los ojos, se debe verificar si se está usando lentes de contacto y removerlas. Se debe enjuagar inmediatamente los ojos con agua corriente durante al menos 15 minutos, manteniendo los párpados abiertos.
- En caso de contacto con la piel, se lava suave y cuidadosamente la piel contaminada con agua corriente y jabón no abrasivo. Se puede utilizar agua fría. Se debe cubrir la piel irritada con un emoliente.
- Si el contacto con la piel es grave, se debe lavar con un jabón desinfectante y cubrir la piel contaminada con una crema antibacteriana.
- En caso de inhalación, se debe dejar reposar a la víctima en un área bien ventilada. Evacuar a la víctima a una zona segura tan pronto como sea posible. Aflojar la ropa apretada, como cuello de camisa, cinturón o corbata. Si la respiración es difícil, administrar oxígeno. Si la víctima no está respirando, realizar una resucitación boca a boca.
- En caso de ingestión, no se debe inducir el vómito.
- En todos los casos se debe buscar atención médica inmediata.
Usos del peróxido de sodio
- El peróxido de sodio se utiliza en blanqueadores de ropa, ya que reacciona con el agua para producir peróxido de hidrógeno, un agente blanqueador según la reacción:
Na2O2 + 2 H₂O → 2 NaOH + H2O2
- Además del peróxido de hidrógeno, la reacción produce hidróxido de sodio (lejía), que mantiene la solución alcalina. Agua caliente y una solución alcalina son ambos necesarios para que el peróxido de hidrógeno funcione mejor como un blanqueador.
- Se usa para blanquear pasta de madera para la producción de papel y textiles.
- Hoy en día, se utiliza principalmente para operaciones de laboratorio especializadas, por ejemplo, la extracción de minerales. Además, en las reacciones químicas se utiliza peróxido de sodio como agente oxidante.
- También se emplea como fuente de oxígeno haciéndola reaccionar con dióxido de carbono para producir oxígeno y carbonato sódico, por lo tanto, es particularmente útil en equipos de buceo, submarinos, etc.
Referencias
- Ashford, R. Ashford’s Dictionary of Industrial Chemicals. Londres: Publications Ltd.
- Field, S. Ingredients –Sodium peroxide. Recuperado de sci-toys.com.
- SODIUM PEROXIDE. Recuperado de cameochemicals.
- Sodium: sodium peroxide. Recuperado de webelements.
- Using sodium peroxide to scrub carbon dioxide emissions. Recuperado de stackexchange.