¿Qué es la superóxido dismutasa?
La superóxido dismutasa (SOD), o superóxido oxidorreductasa, es una familia de enzimas ubicuas en la naturaleza, cuya función principal es la defensa de los organismos aeróbicos frente a radicales libres de oxígeno, especialmente los radicales aniónicos superóxidos.
La reacción que estas enzimas catalizan ocurre virtualmente en todas las células que son capaces de respirar (aeróbicas) y es esencial para la supervivencia de estas, ya que elimina los tóxicos radicales libres del oxígeno, tanto en eucariotas como procariotas.
Muchas enfermedades en los animales se relacionan con la acumulación de diferentes especies reactivas de oxígeno, y lo mismo es cierto para las plantas, dado que el ambiente impone numerosos y constantes tipos de estrés oxidativo, superados gracias a la actividad de las superóxido dismutasas.
Este grupo de enzimas fue descubierto en 1969 por McCord y Fridovich, y desde entonces ha habido avances considerables respecto a estas enzimas y las reacciones que catalizan en los seres vivos.
Características de la superóxido dismutasa
– Función antioxidante. Su principal función es neutralizar los radicales libres, específicamente el radical superóxido (O2·-), una especie altamente reactiva y potencialmente dañina que se genera durante los procesos metabólicos normales, respondiendo a situaciones de estrés.
– Reacción enzimática. Cataliza la conversión del radical superóxido en peróxido de hidrógeno (H2O2) y oxígeno molecular (O2). Esta reacción es esencial para eliminar el superóxido, que de otro modo causaría daño a células y tejidos.
– Coordinación con otras enzimas antioxidantes. Trabaja con otras enzimas antioxidantes, como la catalasa y la glutatión peroxidasa, para neutralizar diferentes especies reactivas de oxígeno y proteger las células contra el estrés oxidativo.
– Ubicación celular. Se encuentra en diversas ubicaciones celulares, incluyendo el citosol, las mitocondrias y el espacio extracelular. Su presencia en diferentes compartimentos celulares destaca la importancia de su función para proteger del estrés oxidativo en diversas áreas de la célula.
– Regulación. Su actividad puede regularse en respuesta a las condiciones celulares y ambientales. Se ha observado que su expresión se incrementa al responder al estrés oxidativo para contrarrestar sus efectos negativos.
– Importancia en enfermedades. La disfunción en su actividad se ha asociado con diversas enfermedades, incluyendo enfermedades neurodegenerativas y trastornos relacionados con el estrés oxidativo.
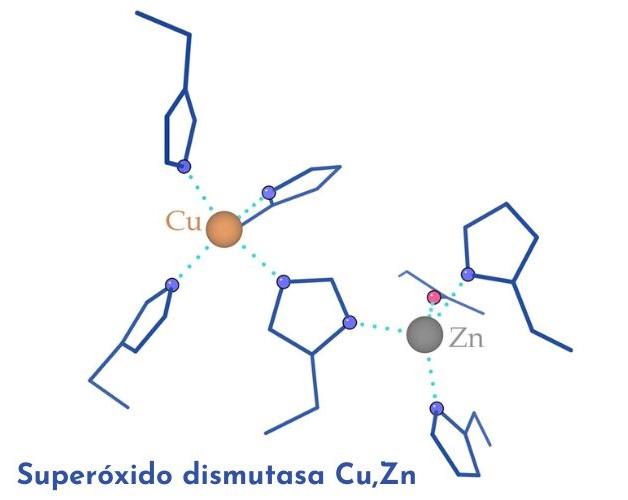
– Variantes. Hay varias formas de superóxido dismutasa, incluyendo la SOD1 (citoplasmática), la SOD2 (mitocondrial) y la SOD3 (extracelular). Cada forma tiene una localización específica en la célula y una función adaptada a su entorno. Dos de estas isoformas poseen átomos de cobre y de zinc en sus centros catalíticos y difieren entre sí en cuanto a su ubicación: intracelular (citosólico, SOD1 o Cu/Zn-SOD) o con elementos extracelulares (EC-SOD o SOD3). La isoforma SOD2 o Mn-SOD, a diferencia de las dos anteriores, tiene un átomo de manganeso como cofactor y su ubicación parece restringida a las mitocondrias de las células aeróbicas.
Estructura de la superóxido dismutasa
Las isoenzimas superóxido dismutasas en los humanos pueden diferir entre sí en cuanto a ciertos aspectos estructurales.
- Peso molecular. Por ejemplo, la isoenzima SOD1 tiene 32 kDa de peso molecular, mientras que la SOD2 y la SOD3 son homotetrámeros de 95 y 135 kDa de peso molecular, respectivamente.
- Estructura. El otro grupo de superóxido dismutasas, las Fe-SOD presentes en plantas y otros organismos distintos a los mamíferos, son enzimas diméricas de subunidades idénticas, es decir, son homodímeros.
- Secuencias. En algunas plantas, estas Fe-SOD contienen una secuencia señal N-terminal putativa para el transporte hacia el interior de los cloroplastos y otras contienen una secuencia C-terminal tripeptídica de transporte hacia los peroxisomas, por lo que se presume que su distribución subcelular se restringe a ambos compartimentos.
- Estructura molecular. La estructura molecular de los tres tipos de enzimas superóxido dismutasa está conformada, en esencia, por hélices alfa y láminas B-plegadas.
Funciones de la superóxido dismutasa
- Neutralización del radical superóxido. Su función principal es catalizar la conversión del radical superóxido (O2·-) en peróxido de hidrógeno (H2O2) y oxígeno molecular (O2). El superóxido es una especie altamente reactiva y tóxica que se produce durante procesos metabólicos normales y puede causar daño a las células.
- Protección contra el estrés oxidativo. El estrés oxidativo sucede cuando hay un desequilibrio entre la producción de especies reactivas de oxígeno (ROS) y la capacidad del sistema antioxidante para neutralizarlos. La SOD ayuda a mantener este equilibrio al eliminar el superóxido, previniendo el daño oxidativo de células y tejidos.
- Colaboración con otras enzimas antioxidantes. Trabaja en conjunto con otras enzimas antioxidantes, como la catalasa y la glutatión peroxidasa. Estas enzimas colaboran para neutralizar diferentes formas de ROS, aportando defensa antioxidante completa.
- Protección de las mitocondrias. La variante mitocondrial de la SOD (SOD2) está específicamente en las mitocondrias, orgánulos celulares fundamentales para la producción de energía. Esta variante desempeña un papel crucial en la protección de las mitocondrias contra el estrés oxidativo, ya que son una fuente importante de especies reactivas de oxígeno.
- Participación en la respuesta inflamatoria. Puede influir en la respuesta inflamatoria al modular la generación de ROS durante procesos inflamatorios. Esto puede ayudar a prevenir el daño tisular asociado con la inflamación crónica.
- Regulación del ciclo redox. Su actividad contribuye a mantener el equilibrio redox en células y tejidos. Este equilibrio es esencial para el funcionamiento adecuado de las células y la prevención de daños oxidativos.
Enfermedades relacionadas con la superóxido dismutasa
Una disminución de la actividad superóxido dismutasa puede darse por varios factores, tanto internos como externos. Algunos se relacionan con defectos genéticos directos en los genes codificantes para enzimas SOD, mientras que otros pueden ser indirectos, relativos a la expresión de moléculas reguladoras.
Gran número de condiciones patológicas de los seres humanos se relaciona con las enzimas SOD, entre ellos la obesidad, la diabetes, el cáncer y otras.
Con respecto al cáncer, se ha determinado que existe gran número de tipos de tumores cancerígenos que poseen bajos niveles de cualquiera de las tres superóxido dismutasas de mamíferos (SOD1, SOD2 y SOD3).
El estrés oxidativo que la actividad superóxido dismutasa previene, también se asocia con otras patologías articulares, como la osteoartritis, la artritis reumatoide. Muchas de estas enfermedades tienen que ver con la expresión de factores que inhiben la actividad SOD, como lo es el factor TNF-α.
Referencias
- Fridovich, I. Superoxide Dismutases. Annu. Rev. Biochem.
- Johnson, F., & Giulivi, C. Superoxide dismutases and their impact upon human health. Molecular Aspects of Medicine.
- Oberley, L. W., & Bueftner, G. R. Role of Superoxide Dismutase in Cancer: A Review. Cancer Research.
- Taylor, P., Bowler, C., Camp, W. Van, Montagu, M. Van, Inzé, D., & Asada, K. Superoxide Dismutase in Plants. Critical Reviews in Plant Sciences.
- Zelko, I., Mariani, T., & Folz, R. Superoxide dismutase Multigene Family: A comparison of the CuZn-SOD (SOD1), Mn-SOD (SOD2), and EC-SOD (SOD3) Gene Structures, Evolution, and Expression. Free Radical Biology & Medicine.