
¿Qué es la prueba de la catalasa?
La prueba de la catalasa es una metodología usada en los laboratorios de bacteriología para poner en evidencia la presencia de la enzima catalasa en aquellas bacterias que la poseen. Junto a la coloración de Gram, son las principales pruebas que se le deben realizar a los microorganismos recién aislados.
Estas pruebas orientan al microbiólogo sobre los pasos a seguir para la identificación definitiva del microorganismo en cuestión.
Por lo general, las bacterias que contienen citocromo poseen la enzima catalasa, es decir, que las bacterias aerobias y anaerobias facultativas deberían poseerla. Sin embargo, existen excepciones, como por ejemplo, los Streptococcus, que a pesar de ser microorganismos anaerobios facultativos, no poseen la enzima catalasa.
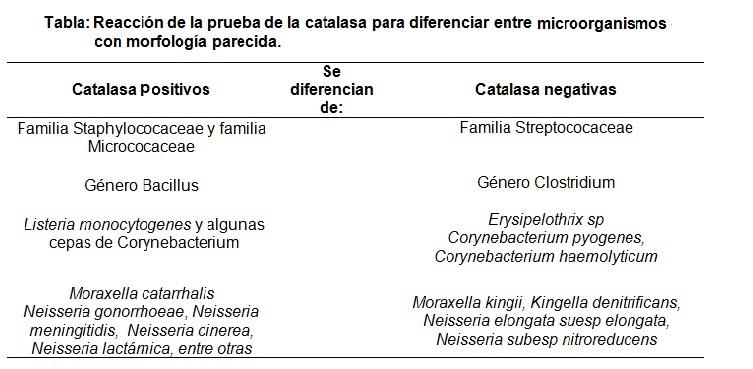
Es por ello que la prueba de la catalasa se emplea principalmente para distinguir a las familias Staphylococaceae y Micrococaceae (ambas catalasa positivas) de la familia Streptococaceae (catalasa negativa).
Así mismo, el género Bacillus (catalasa positiva) se distingue del género Clostridium (catalasa negativo), entre otros.
Fundamento de la prueba de la catalasa
La catalasa es una enzima clasificada como una hidroperoxidasa, esto quiere decir que utilizan como sustrato el peróxido de hidrógeno (H2O2).
También se le considera una oxidorreductasa, ya que en la reacción donde participa hay un elemento que sirve como donante de electrones (sustancia reductora) y otro como receptor de electrones (sustancia oxidante).
La catalasa es una proteína que contiene un grupo prostérico con cuatro átomos de hierro trivalentes (Fe+++), por tanto, es una homoproteína. El ion férrico se mantiene oxidado durante la reacción.
Se puede decir que la catalasa es una enzima desintoxicante, pues su función es eliminar sustancias que se producen durante el metabolismo bacteriano que son tóxicas para las bacterias. Entre estas sustancias se encuentra el peróxido de hidrógeno.
El peróxido de hidrógeno se forma de la descomposición de los azúcares por la vía aeróbica. Este proceso ocurre de la siguiente manera:
El ion superóxido (O2–) (radical libre) se forma como producto final de la asimilación de la glucosa por la vía aerobia. Este es tóxico y se elimina por la enzima superóxido dismutasa, que lo transforma en oxígeno gaseoso y peróxido de hidrógeno.
El peróxido de hidrógeno también es tóxico para las bacterias y debe ser eliminado. La enzima catalasa desdobla el peróxido de hidrógeno en agua y oxígeno.
La catalasa puede actuar sobre otros sustratos diferentes al peróxido de hidrógeno, como alcoholes, aldehídos, ácidos, aminas aromáticas y fenoles. Sin embargo, la catalasa puede utilizar también el peróxido de hidrógeno para oxidar otros compuestos tóxicos, como el alcohol metílico y etílico.
Asimismo, la catalasa está presente en las células fagocíticas, protegiéndolas de la acción tóxica del peróxido de hidrógeno.
Técnica de rutina para la prueba de la catalasa
Método en portaobjeto
Materiales
Peróxido de hidrógeno al 3% (10 volúmenes).
Lámina portaobjeto
Asa plástica desechable o palillo de madera.
Procedimiento
- Tomar suficiente cantidad de la colonia a estudiar sin tocar el agar de donde proviene. La colonia debe ser fresca, es decir, de un cultivo de 18 a 24 horas.
- Colocar la colonia sobre el portaobjeto seco y sobre ella agregar una gota de peróxido de hidrógeno al 3% (también se puede usar H2O2 al 30%). Observar inmediatamente si se desprenden burbujas o no.
Interpretación
Reacción positiva: desprendimiento de gas, que se evidencia con la formación de burbujas (burbujeo fuerte).
Reacción negativa: no hay formación de burbujas.
Método directo en cultivo puro
- Colocar 1 ml de H2O2 al 3% sobre un cultivo puro en placas o en cuñas que no contengan sangre (preferiblemente agar nutritivo). Observar si existe o no formación de burbujas de forma inmediata. También se puede usar H2O2 al 30%.
Se interpreta igual que el método en portaobjeto.
Método con tubo capilar o de Fung y Petrishko
- Llenar un tubo capilar de 67 mm a una altura de 20 mm con peróxido de hidrógeno al 3% por capilaridad.
- Tocar la colonia aislada que se desea estudiar con el capilar lleno de H2O2 al 3%. Observar si el capilar se llena de burbujas en 10 segundos aproximadamente. Este método permite semi-cuantificar la reacción en cruces:
Sin cruces no hay burbujas (reacción negativa).
+ ———- Escasas burbujas (reacción débil o retardada).
++ ——– Abundantes burbujas (reacción moderada).
+++ —— Las burbujas alcanzan el extremo contrario (reacción enérgica).
Método de Taylor y Achanzar para pruebas de catalasa que dan dudosas
- En un portaobjeto limpio y seco colocar una colonia aislada, luego colocar una gota de H2O2 al 0,5% y cubrir con un cubreobjetos. Observar si hay o no formación de burbujas aprisionadas.
Interpretación: la presencia de burbujas indica una reacción positiva. Sin burbujas, se interpreta como una reacción negativa.
Prueba de la catalasa para especies de Mycobacterium
Esta técnica necesita realizarse controlando el pH y la temperatura. Se debe ejecutar bajo una campana de flujo laminar, ya que la manipulación de las distintas especies de Mycobacterium es peligrosa.
Materiales
Peróxido de hidrógeno al 30% o 110 volúmenes (superoxal).
Buffer fosfato pH 7
Tween 80 al 10%
Cultivo de Mycobacterium en cuña de 3 a 4 semanas
Preparación de reactivos
Buffer fosfato pH 7
Pesar:
- 1,361 g de (KH2PO4) fosfato monopotásico anhidro.
- 1,420 g de (Na2HPO3) fosfato disódico anhidro.
- Disolver ambas sales en un poco de agua destilada estéril y completar con agua hasta 1.000 ml.
Tween 80 al 10%
Realizar una dilución 1:10 al Tween 80 que viene comercialmente concentrado, para ello proceder de la siguiente manera:
- Tomar 1 ml de Tween 80 y colocarlo en un poquito de agua destilada, disolver y luego completar el volumen con agua hasta 10 ml.
Reactivo final
- Mezclar una cantidad de buffer fosfato con una cantidad de Tween 80 al 10% (a partes iguales). Definir en el laboratorio cuánto se desea preparar.
Procedimiento
- Colocar 5 ml de buffer fosfato en un tubo de ensayo estéril con tapa de rosca (baquelita).
- Con un asa de inoculación, tomar suficiente colonia de un crecimiento de Mycobacterium sembrado en cuñas y disolver en el buffer fosfato.
- Tapar el tubo sin apretar demasiado la rosca.
- Colocar en baño maría a 68 °C por 20 a 30 minutos. Sacar y dejar enfriar a 22-25 °C.
- Medir 0,5 ml del reactivo final (mezcla) y adicionarlo al tubo con la solución fría. Observar la formación o no de burbujas.
Se interpreta igual que las técnicas anteriores.
Uso de la prueba de la catalasa
Cuando se obtiene un crecimiento de colonias en medios enriquecidos, se le debe realizar una tinción de Gram y una prueba de catalasa a las colonias obtenidas. Esto orientará al microbiólogo sobre los procedimientos a seguir para la identificación definitiva.
Control de calidad
Para evaluar el buen funcionamiento del reactivo de peróxido de hidrógeno, usar cepas controles recién cultivadas, tales como Staphylococcus aureus como control positivo y cepas de Streptococcus sp como control negativo.
Otra alternativa que sirve como control positivo es colocar una gota de peróxido de hidrógeno sobre el agar sangre, los eritrocitos tienen catalasa, por tanto, habrá un burbujeo si el reactivo está en buenas condiciones.
Se puede utilizar un agar chocolate como control negativo, aquí los eritrocitos ya están lisados y la prueba da negativa.
Limitaciones de la prueba de la catalasa
- No usar cultivos viejos para la prueba, ya que esto puede originar falsos negativos.
- Evitar tomar colonias a partir de cultivos en agar sangre, si se hace tener cuidado de no tocar el agar. Este procedimiento puede provocar falsos positivos, porque los eritrocitos contienen catalasa.
- Si se toma la colonia con asa de platino no invertir el orden del procedimiento porque esto puede generar falsos positivos. Esto se debe a que el platino es capaz de reaccionar con el peróxido de hidrógeno, originando un burbujeo.
- No utilizar el reactivo de peróxido de hidrógeno si está muy viejo, ya que el reactivo es muy inestable y tiende a descomponerse con el tiempo.
- Conservar el reactivo de peróxido de hidrógeno protegido de la luz y en refrigeración para evitar que se dañe.
- Realizar un control de calidad al reactivo de peróxido de hidrógeno cada vez que se use.
- Tomar en cuenta que si se usa el H2O2 al 30% las reacciones son más fuertes que las que se producen con H2O2 al 3%.
Referencias
- Koneman, E., Allen, S., Janda, W., Schreckenberger, P., Winn, W. Diagnóstico Microbiológico. 5ta. ed. Editorial Panamericana S.A. Argentina.
- Forbes, B., Sahm, D., Weissfeld, A. Diagnóstico Microbiológico de Bailey & Scott. 12 ed. Editorial Panamericana S.A. Argentina.
- Reactivo de catalasa-Gotario. Recuperado de winklerltda.cl.
- Agua oxigenada. Equivalencia entre volúmenes y porcentaje. Recuperado de vadequimica.com.