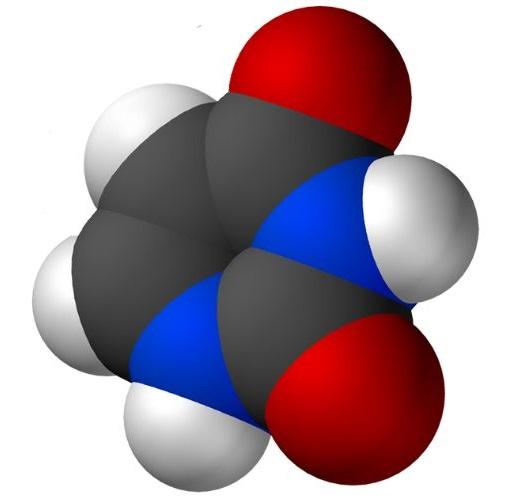
¿Qué es el uracilo?
El uracilo es una base nitrogenada tipo pirimidina, que se encuentra en el ácido ribonucleico (ARN). Es una de las características que diferencian al ARN del ácido desoxriribonucleico (ADN), ya que este último posee timina en lugar de uracilo. Ambas sustancias, uracilo y timina, solo difieren en que la segunda posee un grupo metilo.
Desde el punto de vista evolutivo, se ha propuesto que el ARN fue la primera molécula que almacenó información genética y funcionó como catalizador en las células, antes que el ADN y las enzimas. Debido a ello, se piensa que el uracilo tuvo un papel clave en la evolución de la vida.
En los seres vivos, el uracilo no se encuentra de forma libre, comúnmente forma nucleótidos monofosfato (UMP), difosfato (UDP) y trifosfato (UTP). Estos nucleótidos de uracilo tienen distintas funciones, como la biosíntesis de ARN y de glicógeno, la interconversión isomérica de azúcares y la regulación de la glutamina sintasa.
Estructura y propiedades del uracilo
- Fórmula. El uracilo, denominado 2,4-dioxipiridina, posee la fórmula empírica C4H4N2O2.
- Peso molecular. 112,09 g/mol.
- Aspecto. Es purificado como un polvo blanco.
- Estructura. La estructura de la uridina es un anillo heterocíclico con cuatro átomos de carbono y dos de nitrógeno, con dobles enlaces alternados. Es planar.
- Solubilidad. 50mg/ml, a 25 ºC, en hidróxido de sodio 1M.
- pKa. Entre 7.9 y 8.2.
- Absorbancia. La longitud de onda donde ocurre su absorbancia máxima (ʎmax) se encuentra entre 258 y 260 nm.
Biosíntesis del uracilo
Existe una vía común para la biosíntesis de nucleótidos de pirimidinas (uracilo y citosina).
- Primer paso. Biosíntesis de carbamoil fosfato a partir de CO2 y NH4+, el cual es catalizado por la carbamoil fosfato sintetasa.
- Segundo. La pirimidina se construye a partir de carboil fosfato y aspartato. Ambas sustancias reaccionan y forman N-carbamoilaspartato, reacción catalizada por la aspartato transcabamoilasa (ATCasa).
- Tercero. El cierre del anillo de pirimidina se produce por una deshidratación catalizada por la dihidrootasa, y produce L-dihidrorotato.
- Cuarto. El L-dihidrorotato es oxidado y convertido en orotato; el aceptor de electrones es el NAD+. Es una reacción catalizada por la dihidroorotato deshidrogenasa.
- Quinto. Transferencia del grupo fosforribosil, desde el fosforribosil pirofosfato (PRPP), al orotato. Forma orotidilato (OMP) y pirofosfato inorgánico (PPi), catalizado por la orotato fosforribosil transferasa.
- Sexto. Descarboxilación del anillo de pirimidina del orotidilato (OMP). Forma uridilato (uridin-5′-monofosfato, UMP), que es catalizado por una descarboxilasa. Luego, mediante la participación de una quinasa, un grupo fosfato es transferido desde el ATP al UMP, formándose UDP (uridin-5′-difosfato). Esto último se repite, formándose UTP (uridin-5′-trifosfato).
- Regulación de la biosíntesis. En bacterias, la regulación de la biosíntesis de pirimidinas ocurre mediante retroalimentación negativa, a nivel de la aspartato transcabamoilasa (ATCasa). Esta enzima es inhibida por CTP (citidin-5′-trifosfato), producto final de la vía de biosíntesis de las pirimidinas. La ATCasa posee subunidades reguladoras que se unen al regulador alostérico CTP. En animales, la regulación de la biosíntesis de pirimidinas sucede mediante retroalimentación negativa, a nivel de dos enzimas: 1) la carbamoil fosfato sintasa II, la cual es inhibida por UTP y activada por ATP y PRPP; y 2) la OMP descarboxilasa, que es inhibida por el producto de la reacción que ella misma cataliza, el UMP. La velocidad de biosíntesis del OMP varía con la disponibilidad de PRPP.
Funciones del uracilo
- En la biosíntesis del ARN. El uracilo está presente en todos los tipos de ARN, como el ARN mensajero (ARNm), el ARN de transferencia (ARNt) y el ARN ribosómico (ARNr). La biosíntesis de estas moléculas sucede mediante un proceso denominado transcripción. Durante la transcripción, la información contenida en el ADN es copiada en el ARN mediante una ARN polimerasa. El proceso inverso, en el cual la información contenida en el ARN es copiada en el ADN, sucede en algunos virus y plantas mediante la transcriptasa inversa. La biosíntesis de ARN necesita de nucleósidos trifosfato (NTP), a saber: uridina trifosfato (UTP), citidina trifosfato (CTP), adenina trifosfato (ATP) y guanina trifosfato (GTP). La reacción es:
(ARN)n residuos + NTP -> (ARN)n+1 residuo + PPi
La hidrólisis del pirofosfato inorgánico (PPi) proporciona la energía para la biosíntesis del ARN.
- En la biosíntesis de azúcares. Los ésteres de azúcares son muy comunes en los organismos vivos. Unos de estos ésteres son los difosfatos de ésteres de nucleosidos, como los UDP-azúcares, muy abundantes en las células. Los UDP-azúcares participan en la biosíntesis de disacáridos, oligosacáridos y polisacáridos.
- La biosíntesis de sacarosa en las plantas sucede mediante dos vías: una principal y una secundaria. La vía principal consiste en la transferencia de la D-glucosa desde el UDP-D-glucosa a la D-fructosa para formar sacarosa y UDP. La vía secundaria incluye dos pasos: comienza con UDP-D-glucosa y fructosa-6-fosfato y culmina con la formación de sacarosa y fosfato.
- La biosíntesis de lactosa en las glándulas mamarias sucede a partir de UDP-D-galactosa y glucosa.
- La biosíntesis de celulosa en las plantas se lleva a cabo mediante la condensación continua de residuos de beta-D-glucosilo, desde UDP-glucosa al extremo no reductor de la cadena creciente de poliglucosa.
- La biosíntesis de amilosa y amilopectina requiere de UDP-glucosa como sustrato donador de glucosa a la cadena creciente.
- La biosíntesis de glucógeno en los animales se hace mediante el UDP-glucosa y el ADP-glucosa.
- La biosíntesis de sulfato de condroitina requiere UDP-xilosa, UDP-galactosa y UDP-glucuronato.
- En la interconversión isómérica de azúcares. La conversión de galactosa a un intermediario de la glicólisis sucede a través de la vía Leloir. Uno de los pasos de esta vía es catalizado por la enzima UDP-galactosa-4-epimerasa, la cual facilita la interconversión de UDP-galactosa a UDP-glucosa.
- En la biosíntesis de glicoproteínas. Durante la biosíntesis de glicoproteínas, las proteínas atraviesan los sacos cis, medio y trans del aparato de Golgi. Cada uno de estos sacos posee un conjunto de enzimas que procesan las glicoproteínas. Los monómeros de azúcares, como la glucosa y la galactosa, son adicionados al oligosacárido de la proteína desde UDP-hexosa y otros nucleótidos-hexosa. Los nucleótidos-hexosa son transportados hacia las cisternas del Golgi mediante antiporte. La UDP-galactosa (UDP-Gal) y la UDP-N-acetilgalactosamina(UDP-GalNAc) entran a las cisternas desde el citosol mediante intercambio por UMP. En la cisterna del Golgi, una fosfatasa hidroliza un grupo fosfato del UDP y forma UMP y Pi. El UDP proviene de las reacciones catalizadas por la galactosiltransferasa y la N-acetilgalactosamiltransferasa. El UMP formado por la fosfatasa sirve para el intercambio de nucleótidos-hexosa.
- En la regulación de la glutamina sintasa. Un mecanismo de regulación de la glutamina sintasa es la modificación covalente, la cual consiste en la adenilación, que la inactiva, y la desadenilación, que la activa. Esta modificación covalente es reversible y catalizada por la adeniltransferasa. La actividad de la adeniltransferasa es modulada por la unión de la proteína PII, regulada por una modificación covalente, la uridililación. Tanto la uridililación como la desuridililación son llevadas a cabo por la uridiltransferasa. En esta enzima, la actividad de uridililación se debe a la glutamina y el fosfato, y es activada por la unión del alfa-cetoglutarato y ATP a la PII.
- En la edición del ARN. Algunos ARNm son editados antes de la traducción. En algunos organismos eucariotas, como Trypanosoma brucei, hay edición del ARN del transcripto del gen de la subunidad II de la citocromo oxidasa. Ello sucede mediante la inserción de residuos de uracilo, reacción catalizada por la uridiltransferasa terminal. Un ARN guía, complementario del producto editado, actúa como templado para el proceso de edición. Los pares de bases formados entre el transcripto inicial y el ARN guía implica pares de bases G = U que no son Watson-Crick y son comunes en el ARN.
Biosíntesis de UDP-glucosa
En condiciones fisiológicas, la biosíntesis de glicógeno a partir de glucosa-1-fosfato es termodinámicamente imposible (ΔG positivo). Por ello, previo a la biosíntesis, sucede la activación de la glucosa-1-fosfato (G1P). Esta reacción combina G1P y UTP para formar uridin difosfato glucosa (UDP-glucosa o UDPG).
La reacción es catalizada por la pirofosforilasa del UDP-glucosa, y es la siguiente:
G1P + UTP -> UDP-glucosa + 2Pi.
La variación de energía libre de Gibbs en este paso es grande y negativa (-33,5 KJ/mol). Durante la reacción al oxígeno, el G1P ataca al átomo de fósforo alfa del UTP y forma UDP-glucosa y pirofosfato inorgánico (PPi). Seguidamente, el PPi es hidrolizado por una pirofosfatasa inorgánica, cuya energía de hidrólisis impulsa la reacción general.
La UDP-glucosa es una sustancia de “alta energía”. Permite formar los enlaces glicosídicos entre el residuo de glucosa y la cadena de polisacáridos creciente. Este mismo principio energético es aplicable a las reacciones donde participan los UDP-azúcares, como la biosíntesis de disacáridos, oligosacáridos y glicoproteínas.
Uracilo ADN glicosilasa
Hay lesiones del ADN que se dan espontáneamente. Una de esas lesiones es la desaminación espóntanea de la citosina, y su consecuente conversión en uracilo. En este caso, la reparación tiene lugar por eliminación de la base modificada del ADN mediante una enzima denominada uracilo ADN glicosilasa.
La enzima uracilo ADN glicosilasa elimina la citosina dañada (uracilo), produciendo un residuo de desoxirribosa que carece de la base nitrogenada, denominado sitio AP (sitio apurínico-apirimidínico).
Después, la enzima endonucleasa AP hace un corte en el esqueleto fosfodiéster del sitio AP, eliminando el residuo azúcar-fosfato. La ADN polimerasa I restaura la hebra dañada.
Referencias
- Bohinski, R. Bioquímica. Addison-Wesley Iberoamericana.
- Devlin, T.M. Bioquímica. Editorial Reverté.
- Nelson, D. L., Cox, M. M. Lehninger–Principles of biochemistry. W.H. Freeman.
- Voet, D. and Voet, J. Biochemistry. John Wiley and Sons.