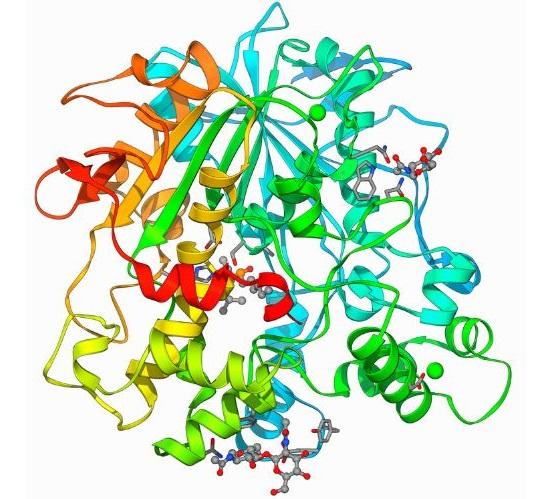
¿Qué son las lipasas?
Las lipasas son una gran familia de enzimas capaces de disgregar grasas, como los triglicéridos, los fosfolípidos, los ésteres de colesterol y algunas vitaminas, para hacerlos más fácilmente absorbibles.
Están presentes prácticamente en todos los reinos de la vida, tanto en microorganismos como bacterias y levaduras, en plantas y animales. En cada uno de estos organismos estas enzimas tienen propiedades y características especiales que las diferencian unas de otras.
Dependiendo del tipo de clasificación, se puede hacer la distinción entre las “verdaderas” lipasas, también conocidas como triacilglicerol lipasas, y otras enzimas con actividad lipolítica similar, como las fosfolipasas, las esterol esterasas y las retinil-palmitato esterasas.
El primer reporte publicado de la secuencia de una enzima lipasa fue el de De Caro y sus colaboradores en 1981, quienes estudiaron la triacilglicerol lipasa pancreática de porcinos. Estudios posteriores demostraron la existencia de muchas otras lipasas sistémicas en los organismos vivos.
Las lipasas más importantes en los animales son las lipasas digestivas producidas por el páncreas y el hígado, que participan en el metabolismo de las grasas consumidas en la dieta regularmente, y que por ello tienen importantes implicaciones fisiológicas desde diversos puntos de vista.
En la actualidad, estas enzimas no solo se estudian con propósitos clínicos y/o metabólicos, sino que también se producen industrialmente con fines comerciales para el procesamiento de alimentos y otros productos, y se pueden obtener a partir del cultivo de microorganismos especiales.
Características de las lipasas
– Solubilidad. Las lipasas son proteínas solubles en agua y catalizan reacciones hidrolíticas en sustratos insolubles.
– Ubicación. Se encuentran en la naturaleza en un equilibrio entre su forma activa y su forma inactiva, y la activación o inactivación depende de distintos factores celulares internos.
– Clasificación. Pertenecen a la superfamilia de enzimas hidrolasas con pliegues α/β, donde también se clasifican las esterasas, las tioesterasas, algunas proteasas y peroxidasas, deshalogenasas y otras hidrolasas intracelulares.
– Codificación. Las lipasas son codificadas por genes que pertenecen a una familia que incluye los genes codificantes de la lipasa pancreática, la lipasa hepática, la lipasa lipoproteica, la lipasa endotelial y la fosfatidilserina fosfolipasa A1.
– Mecanismo catalítico. Algunos autores proponen que la forma de catálisis de estas enzimas es análoga a la de las serín proteasas, lo que se relaciona con la presencia de tres residuos aminoacídicos especiales en el sitio activo. El mecanismo de hidrólisis implica la formación de un complejo enzima-sustrato (lipasa:triglicérido), subsecuentemente la formación de un intermediario hemiacetal y luego la liberación de un diacilglicérido y un ácido graso. El último paso de la hidrólisis, la liberación del ácido graso del sitio activo, ocurre por un modelo conocido como modelo de “catapulta”, que implica que luego del clivaje o la ruptura del enlace éster, el ácido graso es eyectado rápidamente del sitio catalítico.
– Especificidad de sustrato. Las lipasas pueden ser específicas y diferenciar entre sustratos como los triglicéridos, diacilglicéridos, monoglicéridos y fosfolípidos. Algunas son específicas en cuanto a los ácidos grasos, es decir, respecto a su longitud, su grado de saturación, etc. También pueden ser selectivas en cuanto a la región donde catalizan la hidrólisis, esto quiere decir que pueden tener especificidad posicional respecto al sitio al que se unen las moléculas de ácido graso al esqueleto de glicerol (en cualquiera de los tres carbonos).
Estructura de las lipasas
- Topología. Las lipasas se caracterizan por una topología compuesta por hélices α y láminas β-plegadas. El sitio catalítico de estas enzimas generalmente está compuesto por una tríada de aminoácidos: serina, ácido aspártico o glutámico e histidina.
- Peso molecular. La mayor parte de las lipasas son glicoproteínas que, dependiendo del tamaño de la porción carbohidratada, tienen entre 50 y 70 kDa.
- Lipasa pancreática de humanos. Tiene 449 residuos aminoacídicos y dos dominios separados: uno N-terminal, donde se encuentra el sitio catalítico y el pliegue característico de las hidrolasas (α/β), y otro C-terminal, de menor tamaño y considerado “auxiliar”, con una estructura denominada “sándwich β”.
- Peso molecular en humanos. Su peso molecular está entre los 45 y 53 kDa.
- Actividad catalítica. Es mayor a temperaturas cercanas a los 37 °C y a pH entre 6 y 10.
Funciones de las lipasas
- Digestión de grasas. Descomponen las grasas en ácidos grasos y glicerol, lo que facilita su absorción en el intestino delgado. Estas enzimas son secretadas principalmente por el páncreas en forma de lipasa pancreática y ayudan a descomponer los triglicéridos (forma principal en que las grasas se almacenan en los alimentos).
- Absorción de nutrientes. Los lípidos descompuestos en formas más fácilmente absorbibles por las células intestinales, luego son transportados a través del sistema circulatorio para su utilización en diversas funciones metabólicas.
- Metabolismo energético. Los productos finales de la digestión lipídica, como los ácidos grasos, son necesarios para la producción de energía mediante procesos metabólicos como la beta-oxidación, una de las vías metabólicas en la que los ácidos grasos se descomponen en unidades más pequeñas para producir energía.
- Regulación del metabolismo. También tienen un papel en la regulación del metabolismo y el almacenamiento de grasas en el cuerpo. La actividad de estas enzimas puede estar sujeta a la regulación hormonal y otros factores para asegurar un equilibrio adecuado en el almacenamiento y la utilización de grasas.
- Funciones industriales. En la industria de producción de alimentos lácteos, el uso de las lipasas es común para hidrolizar las grasas presentes en la leche, lo que tiene efectos directos en la “potenciación” del sabor en quesos, cremas y otros productos lácteos. También son utilizadas en la manufactura de otros productos alimenticios, especialmente durante la fermentación, para mejorar el sabor y la “digestibilidad” de algunas comidas de preparación industrial. Lejos de la industria alimenticia, el uso de las lipasas de origen microbiano es popular en la formulación de detergentes y sustancias de limpieza general, que disminuyen los efectos deletéreos sobre el ambiente que conlleva la enorme carga química presente en los productos de limpieza convencionales.
Referencias
- Lowe, M. E. The triglyceride lipases of the pancreas. Journal of Lipid Research.
- Mead, J. R., Irvine, S. A., & Ramji, D. P. Lipoprotein lipase: structure, function, regulation, and role in disease. J. Mol. Med.
- Perret, B., Mabile, L., Martinez, L., Tercé, F., Barbaras, R., & Collet, X. Hepatic lipase: structure / function relationship, synthesis, and regulation. Journal of Lipid Research.
- Santamarina Fojo, S., González Navarro, H., Freeman, L., Wagner, E., Nong, Z. Hepatic Lipase, Lipoprotein Metabolism, and Atherogenesis. Arteriosclerosis, Thrombosis, and Vascular Biology.
- Taylor, P., Kurtovic, I., Marshall, S. N., Zhao, X., Simpson, B. K., Kurtovic, I., Zhao, X. I. N. Lipases from Mammals and Fishes. Reviews in Fisheries Science.