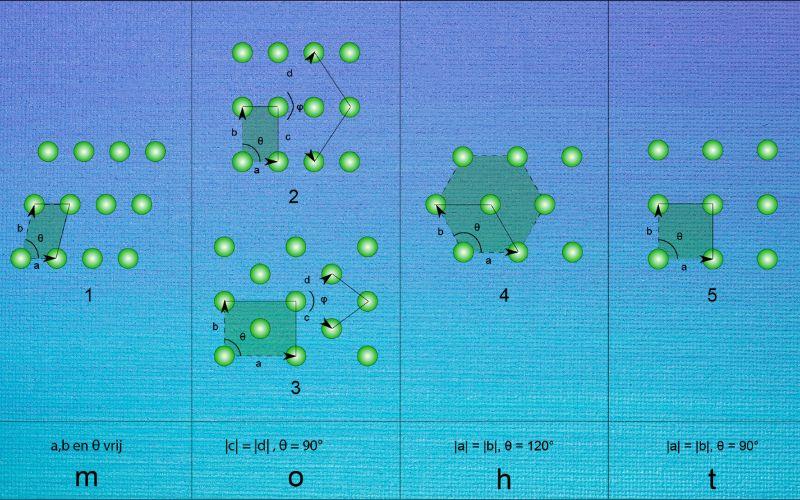
¿Qué son las redes de Bravais?
Las redes de Bravais son el conjunto de catorce celdas unitarias tridimensionales en las que pueden ubicarse los átomos de un cristal. Estas celdas constan de un arreglo tridimensional de puntos que forman una estructura básica que se repite periódicamente en las tres direcciones espaciales.
El origen de esta denominación para las estructuras cristalinas básicas proviene de 1850, cuando Auguste Bravais demostró que solo hay 14 celdas unitarias básicas tridimensionales posibles.
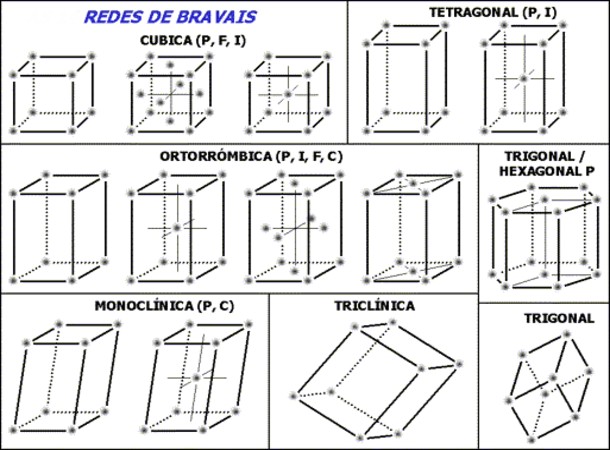
El conjunto de las 14 redes de Bravais se subdivide en siete grupos o estructuras de acuerdo a la geometría de las celdas; estos siete grupos son:
1. Cúbico.
2. Tetragonal.
3. Ortorrómbico.
4. Trigonal-Hexagonal.
5. Monoclínico.
6. Triclínico.
7. Trigonal.
Cada una de estas estructuras define una celda unitaria, siendo esta la porción más pequeña que conserva la disposición geométrica de los átomos en el cristal.
Características de las redes de Bravais
– Periodicidad. El patrón de puntos se repite de forma regular e infinita en el espacio.
– Equivalencia de los puntos. Todos los puntos de la red son idénticos; cada uno tiene el mismo entorno.
– Dimensionalidad. Existen en tres dimensiones (redes cristalinas tridimensionales).
– Celdas unitarias. La red puede describirse mediante una celda unitaria, que al repetirse genera toda la estructura.
– Parámetros de red. Se definen por las longitudes de los ejes (a, b, c) y los ángulos entre ellos (\alpha, \beta, \gamma).
– Simetría. Presentan simetrías de traslación, rotación, reflexión e inversión.
– Tipos finitos. Solo existen 14 redes de Bravais posibles en tres dimensiones.
– Sistemas cristalinos. Las 14 redes se agrupan en 7 sistemas cristalinos (cúbico, tetragonal, ortorrómbico, hexagonal, trigonal, monoclínico y triclínico).
– Independencia del motivo. La red describe solo la disposición geométrica; al añadir un motivo o base (átomos, iones), se forma el cristal real.
Algunas redes de Bravais
- Red cúbica P. Es conveniente resaltar que los átomos se representan por esferas cuyos centros están en los vértices de la celda unitaria cúbica P. En el caso de la red cúbica P, el número de átomos por celda es 1, debido a que en cada vértice solo la octava parte del átomo está dentro de la celda unitaria, entonces 8*⅛ = 1. El número de coordinación indica el número de átomos que son vecinos próximos en la red cristalina. En el caso de la red cúbica P, el número de coordinación es 6.
- Red cúbica I. En este tipo de red, además de los átomos en los vértices del cubo, se tiene un átomo en el centro del cubo. Por lo que el número de átomos por celda unitaria en la red cúbica P es de 2.
- Red cúbica F. Es la red cúbica que, además de los átomos en los vértices, tiene un átomo en el centro de la cara de cada cubo. El número de átomos por celda es 4, ya que cada uno de 6 átomos de la cara tiene la mitad dentro de la celda, es decir, 6*½ = 3 más 8*⅛=1 en los vértices.
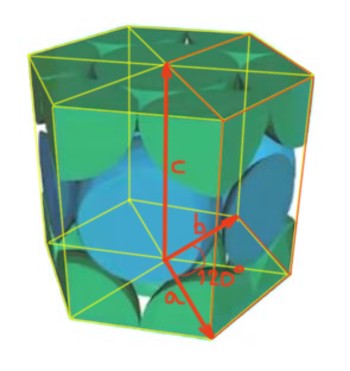
- Red hexagonal. En este caso, la celda unitaria es un prisma recto de base hexagonal. Las redes hexagonales tienen los tres parámetros de red correspondientes, cumpliendo la siguiente relación: a = b ≠ c. Siendo el ángulo entre el vector a y el b de 120º, tal como se muestra en la figura inferior. Mientras que entre los vectores a y c, así como entre el b y el c, se forman ángulos rectos. El número de átomos por celda se calculará de la siguiente manera: En cada una de las 2 bases del prisma hexagonal hay 6 átomos en los seis vértices. Cada uno de estos átomos ocupa ⅙ de la celda unitaria. En el centro de cada una de las 2 bases hexagonales hay 1 átomo que ocupa 1/2 celda unitaria. En las 6 caras laterales del prisma hexagonal hay 3 átomos, cada uno de los cuales ocupa ⅔ de la celda unitaria, y 3 átomos que ocupan cada uno ⅓ de volumen de la celda unitaria. (6 x ⅙ )x 2 + ½ x 2 + ⅔ x 3 + ⅓ x 3 = 6. La relación entre los parámetros de red a y b con el radio atómico R bajo el supuesto que todos los átomos son de igual radio y están en contacto es: a/R = b/R = 2.
Ejemplos de redes de Bravais
Los metales son los principales ejemplos de estructuras cristalinas y también las más simples porque generalmente constan de un solo tipo de átomo. Pero hay otros compuestos no metálicos que también forman estructuras cristalinas, como el diamante, el cuarzo y muchos otros.
- El hierro. El hierro tiene una celda unidad cúbica simple con parámetro de red o arista a = 0,297 nm. En 1 mm hay 3,48 x 10^6 celdas unitarias.
- El cobre. Tiene una estructura cristalina cúbica centrada en las caras, conformada únicamente por átomos de cobre.
- Gemas preciosas. Las gemas preciosas son estructuras cristalinas de básicamente un mismo compuesto, pero con pequeñas porciones de impurezas que muchas veces son las responsables del colorido de las mismas.
- Diamante. Está compuesto únicamente de carbono y no contiene impurezas, razón por la cual carece de color. El diamante tiene estructura cristalina cúbica (isométrico-hexoctaédrico) y es el material más duro conocido.
- Cuarzo. Está compuesto de óxido de sílice; generalmente es incoloro o blanco. Su estructura cristalina es trigonal-trapezoédrica.
- Rubí. Está compuesto de óxido de aluminio con impurezas de cromo que le dan su característico color rojo. Forma una red cristalina hexagonal.
- Zafiro. Es también un cristal de óxido de aluminio, pero con impurezas de titanio y hierro, responsables de su color azul en diversas tonalidades. Al igual que el rubí, tiene estructura hexagonal.
- Jade. Piedra preciosa generalmente de color verde, tiene estructura monoclínica y está compuesta de silicato de hierro-magnesio-calcio.
- Topacio. Es incoloro, con una estructura ortorrómbica de fluoruro de aluminio-hidróxido-silicato.
Ejercicios resueltos
Ejercicio 1
Hallar la relación entre el parámetro de red y el radio atómico para una red cúbica F.
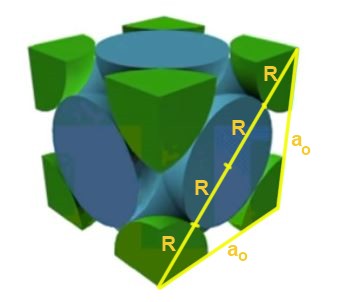
Solución: En primer lugar, se supone que los átomos se representan como esferas todas de radio R en “contacto” unas con otras, como se muestra en la figura. Se forma un triángulo rectángulo en el que se cumple que:
(4 R )^2 = a^2 + a^2 = 2 a^2
Por lo que se tiene que la relación arista-radio es:
a/R = 4/√2
Ejercicio 2
Hallar la relación entre el parámetro de red y el radio atómico para una red cúbica I (centrada en el cuerpo).
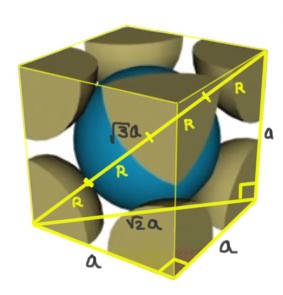
Solución: Se supone que los átomos se representan como esferas todas de radio R en “contacto” unas con otras, como se muestra en la figura.
Se forman dos triángulos rectángulos, uno de hipotenusa √2a y el otro de hipotenusa √3a, como puede demostrarse mediante el uso del teorema de Pitágoras. De allí se tiene que la relación entre el parámetro de red y el radio atómico para una red cúbica I (centrada en el cuerpo) es:
a/R = 4/√3
Ejercicio 3
Hallar el factor de empaquetamiento F para una celda unitaria de una estructura cúbica F (cúbica centrada en las caras) en la que los átomos tienen radio R y están en “contacto”.
Solución: El factor de empaquetamiento F se define como el cociente entre el volumen ocupado por los átomos en la celda unitaria y el volumen de la celda:
F = Vátomos / Vcelda
Como se demostró más arriba, el número de átomos por celda unitaria de una red cúbica centrada en las caras es 4, por lo que el factor de empaquetamiento será:
F = 4[4πR^3 /3]/[a^3] = …
… 4[4πR^3 /3]/[4R/√2]^3 = (√2)π/6 = 0,74
Referencias
- Crystal Structures Academic Resource Center. [PDF]. Recuperado de web.iit.edu.
- Crystals. Recuperado de thoughtco.com.
- Structures in Crystalline Solids. Recuperado de opentextbc.ca.
- Lattice Types Crystal Structures. Recuperado de crystalvisions-film.com.
- Kittel, C. Solid State Physics, Condensed matter Physics (8th edition). Wiley.