¿Qué es la lluvia ácida?
La lluvia ácida es la precipitación húmeda o seca de sustancias que generan un pH inferior a 5,6. Esta precipitación puede ser húmeda (diluidos en el agua de lluvia) o seca (deposiciones de partículas o aerosoles).
El término “lluvia ácida” fue propuesto por primera vez por el investigador inglés Robert Angus Smith en 1850, en plena Revolución industrial. Los ácidos más abundantes que se forman en la atmósfera son el nítrico y el sulfúrico por oxidación de contaminantes naturales o artificiales.
Los contaminantes más relevantes son los óxidos: NO2, NO3, SO2, cuyas fuentes naturales son erupciones volcánicas, incendios forestales y degradación bacteriana. Las fuentes artificiales son las emisiones de gases producto de la quema de combustibles fósiles (actividad industrial y tráfico automotor).
La lluvia ácida causa impactos negativos en el ambiente, como la acidificación de los suelos y aguas, afectando a los seres vivos, incluido el ser humano. Asimismo, los suelos y el agua se contaminan con metales pesados, y en los cuerpos de agua ocurre eutrofización.
A nivel de la vegetación, ocurren daños directos en las hojas que afectan el crecimiento de las plantas. Además, la acidificación del suelo inmoviliza los nutrientes y afecta las micorrizas (hongos del suelo). De igual forma, las edificaciones, maquinarias, monumentos y obras de arte expuestas a la intemperie se oxidan o erosionan gravemente por el efecto de los ácidos precipitados.
Para remediar el efecto de la lluvia ácida se pueden tomar algunas medidas puntales, como proteger los monumentos y corregir la acidificación de suelos y aguas. Sin embargo, la solución de fondo para la lluvia ácida es reducir la emisión de compuestos químicos precursores de la formación de ácidos.
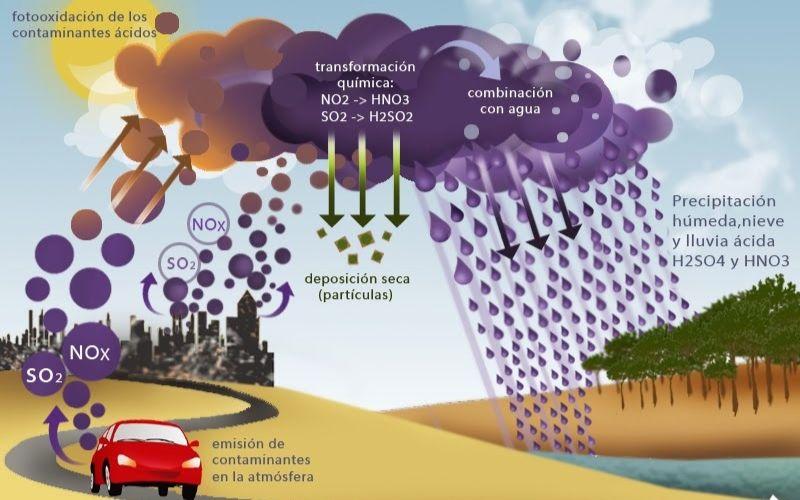
¿Cómo se forma la lluvia ácida?
- Agentes químicos precursores. Este fenómeno se inicia con la emisión a la atmósfera de compuestos químicos precursores de la formación de ácidos. Estos compuestos pueden ser emitidos por fuentes naturales o artificiales. Entre las fuentes naturales están las erupciones volcánicas, los incendios de vegetación y emisiones oceánicas. Como fuentes artificiales, actúan las emisiones industriales, de vehículos a motor de combustión o la quema de residuos. Estas fuentes emiten diversos compuestos que pueden generar ácidos en la atmósfera, pero los más importantes son los óxidos de nitrógeno y los óxidos de azufre. Los óxidos de nitrógeno son conocidos como NOx, e incluyen el dióxido de nitrógeno (NO2) y el óxido nitroso (NO). Por su parte el óxido de azufre es el SO2, o dióxido de azufre.
- Proceso troposférico y ácidos producidos. La lluvia ácida ocurre en la troposfera (zona atmosférica que va desde la superficie terrestre hasta una altura de 16 km). Allí, las corrientes de aire pueden llevar estos compuestos sobre cualquier parte del planeta, haciéndola un problema global. En ese proceso, los óxidos de nitrógeno y azufre interactúan con otros compuestos para formar ácido nítrico y ácido sulfúrico, respectivamente.
- Soporte de las reacciones. Las reacciones químicas pueden llevarse a cabo bien sea sobre partículas sólidas en suspensión o en gotas de agua en suspensión. El ácido nítrico se forma principalmente en la fase gaseosa, debido a su baja solubilidad en agua. Por su parte, el ácido sulfúrico es más soluble en agua, siendo el principal constituyente de la lluvia ácida.
- Ácido nítrico. Para la formación de ácido nítrico (HNO3) los óxidos de nitrógeno reaccionan con el agua, con radicales como el OH (en menor medida con HO2 y CH3O2), o con ozono troposférico (O3).
- Ácido sulfúrico. En la producción de ácido sulfúrico (H2SO4) participan igualmente los radicales OH, HO2, CH3O2, el agua y el ozono. Adicionalmente se puede formar reaccionando con el agua oxigenada (H2O2) y diversos óxidos metálicos.
- Ácido carbónico. El H2CO3 se forma gracias a la reacción fotoquímica del dióxido de carbono con el agua atmosférica.
- Ácido clorhídrico. El HCl representa solo un 2% de la lluvia ácida, y su precursor es el cloruro de metilo (ClCH3). Este compuesto proviene de los océanos y es oxidado por radicales OH para formar el ácido clorhídrico.
- Precipitación. Una vez que se han formado los compuestos ácidos (ácido nítrico o ácido sulfúrico, y en menor medida, ácido clorhídrico), estos precipitan. La precipitación puede ser por deposición de las partículas en suspensión en las que ha tenido lugar la reacción de acidificación en fase gaseosa. Otra manera es que en la lluvia precipite el agua condensada donde se formaron los ácidos.
Composición de la lluvia ácida
La acidez natural de la lluvia es cercana a un pH de 5,6, aunque en algunas áreas no contaminadas se han señalado valores de 5. Estos bajos valores del pH se han asociado a la presencia de ácidos de origen natural. Se considera que dependiendo del nivel de pH, la lluvia se puede clasificar en:
- Ligeramente ácida (pH entre 4,7 y 5,6).
- Medianamente ácida (pH entre 4,3 y 4,7).
- Fuertemente ácida (pH menor o igual a 4,3).
Si la lluvia tiene una concentración >1,3 mg/L de nitratos y >3 mg/L en el caso de sulfatos, se considera que la contaminación es alta.
La lluvia ácida está compuesta, en más de dos tercios de los casos, por la presencia de ácido sulfúrico, seguido en abundancia por el ácido nítrico. Otros componentes que pueden contribuir a la acidez de la lluvia son el ácido clorhídrico y el ácido carbónico.
Reacciones químicas de la lluvia ácida
Formación de ácido sulfúrico (H2SO4)
La producción de ácido sulfúrico puede ocurrir en fase gaseosa o en fase líquida.
Fase gaseosa
Solo el 3 o 4% del SO2 se oxida en fase gaseosa para producir ácido sulfúrico. Existen muchas rutas para la formación del ácido sulfúrico a partir de precursores gaseosos, aquí se muestra la reacción del SO2 con el ozono troposférico.
La reacción ocurre en dos etapas:
- El dióxido de azufre reacciona con el ozono troposférico generando trióxido de azufre y liberando oxígeno.
SO2 + O3 = SO3+O2
- Luego, el trióxido de azufre se oxida con el vapor de agua y produce ácido sulfúrico.
SO3 + H2O = H2SO4
Fase líquida
En las gotas de agua que formarán la lluvia puede producirse ácido sulfúrico por diversas vías:
- El SO2 se disuelve en agua generando ácido sulfuroso, y este es oxidado por el agua oxigenada:
SO2+H2O = H2SO2
H2SO2 +H2O2 = H2SO4 + H2O
- Mecanismo fotocatalítico: en este caso, partículas de óxidos metálicos (hierro, zinc, titanio) se activan gracias a la acción de la luz solar (activación fotoquímica) y oxidan el SO2 generando ácido sulfúrico.
Formación de ácido nítrico (HNO3)
El ozono troposférico O3 produce la transformación de NO2 a HNO3 en un proceso de tres etapas:
- NO2+ O3 = NO3 + O2
- NO3 + NO2 = N2O5
- N2O5 + H2O = 2HNO3
Efectos de la lluvia ácida en el ambiente

- Acidificación de los suelos y sus efectos en la vegetación. El efecto de la lluvia ácida en el suelo varía dependiendo de la composición del mismo. Por ejemplo, los suelos de origen calcáreo, basáltico e ígneo, tienen mayor capacidad para neutralizar la acidez. Por su parte, los suelos ricos en cuarzo como material inerte no son capaces de regular el contenido de ácidos. Así, en los suelos en que la lluvia ácida incrementa la acidez, se liberan y arrastran iones metálicos tóxicos para plantas y animales. Un caso relevante es la disolución de aluminosilicatos, que liberan iones de aluminio muy dañinos para la vegetación. En general, la acidez del suelo disminuye la disponibilidad de nutrientes para las plantas. Además, promueve la liberación y lavado del calcio, lo que provoca deficiencias en plantas.
- Efecto en los acuíferos y la salud humana. En la mayoría de los casos, la lluvia ácida no tiene apariencia o sabor distinto a la lluvia normal, ni genera sensaciones en la piel. Sus efectos en la salud humana son indirectos, y rara vez causa daños en la piel por acidez extrema. Uno de los problemas de la lluvia ácida es que al disminuir los valores de pH por debajo de 5, se liberan y arrastran metales pesados. Estos contaminantes, como el aluminio y el cadmio, pueden pasar a los acuíferos subterráneos. Si el agua de estos acuíferos contaminados pasa a pozos utilizados para el consumo humano, puede causar graves daños a la salud.
- Deterioro de construcciones, monumentos y materiales. La lluvia ácida puede deteriorar irreversiblemente monumentos y construcciones, dañándolas. Las que están hechas en piedra caliza o mármol se ven gravemente afectadas. En el caso de la piedra caliza, la lluvia ácida causa la disolución de la caliza y genera la recristalización de la calcita. Esta recristalización produce tonos blanquecinos en la superficie. El mármol, aunque es más resistente, también se ve afectado por la lluvia ácida. En este caso, se produce la exfoliación de la piedra, por lo que se desprenden capas superficiales de la misma. En el caso de los metales, causa corrosión porque se oxidan. Esto genera enormes pérdidas económicas, ya que las estructuras, equipos, maquinarias y vehículos con piezas metálicas se ven seriamente afectados.

Soluciones para los efectos de la lluvia ácida
- Reducir las emisiones. La solución de fondo para la lluvia ácida es reducir las emisiones de sustancias químicas precursoras de ácidos. Las más importantes son los óxidos de azufre y de nitrógeno. Existen algunas alternativas tecnológicas que pueden ayudar a reducir las emisiones. Por ejemplo, en la industria los llamados “lechos fluidizados” incorporan absorbentes (caliza o dolomita) que retienen el SO2. En el caso de los vehículos a motor y, en general, los motores de combustión, los convertidores catalíticos ayudan igualmente a reducir las emisiones de SO2. Algunos países han implementado programas específicos de reducción de la lluvia ácida, como Estados Unidos, que desarrolló el Programa Nacional de Evaluación de Precipitación Ácida (NAPAP por sus siglas en inglés). Entre alguna de las medidas que contempla el NAPAP, está implementar el uso de combustibles bajos en azufre. Otra medida es la sustitución del parque automotor por coches eléctricos para reducir tanto la lluvia ácida como el calentamiento global. No obstante, aunque existe la tecnología para conseguir esto, la presión de la industria automotriz y la petrolera han retrasado decisiones al respecto.
- Aplicar medidas de corrección de acidez. En algunos casos se puede aumentar el pH de suelos y aguas agregando álcalis, por ejemplo, incorporando grandes cantidades de cal. Sin embargo, esta práctica no es factible en extensiones de terreno muy grandes.
- Protección de superficies
- Piedra. Existen diversos métodos para proteger o disminuir el deterioro de la piedra bajo el efecto de la lluvia ácida. Uno de estos métodos es lavarla con vapor o agua caliente. También se pueden usar agentes químicos, como ácido fluorhídrico o bifluoruro de amonio. Una vez lavada, la piedra se puede sellar aplicando productos especiales que taponan los poros, como el hidróxido de bario.
- Metal. Las superficies metálicas susceptibles de corroerse pueden protegerse recubriéndolas con un metal no corrosivo, como el zinc. Para esto, se puede aplicar electrodeposición, o sumergir la estructura metálica en el metal protector en estado líquido.
Referencias
- Espada, L. y A. Sánchez. Influencia de la lluvia ácida en la corrosión de los metales. Universidad de la Coruña. Servizo de Publicacións. La Coruña, España.
- Likens, G.E., C.T. Driscoll and D.C. Buso. Long-Term Effects of Acid Rain: Response and Recovery of a Forest Ecosystem. Science,.
- Schindler, D.W. Effects of Acid Rain on Freshwater Ecosystems. Science.